Содержание
- 2. Определения и понятия Растворы – это гомогенные термодинамически устойчивые системы, состоящие из 2-х и более веществ,
- 3. Определения и понятия Растворимость – это способность вещества растворяться в том или ином растворителе. Растворитель –
- 4. Растворимость Количественно растворимость (Р) выражают отношением массы вещества (г) к объему или массе растворителя (л). Р=m(вещества)/V(растворителя)
- 5. Физическая теория образования растворов. Основоположниками данной теории являются Аррениус, Оствальд и Вант-Гофф. Эти ученые рассматривали процесс
- 6. Химическая теория образования растворов Основные тезисы химической теории были представлены в 1887 году Д.И. Менделеевым. В
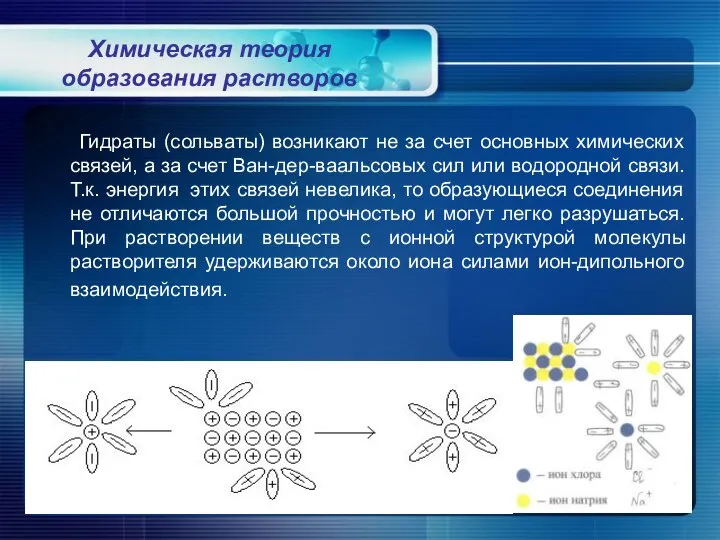
- 7. Гидраты (сольваты) возникают не за счет основных химических связей, а за счет Ван-дер-ваальсовых сил или водородной
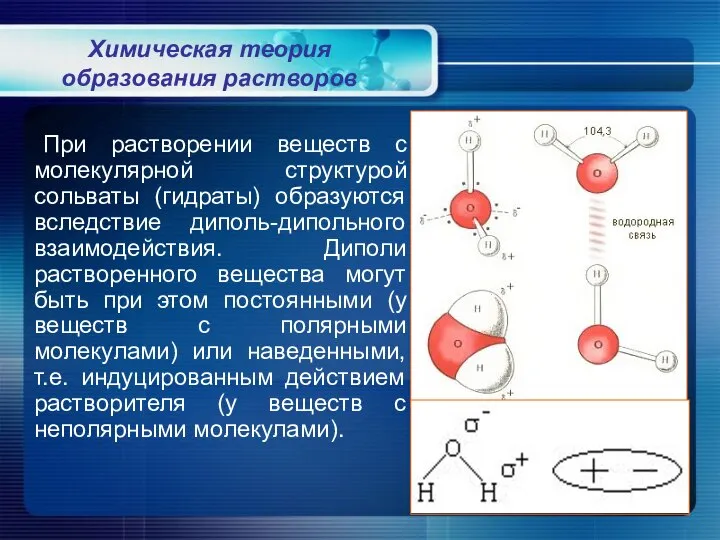
- 8. При растворении веществ с молекулярной структурой сольваты (гидраты) образуются вследствие диполь-дипольного взаимодействия. Диполи растворенного вещества могут
- 9. Современная теория образования растворов Современная теория растворения объединяет физическую и химическую теории и рассматривает растворение, как
- 10. Современная теория образования растворов Стадия гидратации экзотермическая, а стадия растворения эндотермическая. Общий тепловой эффект процесса состоит
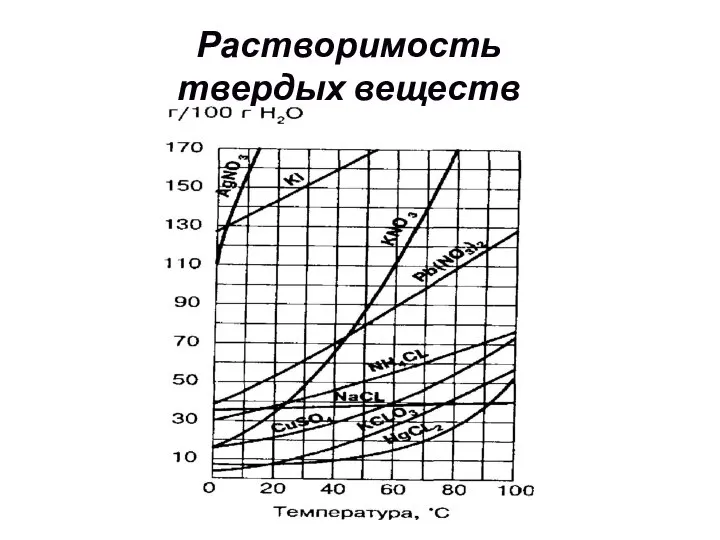
- 11. Растворимость твердых веществ
- 12. Как правило с повышением температуры растворимость большинства твердых веществ повышается. При осторожном охлаждении таких систем получают
- 13. Растворимость газов На растворимость газов в жидкостях оказывает влияние температура и давление. Зависимость растворимости газов от
- 14. Способы выражения концентрации 1. Массовая доля W – это отношение массы растворенного вещества (m в-ва) к
- 15. Способы выражения концентрации 3. Молярная концентрация (См) показывают какое количество вещетва (n) растворено в 1 л
- 16. Способы выражения концентрации 6. Титр (Т) показывает сколько граммов вещества (m в-ва) растворено в 1 мл
- 17. Формулы перехода для бинарных растворов Формулы пересчета молярной концентрации в молярную концентрацию эквивалента и наоборот 1.
- 18. Формулы пересчета массовой доли в молярную концентрацию и в молярную концентрацию эквивалента Формулы перехода для бинарных
- 19. Зависимость между титром и молярной концентрацией эквивалента Формулы перехода для бинарных растворов
- 20. Классификация растворов По агрегатному состоянию: Газообразные (воздух – N2+O2+He+CO2) Жидкие (NaOH+H2O; NaCl + H2O) Твердые (сплавы
- 21. Классификация растворов 3. Растворы делят на насыщение, не насыщенные и пересыщенные Насыщенные растворы это растворы в
- 22. Дисперсные системы Дисперсные системы это гетерогенные системы, которые характеризуются дисперсностью. Дисперсность – это величина, обратная размеру
- 23. Идеальные растворы Раствор состоит из растворенного вещества (А) и растворителя(В) Между одноименными молекулами, а также между
- 24. Закон Рауля. Коллигативные свойства растворов. Ф. Рауль установил, что: Для идеальных (разбавленных) растворов давление насыщенного пара
- 25. Закон Рауля. Коллигативные свойства растворов. Вторая формулировка данного закона: Относительное понижение давления насыщенного пара растворителя над
- 26. Коллигативные свойства растворов. Эбулиоскопия. Коллигативные свойства характерны для растворов не электролитов. К данным свойствам относят также
- 27. Криоскопия Уменьшение давления насыщенного пара над раствором приводит к понижению температуры его замерзания. Другими словами температура
- 28. Осмос. Осмотическое давление. Процесс диффузии вещества через полунепроницаемую мембрану называют осмосом. А то давление, которое необходимо
- 29. Закон Вант-Гоффа – Пфефера Осмотическое давление раствора равно такому давлению, которое имело бы растворенное вещество, если
- 30. Закон Вант-Гоффа – Пфефера В растворах электролитов количество частиц в единице объема раствора больше, так как
- 31. Изотоничность Кровь, лимфа и другие тканевые жидкости организма человека имеют осмотическое давление приблизительно 800 кПа., такое
- 33. Скачать презентацию



























 СПИРТЫ
СПИРТЫ  Круговорот углерода в природе. Изготовлено: А.С.Большаков
Круговорот углерода в природе. Изготовлено: А.С.Большаков Контроль в процессе обучения химии на старшей ступени школы
Контроль в процессе обучения химии на старшей ступени школы Лед – как состояние воды
Лед – как состояние воды Презентация по Химии "Средства для борьбы с насекомыми" - скачать смотреть
Презентация по Химии "Средства для борьбы с насекомыми" - скачать смотреть 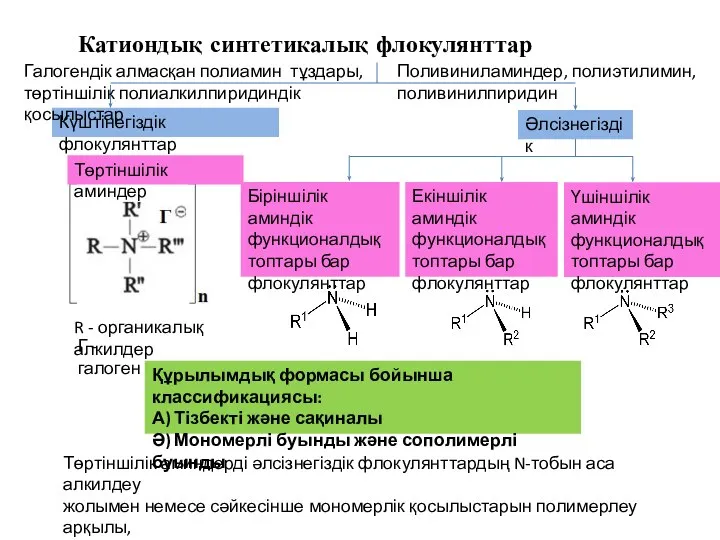 Катиондық синтетикалық флокулянттар
Катиондық синтетикалық флокулянттар Кислоты: классификация, реакции, применение
Кислоты: классификация, реакции, применение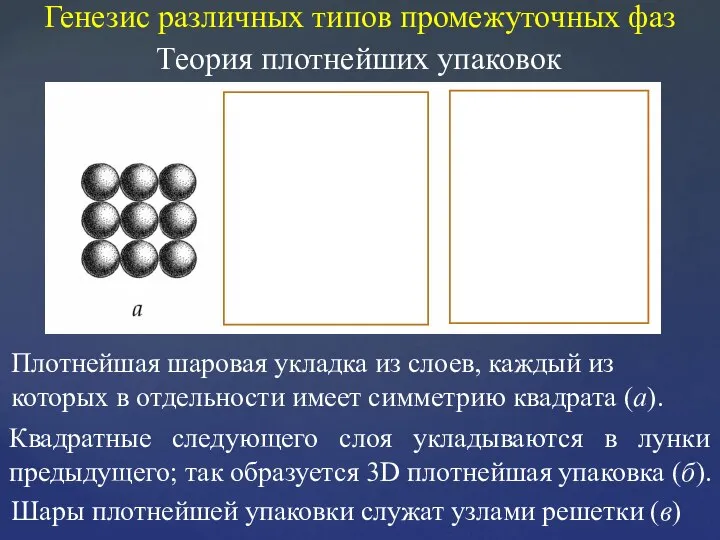 Генезис различных типов промежуточных фаз. Теория плотнейших упаковок
Генезис различных типов промежуточных фаз. Теория плотнейших упаковок Що ховається за цифрами? Харчові домішки
Що ховається за цифрами? Харчові домішки Добування кисню та вивчення його властивостей
Добування кисню та вивчення його властивостей Химия и физика пигментов
Химия и физика пигментов Поліетелен Застосування поліетилену Автор Фурка Т.А.
Поліетелен Застосування поліетилену Автор Фурка Т.А.  Уравнения химической реакции 8 класс
Уравнения химической реакции 8 класс Карбонатна кислота. Карбонати. Підготувала: Учениця 10 класу Прилуцької ЗОШ І-ІІІ ст. № 13 Імені Святителя Іоасафа Бєлгородсько
Карбонатна кислота. Карбонати. Підготувала: Учениця 10 класу Прилуцької ЗОШ І-ІІІ ст. № 13 Імені Святителя Іоасафа Бєлгородсько Изомерия органических соединений. 10 класс
Изомерия органических соединений. 10 класс Эмульгаторы. Коллоиды. Гелеобразующие и увлажняющие вещества в косметическом производстве
Эмульгаторы. Коллоиды. Гелеобразующие и увлажняющие вещества в косметическом производстве Кислоты. Состав кислот
Кислоты. Состав кислот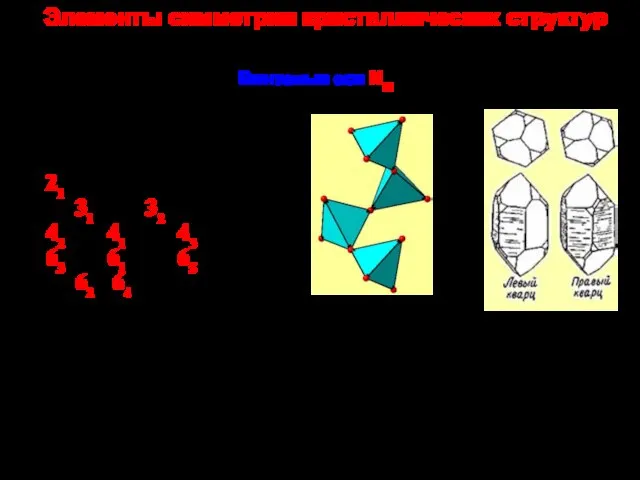 Элементы симметрии кристаллических структур
Элементы симметрии кристаллических структур Аналитическая химия Преподаватель Ельчищева Юлия Борисовна
Аналитическая химия Преподаватель Ельчищева Юлия Борисовна  Торий
Торий Характеристика и свойства истинных растворов
Характеристика и свойства истинных растворов Химические формулы. Атомная и молекулярная массы
Химические формулы. Атомная и молекулярная массы Энергетический обмен
Энергетический обмен Основные классы неорганических соединений
Основные классы неорганических соединений Обмен липидов
Обмен липидов Сложные вопросы ЕГЭ по химии
Сложные вопросы ЕГЭ по химии Гидроксид аммония
Гидроксид аммония Производные аминоалкилбензолов. (Тема 3)
Производные аминоалкилбензолов. (Тема 3)