Содержание
- 2. Положение металлов в периодической системе химических элементов Д.И.Менделеева 19.04.2016 Соколова О.Е. Группы элементов VII VIII Периоды
- 3. Особенности строения атомов металлов 11 Na 20 Са 26 Fe 19.04.2016 2е 8е 1е 2е 8е
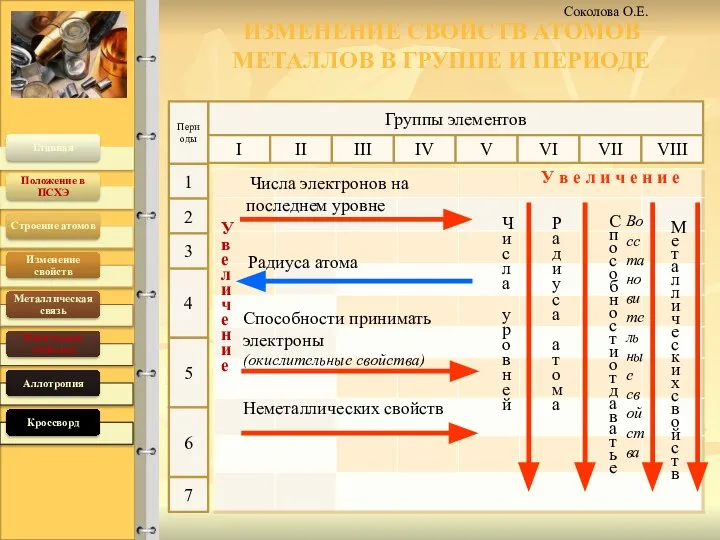
- 4. 19.04.2016 Соколова О.Е. ИЗМЕНЕНИЕ СВОЙСТВ АТОМОВ МЕТАЛЛОВ В ГРУППЕ И ПЕРИОДЕ Группы элементов Увеличение У в
- 5. Металлическая связь – это особый тип связи в металлах и сплавах между атомами и ионами металлов
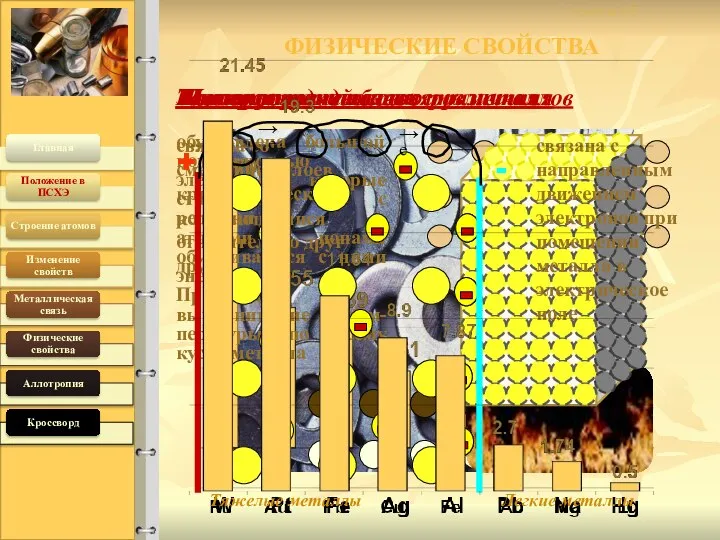
- 6. Металлический блеск 19.04.2016 Температура плавления различная Плотность металлов различная связана со смещением слоев кристаллической решетки относительно
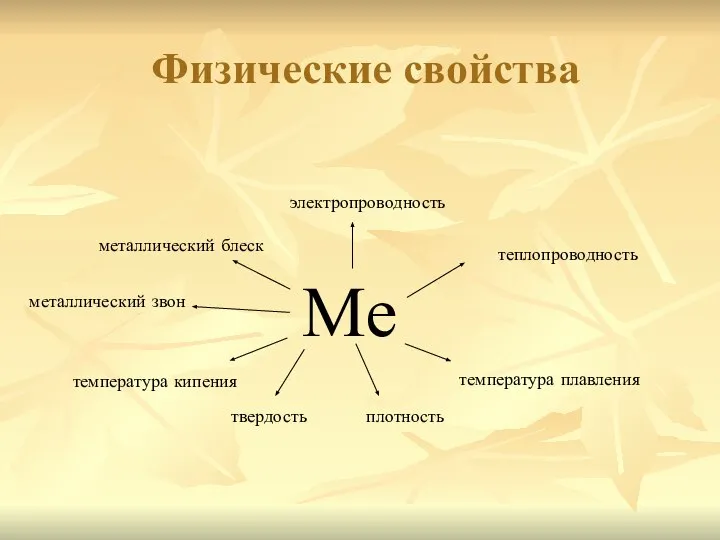
- 7. Физические свойства
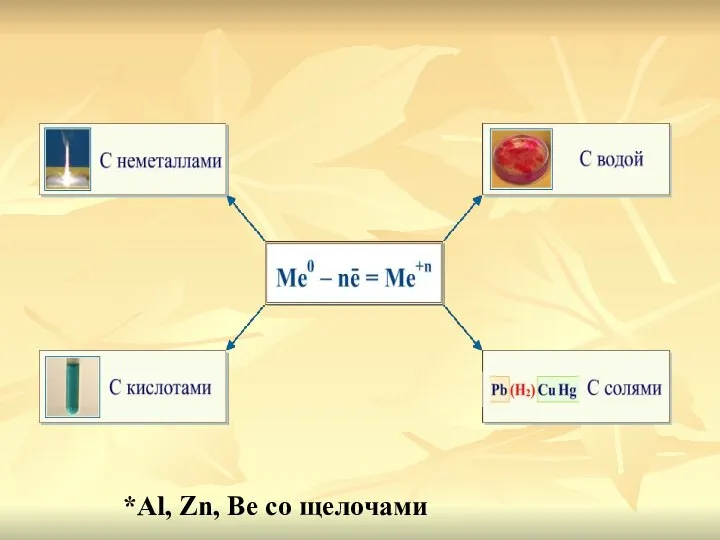
- 8. *Al, Zn, Be cо щелочами
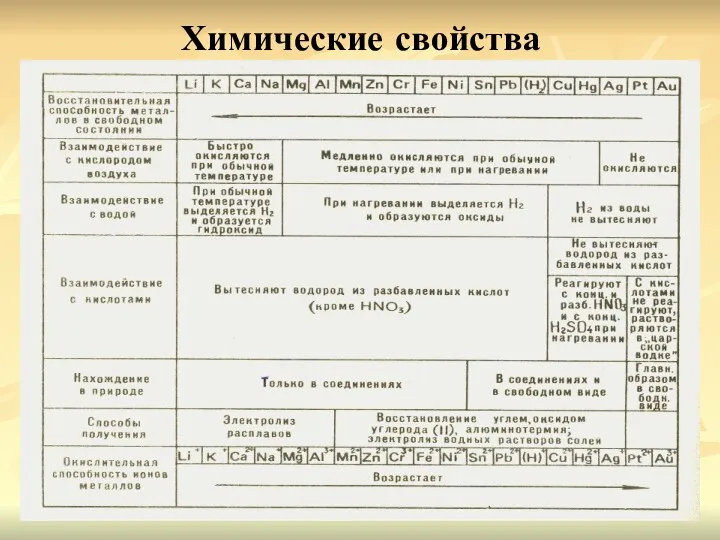
- 9. Химические свойства
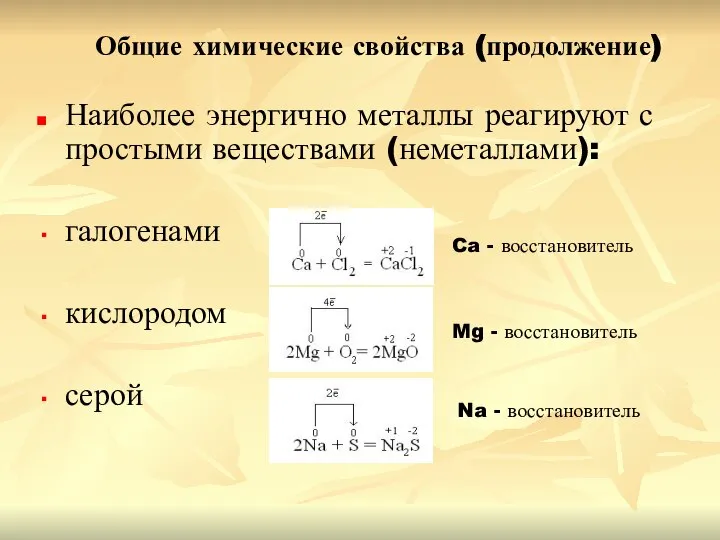
- 10. Общие химические свойства (продолжение) Наиболее энергично металлы реагируют с простыми веществами (неметаллами): галогенами кислородом серой Ca
- 11. Химические свойства металлов Взаимодействие с неметаллами: с кислородом с серой с галогенами
- 12. Общие химические свойства (продолжение) Металлы могут окисляться также ионами водорода и ионами других металлов. Металлы реагируют
- 13. Взаимодействие со сложными веществами: с водой
- 14. Взаимодействие c растворами кислот
- 15. Взаимодействие с растворами солей Каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в
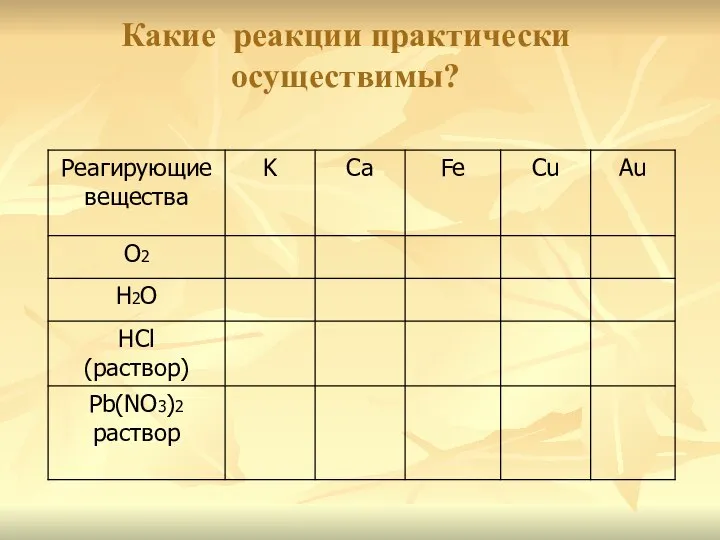
- 16. Какие реакции практически осуществимы?
- 18. Скачать презентацию








 Ионная химическая связь
Ионная химическая связь Ароматические углеводороды
Ароматические углеводороды Комплексные соединения
Комплексные соединения Контроль в процессе обучения химии на старшей ступени школы
Контроль в процессе обучения химии на старшей ступени школы Презентація по хімії на тему:БУДІВЕЛЬНІ МАТЕРІАЛИ
Презентація по хімії на тему:БУДІВЕЛЬНІ МАТЕРІАЛИ  Урок по химии в 10 классе по теме Каучуки
Урок по химии в 10 классе по теме Каучуки Углеводы. Глюкоза
Углеводы. Глюкоза Алюминий и его свойства
Алюминий и его свойства Массовая и объемная доля компонентов смеси
Массовая и объемная доля компонентов смеси Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Гликозилирование, эффективная синтетическая стратегия для повышения биодоступности терапевтических пептидов
Гликозилирование, эффективная синтетическая стратегия для повышения биодоступности терапевтических пептидов Интересные факты о нефти
Интересные факты о нефти Фармацевтические суспензии и эмульсии
Фармацевтические суспензии и эмульсии Бальзам-ополаскиватель для волос
Бальзам-ополаскиватель для волос Углеводы. Структура
Углеводы. Структура Внеурочная работа по химии. Краеведение
Внеурочная работа по химии. Краеведение Химия элементов. Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе
Химия элементов. Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе Решение задач на вывод формул органических веществ относительно плотности
Решение задач на вывод формул органических веществ относительно плотности Обмен белков - 1
Обмен белков - 1 Мембранные липиды: строение и функции
Мембранные липиды: строение и функции Cтроение и спектры молекул
Cтроение и спектры молекул L’introduction a la biochimie. La structure et les proprietes des proteines
L’introduction a la biochimie. La structure et les proprietes des proteines Углерод. Нахождение в природе
Углерод. Нахождение в природе Интернет-тренажеры
Интернет-тренажеры Исследование химических моделей (11 класс)
Исследование химических моделей (11 класс) Окислительные методы получения органических соединений
Окислительные методы получения органических соединений Презентация по Химии "Вода - найдивовижніша речовина в світі" - скачать смотреть бесплатно
Презентация по Химии "Вода - найдивовижніша речовина в світі" - скачать смотреть бесплатно Фотосинтез. Суммарное уравнение, общий вид
Фотосинтез. Суммарное уравнение, общий вид