Содержание
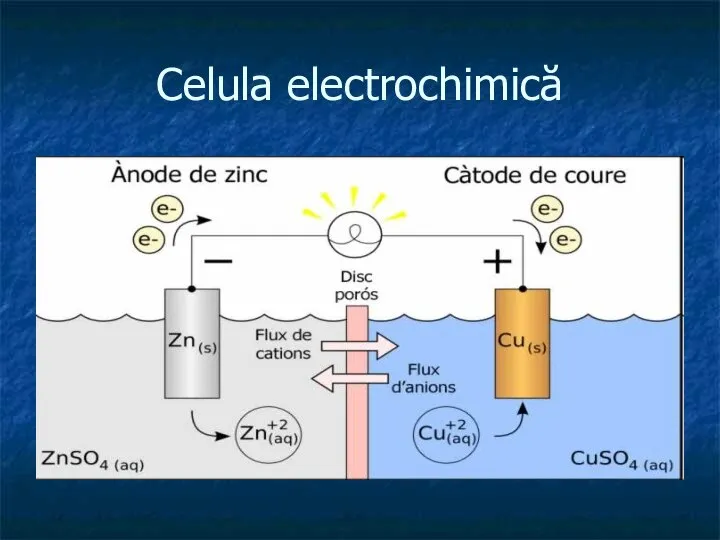
- 2. Celula electrochimică
- 3. Metode electrochimice Generalităţi Parametrii metodelor electrochimice - bazate pe astfel de reacţii - sunt legaţi de
- 4. Metode electrochimice Generalităţi Oricare ar fi parametrul măsurat, acesta poate fi corelat cu concentraţia speciilor chimice
- 5. Metode electrochimice Generalităţi Unele dintre metode, care măsoară tot curentul însă în condiţii de tensiune variabilă
- 6. Metode electrochimice Generalităţi Toate metodele utilizează în procesul de măsurare doi sau trei electrozi scufundaţi în
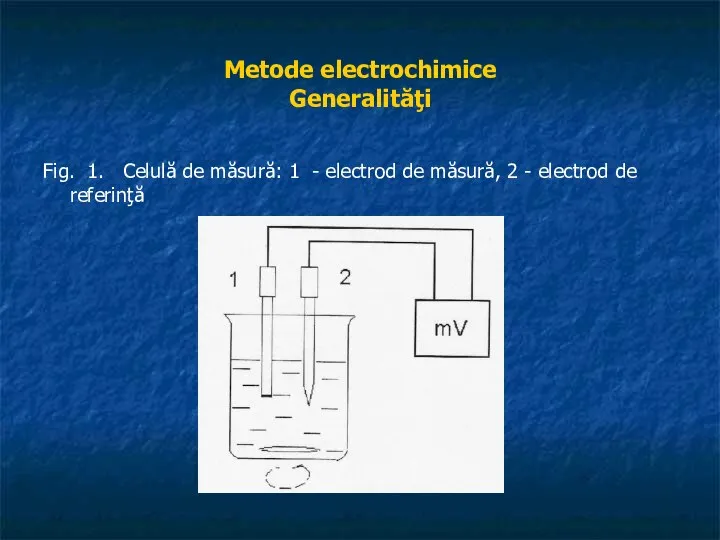
- 7. Metode electrochimice Generalităţi Fig. 1. Celulă de măsură: 1 - electrod de măsură, 2 - electrod
- 8. Metode electrochimice Generalităţi Titrările electrochimice utilizează măsurătorile unor parametri electrochimici pentru găsirea punctului de echivalenţă dintr-o
- 9. Metode electrochimice Generalităţi În cadrul acestor metode, se determină potenţialul electric la curent nul (forţa electromotoare),
- 10. Metode electrochimice Generalităţi Se cunosc două metode principale: potenţiometria directă titrările potenţiometrice
- 11. Metode electrochimice Generalităţi Potenţiometria directă este mult folosită în practică întrucât semnalul se pretează la o
- 13. Metode electrochimice Generalităţi Titrările potenţiometrice, mai utilizate în laboratoare datorită simplităţii, preţului de cost scăzut, preciziei
- 14. Metode electrochimice Generalităţi Reprezentarea electrozilor în cadrul textelor tehnice se face prin prezentarea formulelor chimice ale
- 15. Metode electrochimice Generalităţi Uneori unul dintre electrozi este separat de soluţie printr-o diafragmă. În acest caz
- 16. Titrări potenţiometrice Aceste metode măsoară o specie chimică pe baza unei reprezentări a potenţialului unui electrod,
- 17. Titrări potenţiometrice Ecuaţia lui Nernst
- 18. Ecuaţia lui Nernst ε - este potenţialul de electrod, εo - potenţialul normal standard, R -
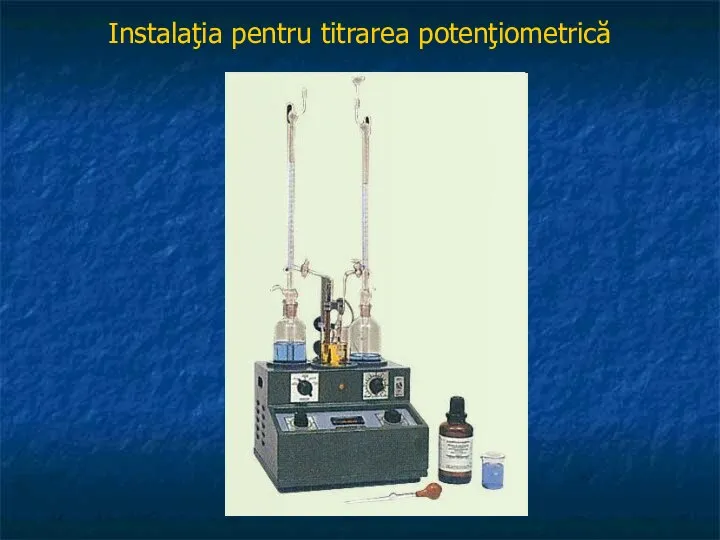
- 19. Instalaţia pentru titrarea potenţiometrică
- 20. Fig. Curbe de titrare potenţiometrică
- 21. Tipuri de electrozi Electrozii de speţa 1-a Metal, ion metalic sau M|Mz+; pe care are loc
- 22. Electrozii de speţa 1-a
- 23. Electrozii de speţa 1-a
- 24. Electrozii de speţa 1-a cu echilibrul pe electrod: H+(aq) + e- ↔ 1/2 H2(g) (1 atm
- 25. Electrodul de hidrogen (Pt)H2 | H+
- 26. Electrozii de speţa 1-a Electrodul de hidrogen Ecuaţia potenţialului de electrod se poate exprima:
- 27. Electrozii de speţa 1-a Electrodul de hidrogen Dar, cum în situaţia considerată - standard - prin
- 28. Electrozii de speţa a 2-a sunt formaţi prin asocierea a două straturi: metal/sare greu solubilă a
- 29. Electrozii de speţa a 2-a argint/clorură de argint Electrodul de argint/clorură de argint, cu formula electrochimică:
- 30. Electrod AgCl
- 31. Electrozii de speţa a 2-a de calomel Electrodul de calomel, care este format din contactul: mercur
- 32. Electrod de calomel
- 33. Electrozii de speţa a 3-a sunt formaţi dintr-un metal, pe care se află depuse două combinaţii
- 34. Electrozii de speţa a 3-a De exemplu, un astfel de electrod este redat de lanţul: Pb
- 35. Electrozii redox sunt electrozi compuşi din metale nobile scufundaţi în soluţia a două specii chimice, aflate
- 36. Electrozii redox O schemă generală de reprezentare a acestor electrozi este: Pt | Ox; Red sau
- 37. Electrozii redox
- 38. Electrozii membrana ion selectivi electrodul de sticlă Utilizarea sa se bazează pe faptul că potenţialul existent
- 39. Electrod de sticlă
- 40. Electrozii membrana ion selectivi electrodul de sticlă Simbolurile (1) şi (2) reprezintă respectiv: (1) - specia
- 41. Electrozii membrana ion selectivi electrodul de sticlă Considerându-se concentraţia (cea din interiorul electrodului de sticlă) constantă,
- 42. electrozi membrană ion selectivi Orice fază neapoasă, prezentând conducţie ionică, interpusă între 2 soluţii apoase constituie
- 43. electrozi membrană ion selectivi Feţele membranei trebuie sa aibă un rol de schimbător de ioni. Asemănător
- 45. Скачать презентацию







































 Коллоидное состояние вещества
Коллоидное состояние вещества Презентация по Химии "Спирты" - скачать смотреть _
Презентация по Химии "Спирты" - скачать смотреть _ Вторая фаза метаболизма ксенобиотиков и эндогенных соединений
Вторая фаза метаболизма ксенобиотиков и эндогенных соединений Диаграмма состояния железо–углерод
Диаграмма состояния железо–углерод Непредельные углеводороды
Непредельные углеводороды Алкены.10 класс
Алкены.10 класс Сплавы. Свойства сплавов
Сплавы. Свойства сплавов Химическая технология органических веществ
Химическая технология органических веществ Алкины
Алкины Начало нанотехнологической эры. Фуллерены
Начало нанотехнологической эры. Фуллерены Фазовое равновесие в насыщенном растворе малорастворимого электролита
Фазовое равновесие в насыщенном растворе малорастворимого электролита Инсулин гормон жизни
Инсулин гормон жизни  Роль химии в сохранении окружающей среды
Роль химии в сохранении окружающей среды Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии
Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии Презентация по Химии "Органическая химия" - скачать смотреть
Презентация по Химии "Органическая химия" - скачать смотреть  Коллоидная химия
Коллоидная химия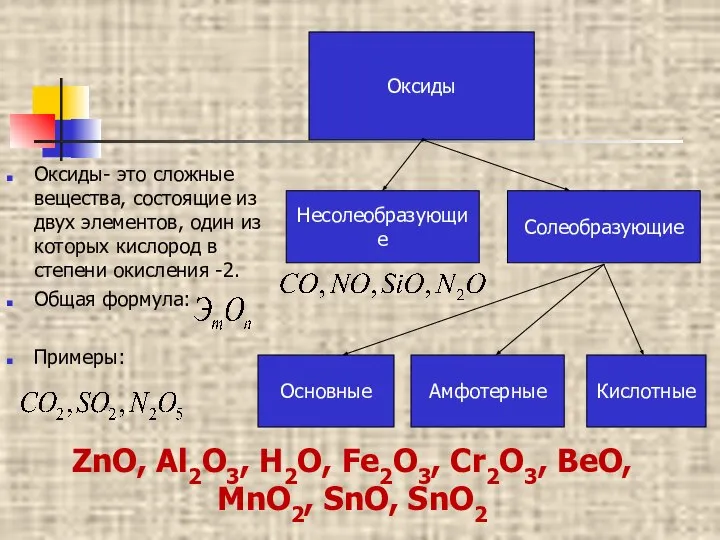 Оксиды. Классификация неорганических веществ
Оксиды. Классификация неорганических веществ Выявление уровня токсичности почв пришкольного участка и прилежащих к нему территорий
Выявление уровня токсичности почв пришкольного участка и прилежащих к нему территорий Технология кварцевого стекла
Технология кварцевого стекла Химиялық тепе-теңдік
Химиялық тепе-теңдік Біохімічний склад кормів - первинний показник їх технологічної й продуктивної можливості
Біохімічний склад кормів - первинний показник їх технологічної й продуктивної можливості Стекла. Структура и свойства
Стекла. Структура и свойства Емтихан сұрақтары
Емтихан сұрақтары Методы разделения белковых смесей. Электрофорез
Методы разделения белковых смесей. Электрофорез Косметические средства. Виды, состав и влияние на организм
Косметические средства. Виды, состав и влияние на организм Зависимость стадии конверсии метана от технологических параметров процесса в производстве метанола
Зависимость стадии конверсии метана от технологических параметров процесса в производстве метанола Получение этилена и изучение его свойств
Получение этилена и изучение его свойств Классификация неорганических веществ. Степень окисления
Классификация неорганических веществ. Степень окисления