Содержание
- 2. Методы и задачи аналитического контроля Классификация методов анализа в зависимости от количества анализируемого вещества Выбор метода
- 3. Средняя проба – это небольшое, взятое из общей массы количество вещества, средней состав которого идентичен среднему
- 4. Методы переведения пробы в раствор Растворение галогенводородными кислотами Для растворения минералов, содержащих графит, кварц и другие
- 5. Царская водка: HCl+HNO3=3:1 3HCl + HNO3 = NOCl + Cl2 + 2H2O
- 6. Растворение кислородсодержащими кислотами Серная кислота (H2SO4) В концентрированном состоянии – окислитель. В процессе окисления H2SO4 восстанавливается
- 7. Растворение металлов
- 8. Растворение сплавов
- 9. Методы разделения и концентрирования Осаждение как химический метод разделения. Осаждение считается полным, когда в растворе остается
- 10. Соосаждение 1. Адсорбционное – соосаждение возникает за счет сил адсорбции на поверхности осадка, создаваемых вследствие возникающего
- 11. Другие способы разделения многокомпонентных систем Отгонка Термообработка с образованием газообразных продуктов СаСО3 + 2Н + →
- 12. Гравиметрический (весовой) метод анализа Наиболее распространенные методы весового анализа основаны на выделении определяемого компонента в виде
- 13. Растворимость осадков в присутствии избытка (осадителя) общих ионов 1. Избыток осадителя может вызвать осаждение не только
- 14. Вычисление растворимости осадков, исходя из величины ПР Ca3(PO4)2 ↔ 3Ca2+ + 2PO43- ПРCa3(PO4)2 = [Ca2+]3 ⋅[PO43-]2
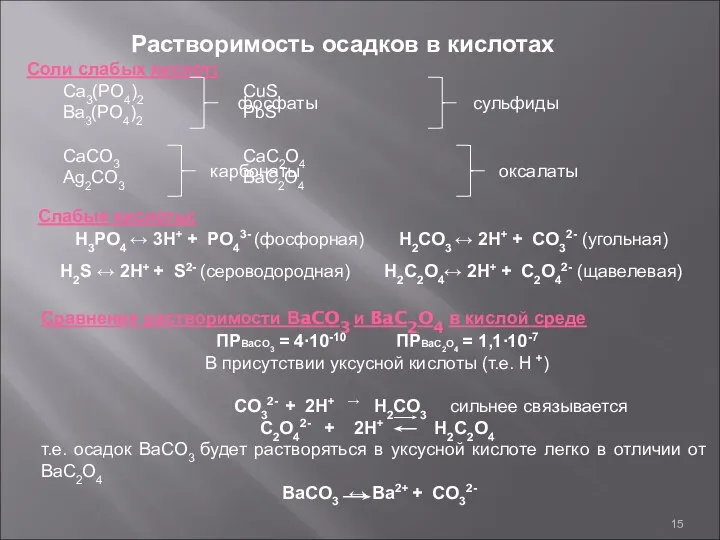
- 15. Растворимость осадков в кислотах Соли слабых кислот: Ca3(PO4)2 CuS Ba3(PO4)2 PbS CaCO3 CaC2O4 Ag2CO3 BaC2O4 фосфаты
- 16. Зависимость растворимости осадков от состава смесей водных и неводных растворителей Растворимость K[PtCl4] в граммах на 100г
- 17. Условия осаждения и промывания осадков Выбор осадителя: наилучшим осадителем обычно является тот, который образует наименее растворимый
- 18. Титрометрический (объемный) метод анализа N – нормальная концентрация: количество г-экв. вещества, содержащегося в 1л. раствора. Например:
- 19. Вычисления в объемном анализе Закон эквивалентов: N 1∙V1 =N2 ∙V2; Na2CO3 + 2HCl → H2CO3 +
- 20. БУФЕРНЫЕ РАСТВОРЫ
- 21. Зависимость окраски индикатора от рН среды 21
- 22. ИНТЕРВАЛ ПЕРЕХОДА ОКРАСКИ ИНДИКАТОРА Метиловый оранжевый желтый красный раствор оранжевый 1) 2) 3) 4)
- 23. Показатели титрования индикатора (рТ) Титрование слабых оснований Выбрать индикатор для титрования 0,1N NH4OH 0,1 N рабочим
- 24. Кривые титрования Титрование сильной кислоты сильным основанием HCl + NaOH→ NaCl + H2O
- 25. Титрование многоосновных кислот и их солей Для 0,1 М раствора 1) Na2CO3 + HCl → NaHCO3
- 26. Неводное кислотно – основное титрование Смесь МУХК и НСl КCH2ClCOOH = 1,4∙10-3 (МУХК) в водном растворе.
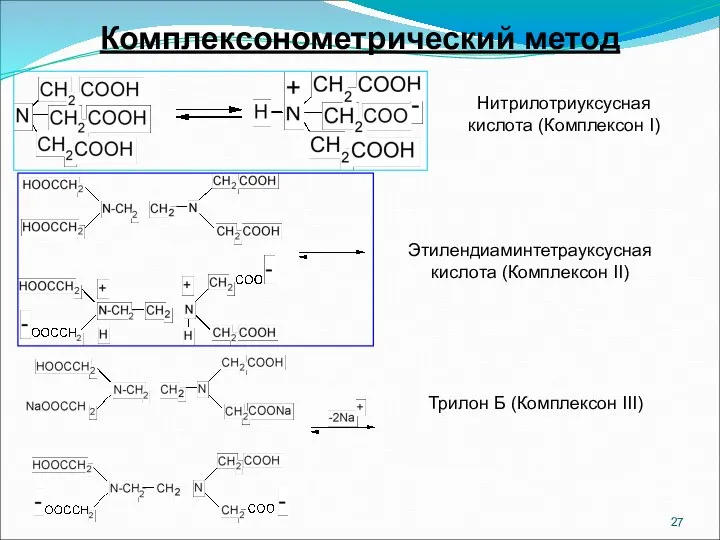
- 27. Комплексонометрический метод Нитрилотриуксусная кислота (Комплексон I) Этилендиаминтетрауксусная кислота (Комплексон II) Трилон Б (Комплексон III)
- 29. Типы реакций используемых в комплексонометрии Комплексон II 1.Реакции прямого воздействия иона металла с комплексоном 2.Реакции взаимодействия
- 30. Другие комплексоны 1-фенилиминодиуксусная кислота 2-оксифенилиминодиуксусная кислота 2-окси-5-метилфенилиминодиуксусная кислота
- 31. ИНДИКАТОРЫ Эриохром черный Т (производное диоксиазонафталина) Образует соединения синего цвета с ионами: Cu2+, Mg2+, Zn2+, Mn2+,
- 32. Определение жесткости воды Индикатор: эриохром черный Т или хром темно-синий Титрант: комплексон II, N=0,05 Буферный раствор:
- 33. Методы окисления - восстановления (Reduction-Oxidation, Red - Ox) K2Cr2O7 + 6FeCl3 + 14 HCl →2CrCl3 +
- 34. 1. Значения Е0 относятся к определенным условиям среды: MnO4- + 8H+ + 5ē↔Mn2+ + 4H2O, Е0
- 35. Е, В V, 0,1N р-ра V5+, мл Кривые титрования Fe2+ + V5+ → Fe3+ + V4+
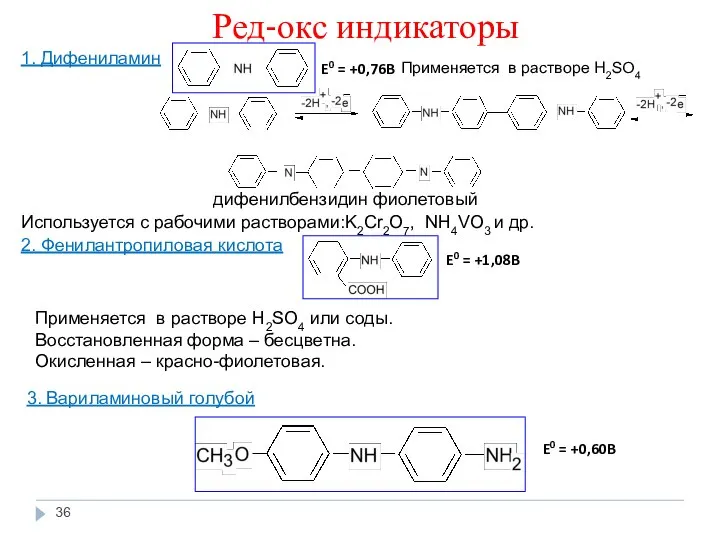
- 36. Ред-окс индикаторы 1. Дифениламин дифенилбензидин фиолетовый Используется с рабочими растворами:K2Cr2O7, NH4VO3 и др. 2. Фенилантропиловая кислота
- 37. Перманганатометрия MnO4- + 8H+ + 5ē ↔ Mn2+ + 4H2O, Е0 = 1,52В Для установления нормальности
- 38. Иодометрия I2 +ē ↔ 2I-, Определение меди E0Cu2+/Cu+ =0,16 B E0I2/I2- =0,53 B 2CuSO4 + 4KI
- 39. Иодометрия I2 +ē ↔ 2I-, Определение меди E0Cu2+/Cu+ =0,16 B E0I2/I2- =0,53 B 2CuSO4 + 4KI
- 41. Скачать презентацию












![Вычисление растворимости осадков, исходя из величины ПР Ca3(PO4)2 ↔ 3Ca2+ + 2PO43- ПРCa3(PO4)2 = [Ca2+]3 ⋅[PO43-]2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1402862/slide-13.jpg)






















 Сложные эфиры
Сложные эфиры Фазовое равновесие в насыщенном растворе малорастворимого электролита. (Глава 4. Задача 10)
Фазовое равновесие в насыщенном растворе малорастворимого электролита. (Глава 4. Задача 10) фізичні властивості полімеру спиртів та карбонових кислот
фізичні властивості полімеру спиртів та карбонових кислот  Химические индикаторы
Химические индикаторы Обмен липидов
Обмен липидов Технология производства простых полиэфиров
Технология производства простых полиэфиров Презентация по Химии "Форфор" - скачать смотреть
Презентация по Химии "Форфор" - скачать смотреть  Вода ценный дар природы. Биологическая роль воды
Вода ценный дар природы. Биологическая роль воды Геохимия урана и тория в карбонатитовом процессе
Геохимия урана и тория в карбонатитовом процессе Физическая и коллоидная химия
Физическая и коллоидная химия Физические явления в химии (8 класс)
Физические явления в химии (8 класс) Қабаттағы мұнай
Қабаттағы мұнай Як прості речовини
Як прості речовини  Цинк. Знаходження в періодичній системі і основні характеристики
Цинк. Знаходження в періодичній системі і основні характеристики Адам мен жануар организміне бордың әсері
Адам мен жануар организміне бордың әсері Высокомолекулярные вещества полимеры
Высокомолекулярные вещества полимеры Окислительно-восстановительные процессы. Лекция 8
Окислительно-восстановительные процессы. Лекция 8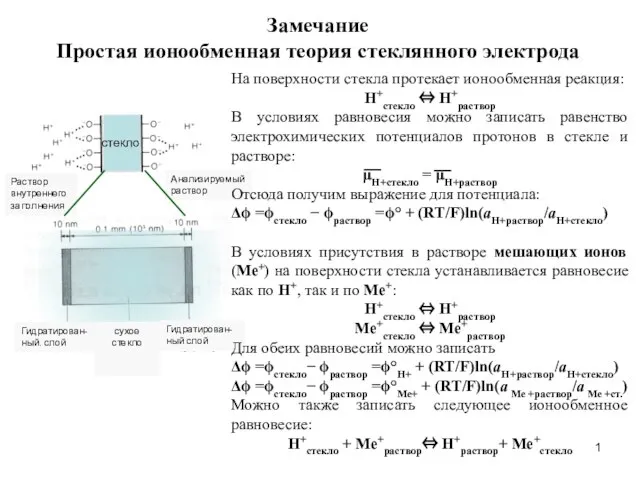 Простая ионообменная теория стеклянного электрода
Простая ионообменная теория стеклянного электрода Биологический метод исследования. Определение патогенности и вирулентности микроорганизмов
Биологический метод исследования. Определение патогенности и вирулентности микроорганизмов Работа выполнена обучающейся 9 «А» класса МОУ «СОШ №2» Мусафировой Анастасией
Работа выполнена обучающейся 9 «А» класса МОУ «СОШ №2» Мусафировой Анастасией Химия, 8. Урок 1
Химия, 8. Урок 1 Биопластики: область применения
Биопластики: область применения Производные карбоновых кислот. Ненасыщенные карбоновые кислоты
Производные карбоновых кислот. Ненасыщенные карбоновые кислоты Caustic Soda
Caustic Soda Презентация по Химии "Неметаллы" - скачать смотреть
Презентация по Химии "Неметаллы" - скачать смотреть  Презентация по Химии "Биополимеры" - скачать смотреть
Презентация по Химии "Биополимеры" - скачать смотреть  Химия в пищевой промышленности
Химия в пищевой промышленности Интересные факты о нефти
Интересные факты о нефти