Содержание
- 2. Лекция 2 Жидкость - жидкостная экстракция органических соединений и ионов металлов 1. Жидкостная экстракция органических соединений
- 3. ПРИ ОПИСАНИИ Э. И ВЫБОРЕ УСЛОВИЙ НАС БУДУТ ИНТЕРЕСОВАТЬ: 1. Движущая сила процесса 2. Тип экстрагента,
- 4. Гидратация ↔ Сольватация Типы экстракционных систем 1. Физическое распределение (∆Gгидр. 2. Реакционная экстракция (∆Gгидр. > ∆Gcольв.)
- 5. Экстракция по механизму физического распределения Органические соединения экстрагируются в нейтральной форме Ав ↔ Ао Главная причина
- 6. Природа экстрагента (органического растворителя) Состав водной фазы Природа экстрагирующегося соединения рН водной фазы (для ионизированных органических
- 7. Экстрагенты – органические растворители самой разной природы, которые экстрагируют молекулы органических соединений по механизму физического распределения
- 8. Тип связи, образуемый растворителем с экстрагируемым веществом
- 9. Сложные эфиры > спирты > простые эфиры > ароматические > хлорсодержащие > непредельные У. > предельные
- 10. Требования к растворителям Обеспечивать высокие R,% Обладать низкой растворимостью в воде Обладать высокой Ткипения (>500) Обладать
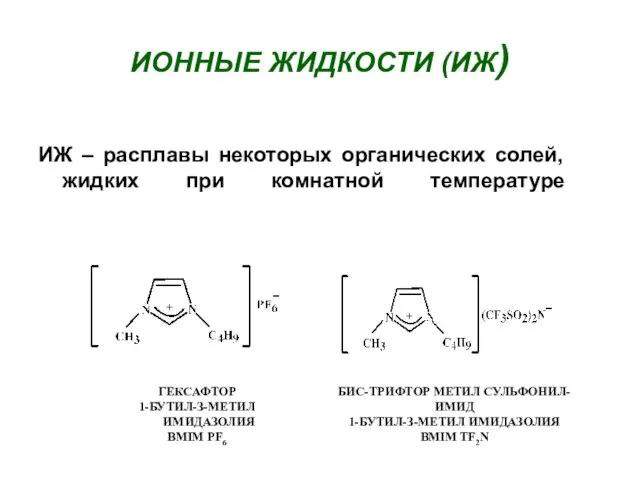
- 11. ИОННЫЕ ЖИДКОСТИ (ИЖ) ИЖ – расплавы некоторых органических солей, жидких при комнатной температуре
- 12. НЕКОТОРЫЕ СВОЙСТВА ИЖ: Негорючесть Термическая устойчивость Низкое давление паров Несмешиваемость с водой Нетоксичность, экологичность (Green chemistry)
- 13. Экстракционные свойства ИЖ 1. По экстракционным свойствам ИЖ похожи на сложные эфиры и замещенные ароматические углеводороды
- 14. 2. Состав водной фазы Высаливание - понижение Sв органического соединения в присутствии неорганических солей Чем объясняется
- 15. Всаливание - повышение Sв органического соединения в присутствии некоторых веществ) Какие вещества обладают всаливающим действием? Мочевина,
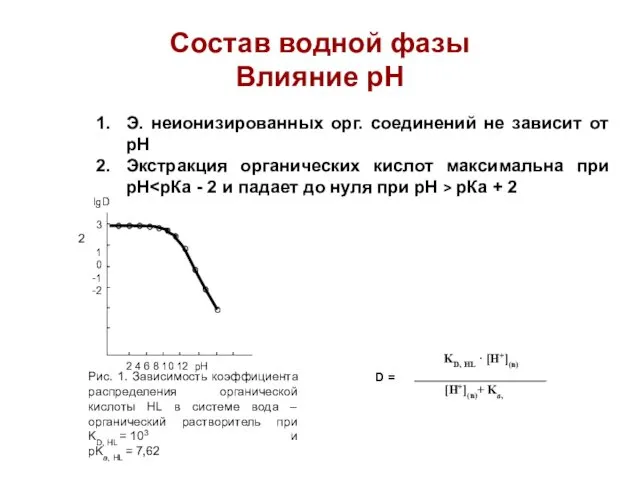
- 16. Состав водной фазы Влияние рН Э. неионизированных орг. соединений не зависит от рН Экстракция органических кислот
- 17. 3. Природа экстрагирующегося соединения Молекулярная масса соединения (число атомов С) Его полярность или гидрофобность и связанную
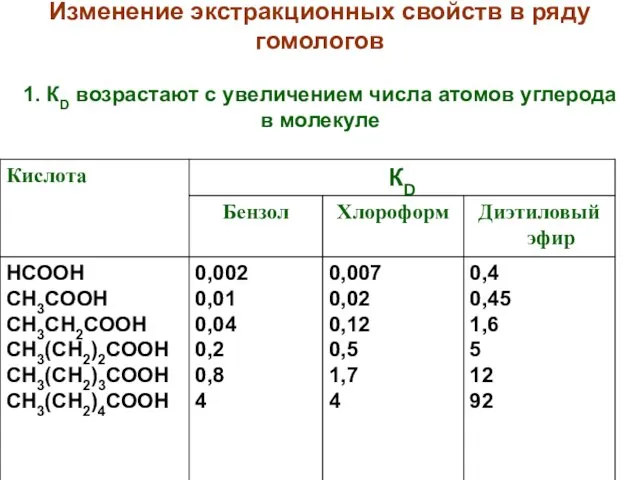
- 18. Изменение экстракционных свойств в ряду гомологов 1. КD возрастают с увеличением числа атомов углерода в молекуле
- 19. 2. КD возрастают при введении в молекулу заместителей, например, галоидов Важно! 1) КD возрастают в ряду:
- 20. Kt+о + An- о↔ Kt+An-о Kt+о + An- о↔ Kt+An-о Экстракционно-фотометрические и экстракционно-люминесцентные методы определения органических
- 21. Факторы, оказывающие влияние на экстракцию ионных ассоциатов Гидрофобность компонентов, образующих ионную пару (в качестве противоионов используют
- 22. Комплексообразование «гость-хозяин» Хозяин – макроциклические аналитические реагенты (краун-эфиры, поданды и др. циклические молекулы). Гости – определяемые
- 24. 2. Жидкостная экстракция ионов металлов
- 25. Движущая сила процесса Гидратация ↔ Сольватация Sв Типы экстракционных систем 1. Физическое распределение 2. Реакционная экстракция
- 26. Реакционная экстракция (ионы M(H2O)n m+ , M(L) n m+ , M(A) n m- ) ∆Gгидр. >
- 27. Основные процессы, протекающие при проведении реакционной Э. 1. Дегидратация ионов (затрата энергии) 2. Ассоциация ионов и
- 28. Комплексообразование и экстракция Экстракция элементов – это реакция комплексообразования, протекающая в двухфазной гетерогенной системе; Для экстракционного
- 29. Условия экстракции ионов металлов 1. Нейтрализация заряда Ионы металла связывают в незаряженный комплекс; Заряженные частицы экстрагируют
- 30. Типы и группы экстрагирующихся соединений
- 31. Основные типы экстрагентов
- 32. Хелатообразующие: β-дикетоны (ацетилацетон); купфероны; дитиокарбаматы (диэтилдитиокарбами-нат натрия, пирролидиндитиокарбаминат амммония); 8-гидроксихинолин и его производные; дитизон, диметилглиоксим; и
- 33. Выбор экстрагента в соответствии с принципом о жестких и мягких кислот и оснований (ЖМКО, принцип Пирсона)
- 34. Классификация ионов металлов (кислот) в соответствии с принципом ЖМКО
- 35. Классификация экстрагентов (оснований) в соответствии с принципом ЖМКО
- 36. Принцип Пирсона утверждает, что жесткие кислоты предпочтительно реагируют с жесткими основаниями и, наоборот – мягкие кислоты
- 37. Априорная оценка экстракционного поведения ионов металлов Вопросы??? 1. В какой последовательности будут изменяться константы устойчивости комплексов
- 38. Особенности экстракции элементов по типам и группам экстрагирующихся соединений
- 39. Координационно несольватированные соединения с ковалентной связью I2, Br2 HgCl2, AsCl3, SbCl3, GeCl4 HgBr2, AsBr3, SbBr3, GeBr4,
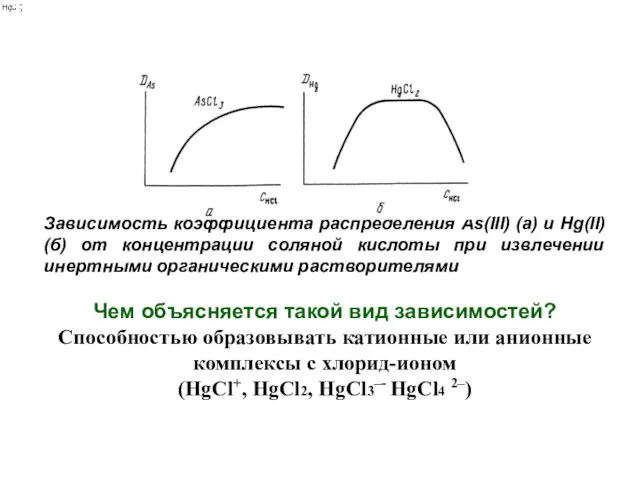
- 40. Факторы, влияющие на экстракцию Kэх = βMXn ×KD,MXn Экстракция возрастает: С увеличением констант устойчивости (βMXn) HgCl2
- 41. Зависимость коэффициента распределения As(III) (a) и Hg(II) (б) от концентрации соляной кислоты при извлечении инертными органическими
- 42. Нейтральные координационно сольватированные соединения MXnLm M – ион металла, X – неорганический анион (Cl−, Br−, I
- 43. Выбор экстрагента, исходя из принципа ЖМКО 1. Для жестких РЗЭ, актинидов, циркония, железа используют жесткие кислородсодержащие
- 44. Хелаты (внутрикомплексные соединения) MLm Хелат – комплексное соединение, образованное при взаимодействии ионов металлов с органическими полидентатными
- 45. От чего зависит коэффициент распределения хелата (D)? М(в) + mHL(о) = МLm(о) + mH(в) lgD =
- 46. Примеры функционально-аналитических группировок и образуемых хелатных циклов с ионами металлов
- 47. Виды хелатов Координационно-насыщенные хелаты Причины образования: координационное число равно удвоенному заряду иона металла. Пример: ацетилацетонат алюминия.
- 48. Виды хелатов 2. Координационно-ненасыщенные хелаты Причины образования: координационное число больше удвоенного заряда иона металла. Пример: 8-гидроксихинолат
- 49. Виды хелатов 3. Катионные хелаты Причины образования: 1. К.ч. меньше удвоенного заряда иона металла; Пример: Au(III),
- 50. Виды хелатов 4. Анионные хелаты Причины образования: 1. Использование экстрагентов, содержащих, помимо хелатообразующей группировки, легко диссоциирующуюся
- 51. Координационно-несольватированные ионные ассоциаты [Kt+][A─] [Kt+], [A─] - крупные и гидрофобные катионы и анионы, которые не сольватированы
- 52. Факторы, влияющие на экстракцию ИА Экстракция возрастает: 1. С увеличением ε растворителей 2. С увеличением размера
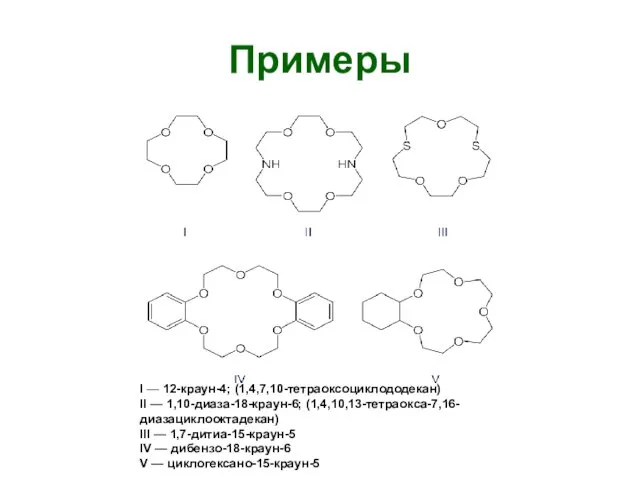
- 53. Экстракция ионов металлов краун-эфирами и макроциклическими соединениями Краун-эфиры – это макроциклические полиэфиры, содержащие от 4 до
- 54. Примеры I — 12-краун-4; (1,4,7,10-тетраоксоциклододекан) II — 1,10-диаза-18-краун-6; (1,4,10,13-тетраокса-7,16-диазациклооктадекан) III — 1,7-дитиа-15-краун-5 IV — дибензо-18-краун-6 V
- 55. Особенность комплексообразования: краун-эфиры образуют комплексы с солями щелочных и щелочноземельных металлов. При комплексообразовании катион включается во
- 56. Комплексные металлгалогенидные кислоты HnMXm+n M – ион металла, X – неорганический анион (F−, Cl−, Br−, I−,SCN
- 58. Факторы, влияющие на экстракцию D = Kex ×[H+]n(в) × [ X−](n +m)(в) × [S]y(о) Катион 1.Влияние
- 59. Факторы, влияющие на экстракцию Анион 1 Концентрация Х − 2. Размер иона. С ростом размера в
- 60. Литература 1. Концентрирование следов органических соединений /Под ред. Н.М. Кузьмина. М.: Наука, 1990. 280 с. .
- 61. Спасибо за внимание
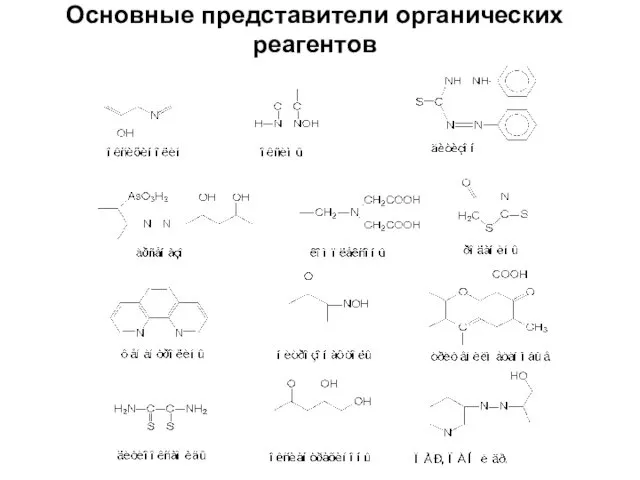
- 62. Основные представители органических реагентов
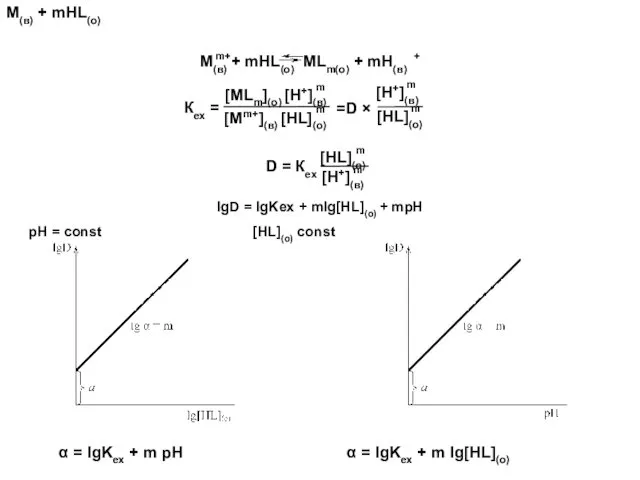
- 63. Количественное описание экстракции хелатов Определение состава комплекса
- 64. М(в) + mHL(о) α = lgKex + m pH α = lgKex + m lg[HL](о) lgD
- 66. Скачать презентацию













































![Координационно-несольватированные ионные ассоциаты [Kt+][A─] [Kt+], [A─] - крупные и гидрофобные катионы](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/460041/slide-50.jpg)





![Факторы, влияющие на экстракцию D = Kex ×[H+]n(в) × [ X−](n](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/460041/slide-57.jpg)




 Химия: основные понятия
Химия: основные понятия Функции металлов в истинном металлоферменте. (Лекция 16)
Функции металлов в истинном металлоферменте. (Лекция 16) Методы диагностики плазмы
Методы диагностики плазмы Презентация по Химии "Дмитро Менделєєв" - скачать смотреть бесплатно
Презентация по Химии "Дмитро Менделєєв" - скачать смотреть бесплатно Дифференциация магмы
Дифференциация магмы Основные классы неорганических соединений
Основные классы неорганических соединений Предельные углеводороды
Предельные углеводороды Ацетилен. Физические и химические свойства
Ацетилен. Физические и химические свойства Кинетика химических реакций
Кинетика химических реакций Chemical reactions. (Chapter 5)
Chemical reactions. (Chapter 5) Условная оптимизация методом классического математического анализа с применением множителей
Условная оптимизация методом классического математического анализа с применением множителей Фармацевтичний аналіз
Фармацевтичний аналіз Фосфор
Фосфор Углеводороды. Применение природных источников углеводородов и продуктов их переработки
Углеводороды. Применение природных источников углеводородов и продуктов их переработки ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров
ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров Алкалоидтар
Алкалоидтар Metals
Metals Гидролиз органических веществ
Гидролиз органических веществ Мел - полезное ископаемое моего села
Мел - полезное ископаемое моего села Презентация по Химии "Металлы. Общая характеристика металлов (нахождение в природе и физические свойства)" - скачать смотреть
Презентация по Химии "Металлы. Общая характеристика металлов (нахождение в природе и физические свойства)" - скачать смотреть  Э.М. Спиридонов. Эволюция минералов ртути в зоне гипергенеза
Э.М. Спиридонов. Эволюция минералов ртути в зоне гипергенеза Использование активных методов обучения на уроках химии
Использование активных методов обучения на уроках химии Моделирование структуры биомакромолекул
Моделирование структуры биомакромолекул Vitaminele
Vitaminele Основні методи синтезу та стабілізації наносистем
Основні методи синтезу та стабілізації наносистем Фенолы. Физические свойства
Фенолы. Физические свойства Химическая связь
Химическая связь Липиды омыляемые и неомыляемые
Липиды омыляемые и неомыляемые