Микроколичественное определение 2,3-бутандиола для анализа антирадикальной активности фенольных соединений
Содержание
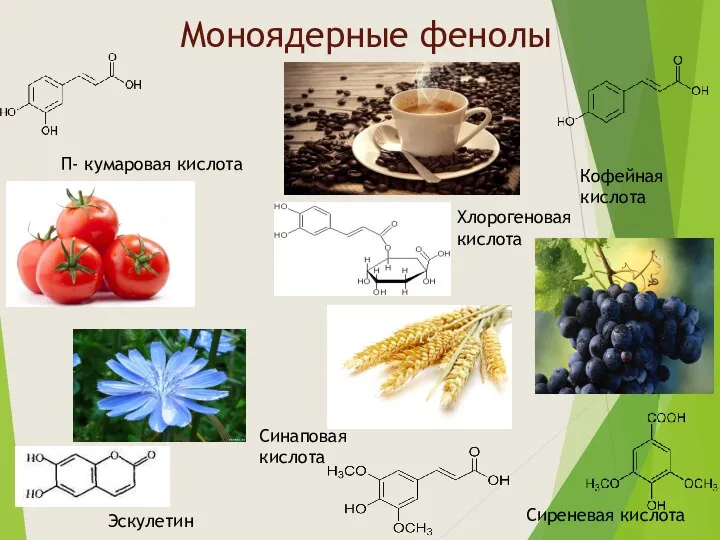
- 2. Моноядерные фенолы П- кумаровая кислота Кофейная кислота Хлорогеновая кислота Эскулетин Сиреневая кислота Синаповая кислота
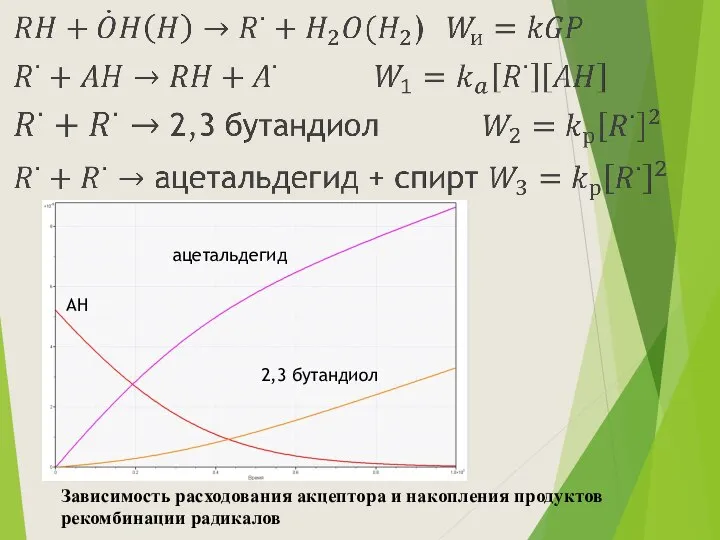
- 3. Основными молекулярными продуктами рекомбинации α-гидроксиэтильного радикала являются ацетальдегид и 2,3-бутандиол: димеризация диспропорционирование
- 4. Зависимость расходования акцептора и накопления продуктов рекомбинации радикалов АН ацетальдегид 2,3 бутандиол
- 5. Задачи: Изучить литературные данные по теме исследования. Подобрать оптимальные газохроматографические условия для инструментального анализа 2,3- бутандиола.
- 6. Методы исследования Эмпирические Теоретические C= (G·D·М·ρсм)/(100·Na·1,6·10-19) , где C – концентрация [г/л], Na–число Авогадро, D–доза облучения
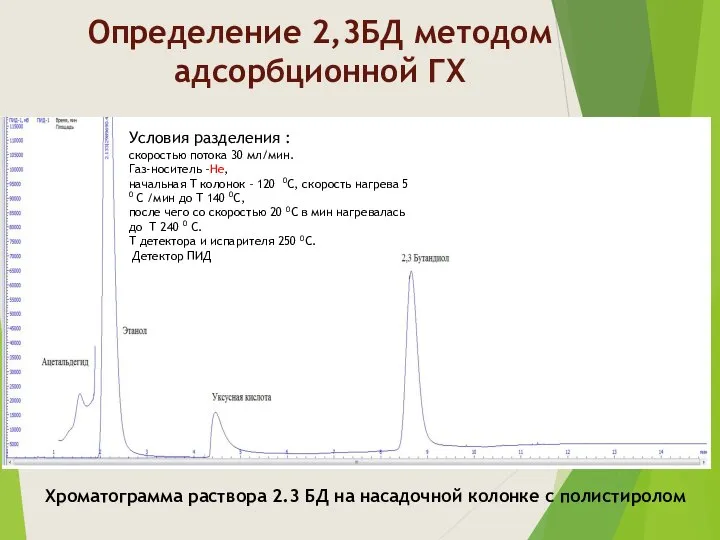
- 7. Определение 2,3БД методом адсорбционной ГХ Хроматограмма раствора 2.3 БД на насадочной колонке с полистиролом Условия разделения
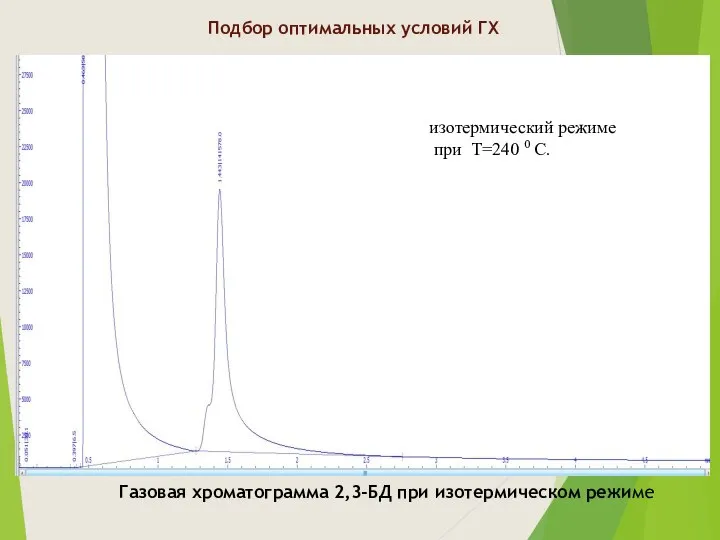
- 8. Газовая хроматограмма 2,3-БД при изотермическом режиме Подбор оптимальных условий ГХ изотермический режиме при Т=240 0 С.
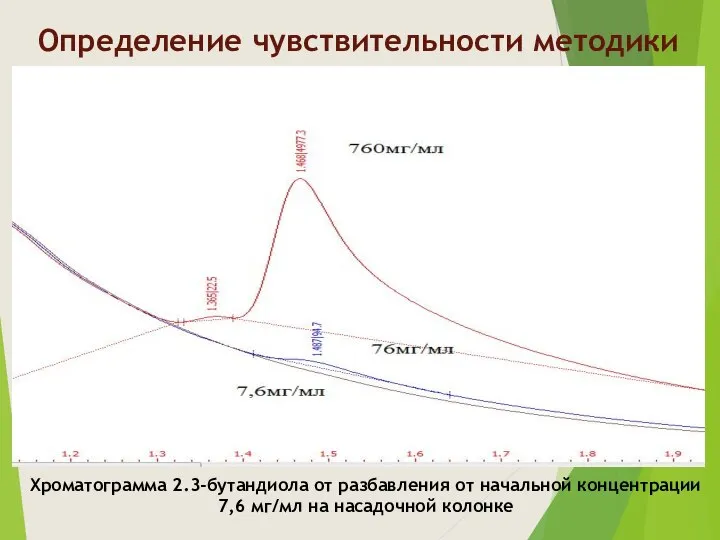
- 9. Определение чувствительности методики Хроматограмма 2.3-бутандиола от разбавления от начальной концентрации 7,6 мг/мл на насадочной колонке
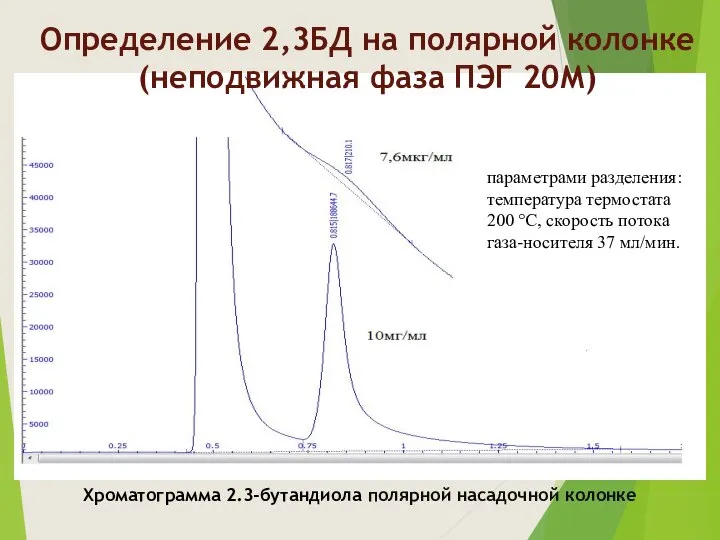
- 10. Хроматограмма 2.3-бутандиола полярной насадочной колонке параметрами разделения: температура термостата 200 °C, скорость потока газа-носителя 37 мл/мин.
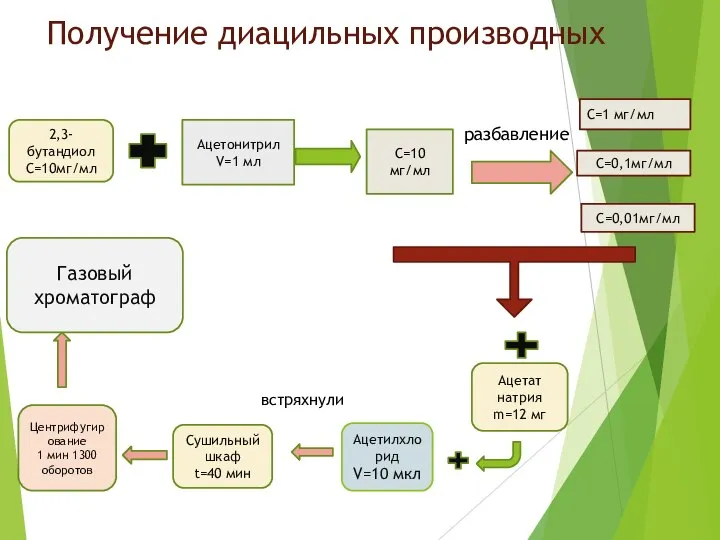
- 11. Получение диацильных производных 2,3-бутандиол С=10мг/мл Ацетонитрил V=1 мл разбавление С=10 мг/мл С=1 мг/мл С=0,1мг/мл С=0,01мг/мл Ацетат
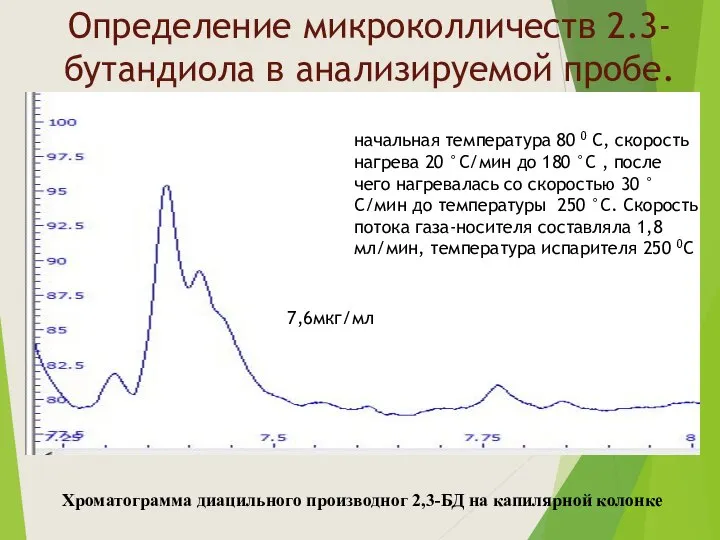
- 12. Определение микроколличеств 2.3-бутандиола в анализируемой пробе. Хроматограмма диацильного производног 2,3-БД на капилярной колонке начальная температура 80
- 13. Масс-спектр триметилсиллильного производного 2,3-БД
- 14. Хроматограмма триметилсилильного производного Соотношение сигнала к шуму 10мкг/мл
- 15. Выводы: Изучили литературные данные по теме исследования. Выявили методики определения диолов в смесях. Провели модификацию методики
- 16. Спасибо за внимание!
- 18. Скачать презентацию







 Химические свойства строительных материалов. Урок №5
Химические свойства строительных материалов. Урок №5 Коррозия металлов
Коррозия металлов Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск
Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск Кристаллы. Выращивание кристаллов в домашних условиях
Кристаллы. Выращивание кристаллов в домашних условиях Карбоновые кислоты Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна
Карбоновые кислоты Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна  Презентация по Химии "Азотсодержащие органические соединения" - скачать смотреть
Презентация по Химии "Азотсодержащие органические соединения" - скачать смотреть  Непредельные углеводороды (обобщающий урок)
Непредельные углеводороды (обобщающий урок) История нефтедобычи в России Материал для урока химии в 10 классе УМК О.С. Габриеляна Составила Яковлева Л.А.
История нефтедобычи в России Материал для урока химии в 10 классе УМК О.С. Габриеляна Составила Яковлева Л.А.  Соединения азота. Оксиды азота
Соединения азота. Оксиды азота Презентация по Химии "«Соединения бериллия»" - скачать смотреть _
Презентация по Химии "«Соединения бериллия»" - скачать смотреть _ Каталитические процессы нефтепереработки
Каталитические процессы нефтепереработки Д.І.Менделєєв Визначні дати в його житті.
Д.І.Менделєєв Визначні дати в його житті.  Решение задачи №10. Гидроксид рубидия. Команда «Карбораны»
Решение задачи №10. Гидроксид рубидия. Команда «Карбораны» Кислородосодержащие органические соединения
Кислородосодержащие органические соединения Chem-квест. Химический диктант
Chem-квест. Химический диктант Введение. Виды стекол. Применение конструкций из стекла
Введение. Виды стекол. Применение конструкций из стекла Электропроводность растворов электролитов. Числа переноса
Электропроводность растворов электролитов. Числа переноса Полимеры. Классификация полимеров
Полимеры. Классификация полимеров Ультрадисперсные, наноструктурные и ультрамелкозернистые материалы
Ультрадисперсные, наноструктурные и ультрамелкозернистые материалы Минералдар және олардың агрегаттарының морфологиясы. Минералдарды жүйелеуінің негізі
Минералдар және олардың агрегаттарының морфологиясы. Минералдарды жүйелеуінің негізі Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Алюміній оксид Al2O3
Алюміній оксид Al2O3  «Многоатомные спирты»
«Многоатомные спирты»  Презентация по Химии "«Химические волокна»" - скачать смотреть
Презентация по Химии "«Химические волокна»" - скачать смотреть  Геометрия молекул
Геометрия молекул Методы определения основных групп токсических веществ. Этапы химико-токсикологического анализа
Методы определения основных групп токсических веществ. Этапы химико-токсикологического анализа Презентація уроку «Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття» Підготувала: учит
Презентація уроку «Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття» Підготувала: учит Новые требования, предъявляемые к лабораторно-минералогическим исследованиям
Новые требования, предъявляемые к лабораторно-минералогическим исследованиям