Содержание
- 2. 1. Електронна будова бензолу. Ароматичні властивості. Загальні критерії ароматичності. 2. Номенклатура та ізомерія моноядерних аренів. 3.
- 5. Вуглеводні: ароматичні Назва класу вуглеводню Загальна формула Тип гібридизації атома Карбону Основний тип реакції Особливості будови,
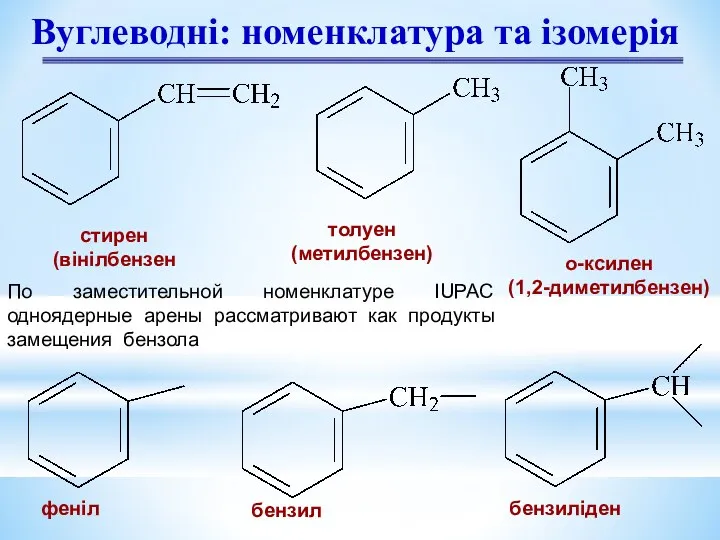
- 6. Вуглеводні: номенклатура та ізомерія стирен (вінілбензен толуен (метилбензен) о-ксилен (1,2-диметилбензен) феніл бензил бензиліден По заместительной номенклатуре
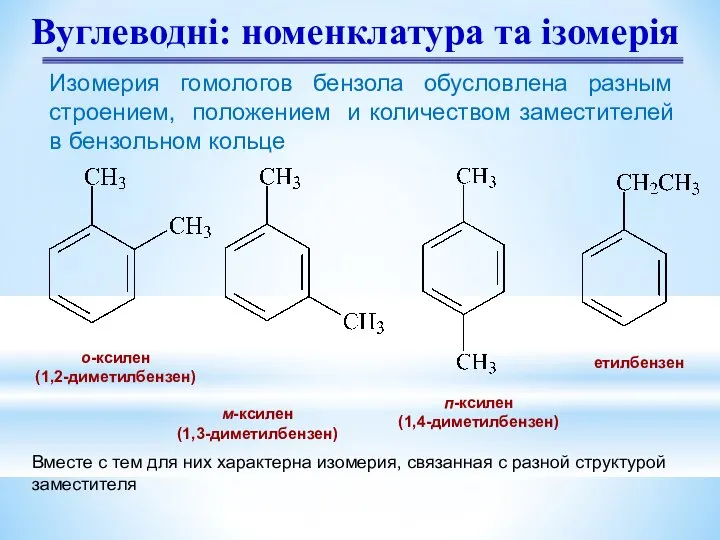
- 7. Вуглеводні: номенклатура та ізомерія о-ксилен (1,2-диметилбензен) м-ксилен (1,3-диметилбензен) п-ксилен (1,4-диметилбензен) етилбензен Изомерия гомологов бензола обусловлена разным
- 8. Вуглеводні: будова молекул Арени 6 електронів в делокалізованому π зв′язку
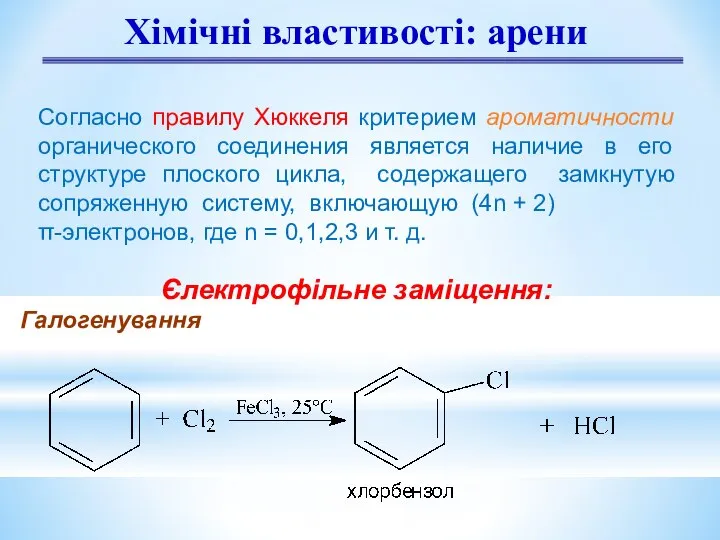
- 9. Хімічні властивості: арени Єлектрофільне заміщення: Галогенування Согласно правилу Хюккеля критерием ароматичности органического соединения является наличие в
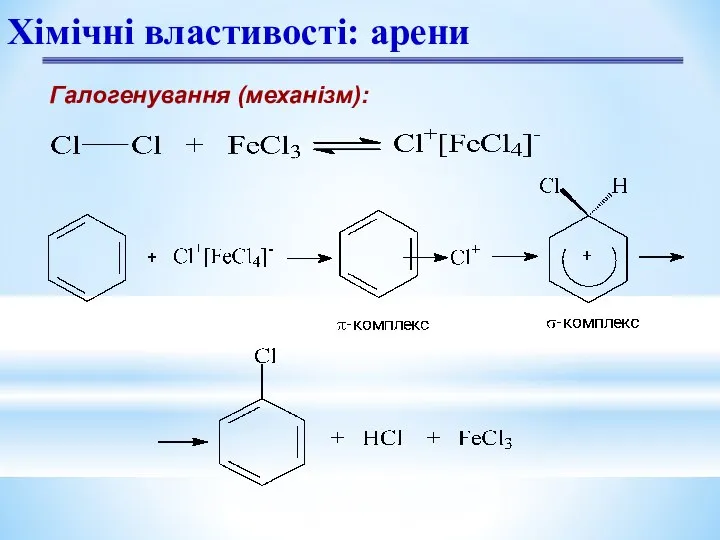
- 10. Галогенування (механізм): Хімічні властивості: арени
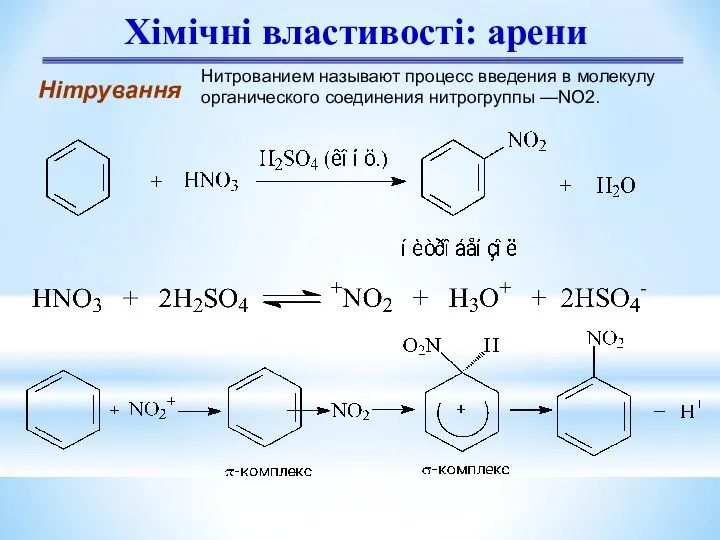
- 11. Хімічні властивості: арени Нітрування Нитрованием называют процесс введения в молекулу органического соединения нитрогруппы —NO2.
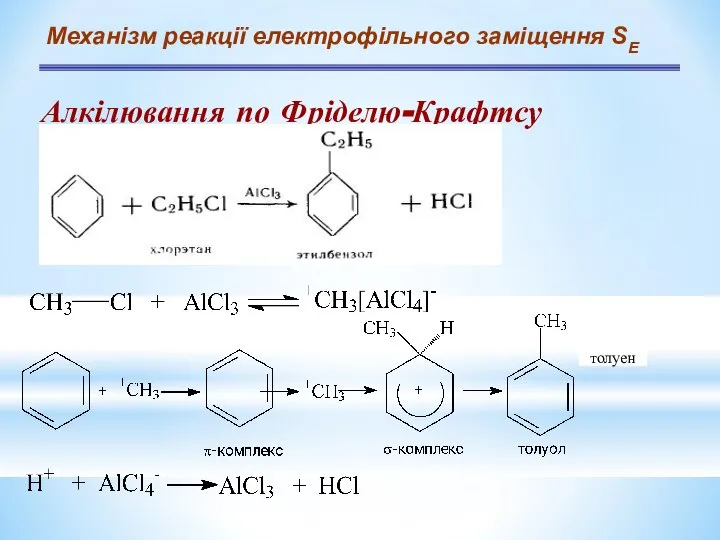
- 12. Механізм реакції електрофільного заміщення SЕ Алкілювання по Фріделю-Крафтсу толуен
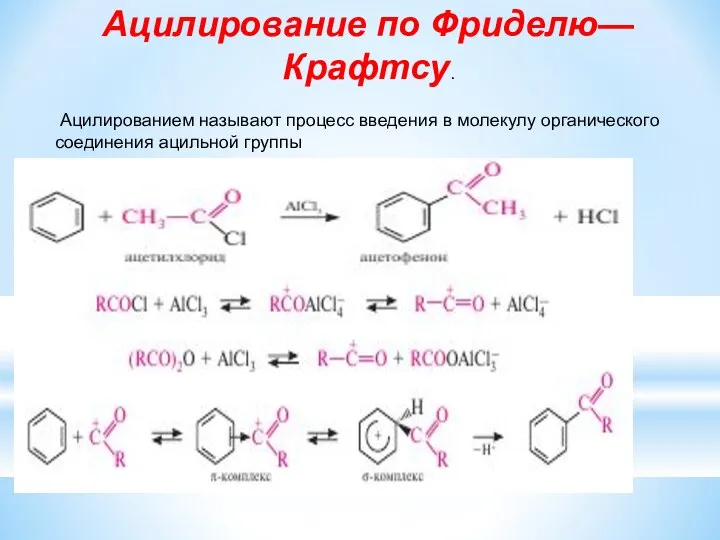
- 13. Ацилирование по Фриделю—Крафтсу. Ацилированием называют процесс введения в молекулу органического соединения ацильной группы
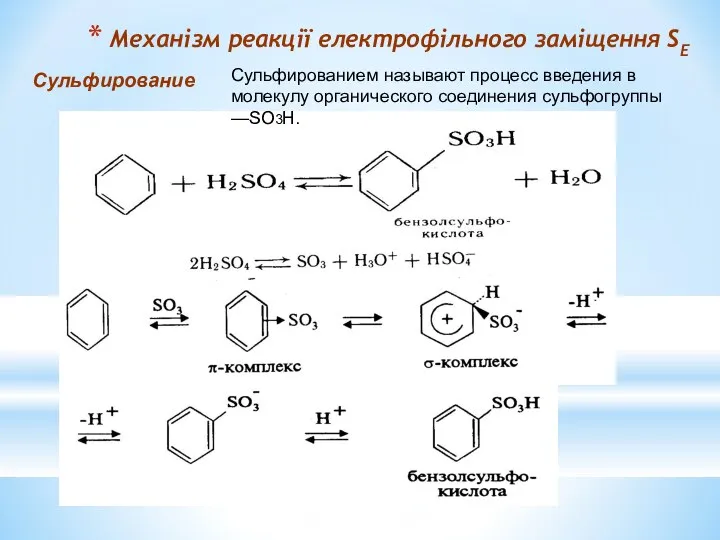
- 14. Механізм реакції електрофільного заміщення SЕ Сульфирование Сульфированием называют процесс введения в молекулу органического соединения сульфогруппы —SO3H.
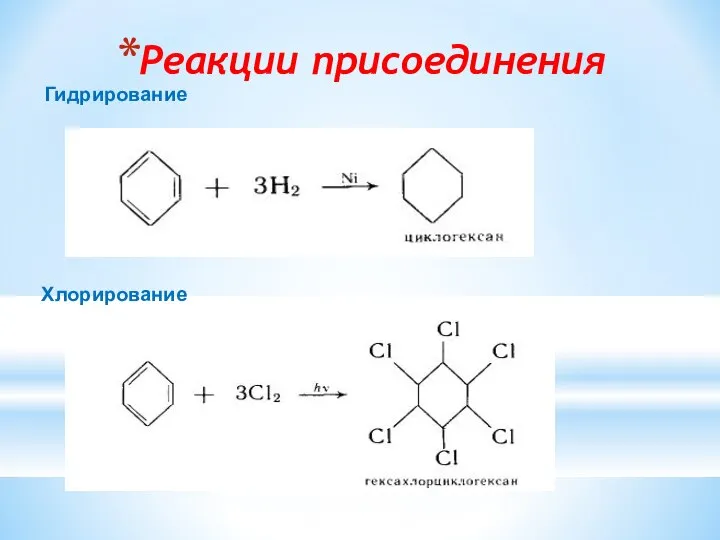
- 15. Реакции присоединения Гидрирование Хлорирование
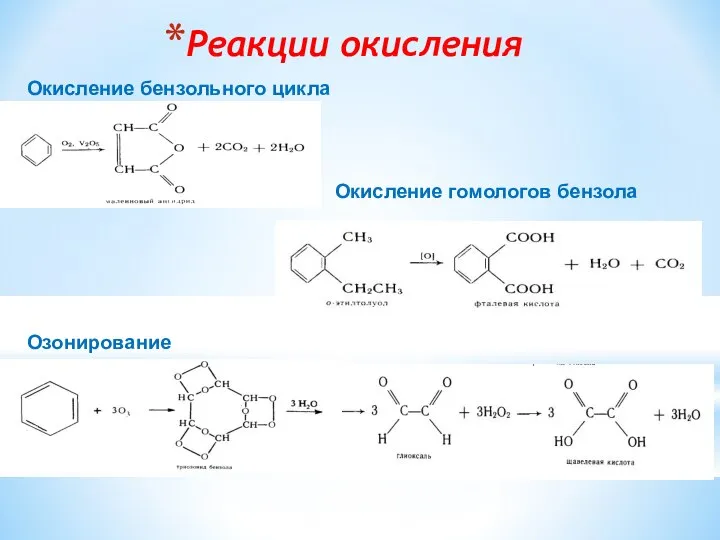
- 16. Реакции окисления Окисление бензольного цикла Окисление гомологов бензола Озонирование
- 17. Правила орієнтації – замісники І роду Замісники (орієнтанти) І роду – орто- і пара-положення: Активуючі, електронодонорні
- 18. Правила орієнтації – замісники ІІ роду Замісники (орієнтанти) ІІ роду – замісники мета-положення: —CN, —СООН, —SO3H,
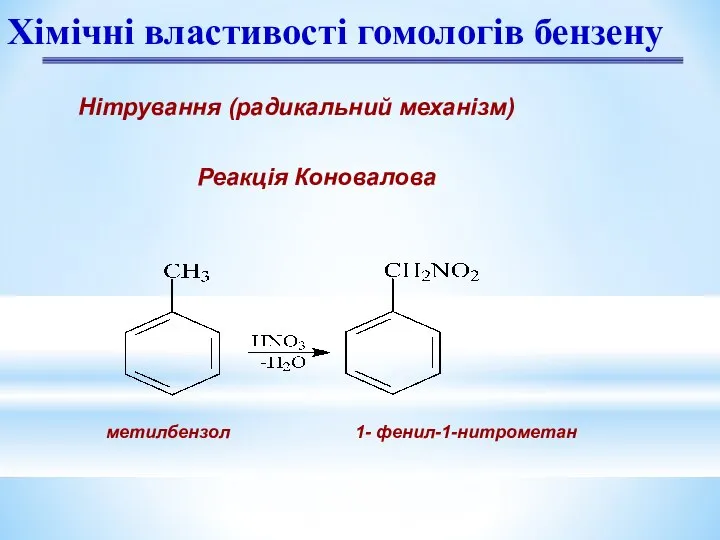
- 19. Нітрування (радикальний механізм) Реакція Коновалова Хімічні властивості гомологів бензену метилбензол 1- фенил-1-нитрометан
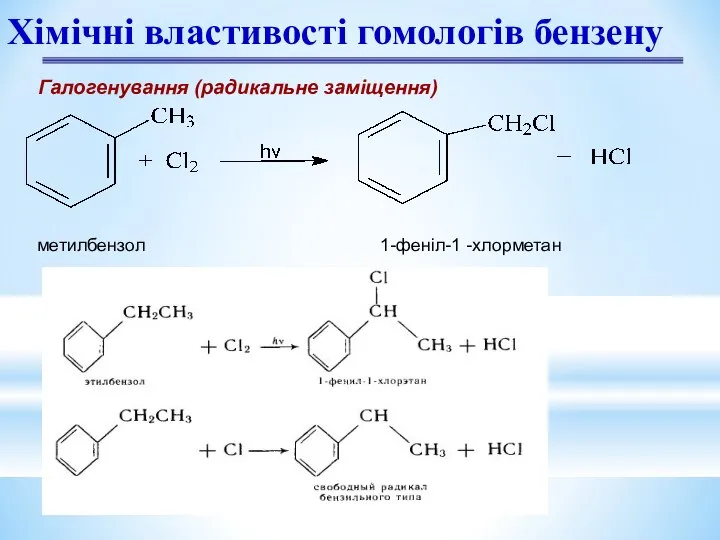
- 20. Хімічні властивості гомологів бензену Галогенування (радикальне заміщення) метилбензол 1-феніл-1 -хлорметан
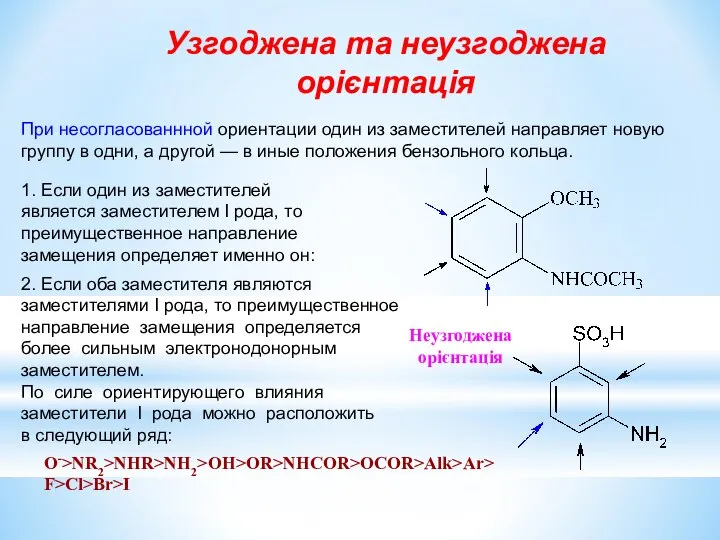
- 21. При согласованной ориентации оба имеющихся заместителя направляют новую группу в одни и те же положения бензольного
- 22. При несогласованнной ориентации один из заместителей направляет новую группу в одни, а другой — в иные
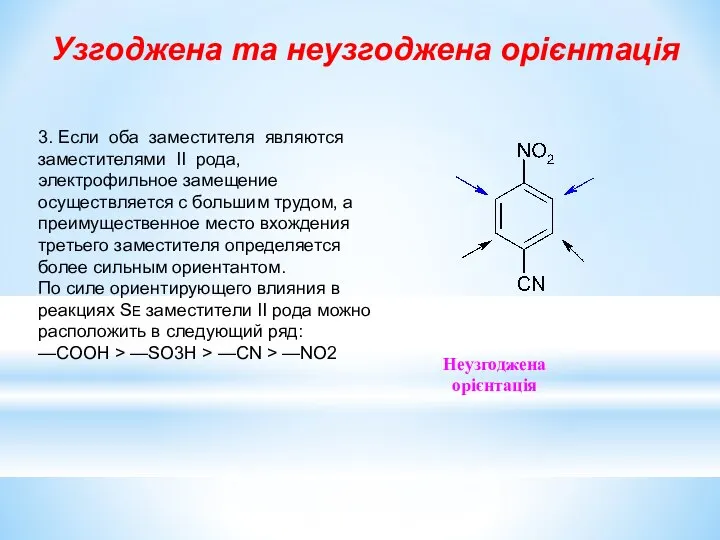
- 23. 3. Если оба заместителя являются заместителями II рода, электрофильное замещение осуществляется с большим трудом, а преимущественное
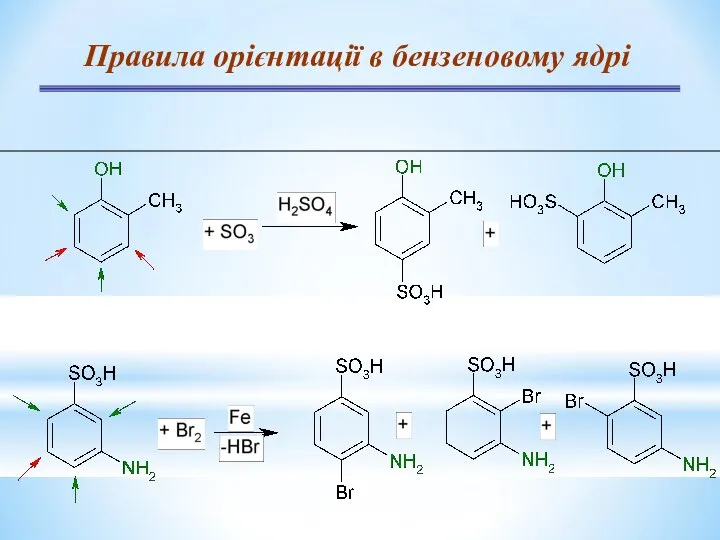
- 24. Правила орієнтації в бензеновому ядрі
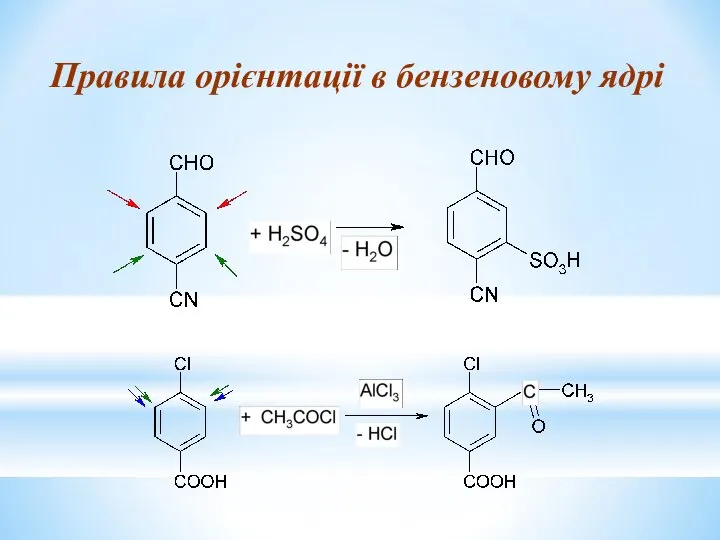
- 25. Правила орієнтації в бензеновому ядрі
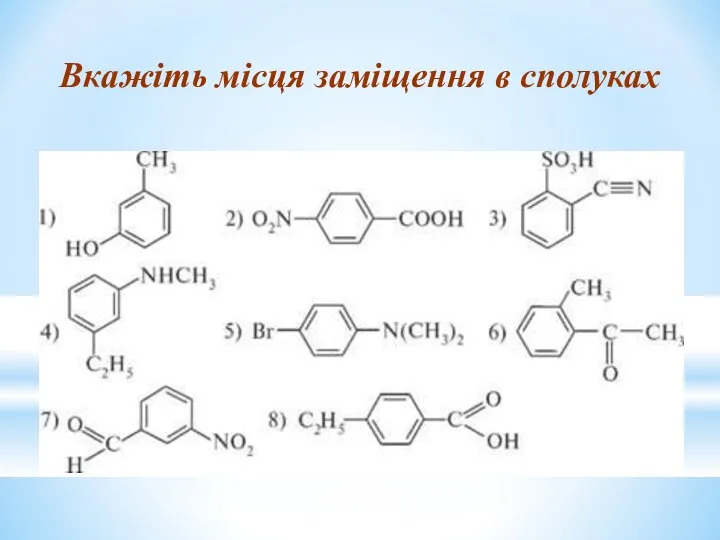
- 26. Вкажіть місця заміщення в сполуках
- 28. Дякую за увагу!
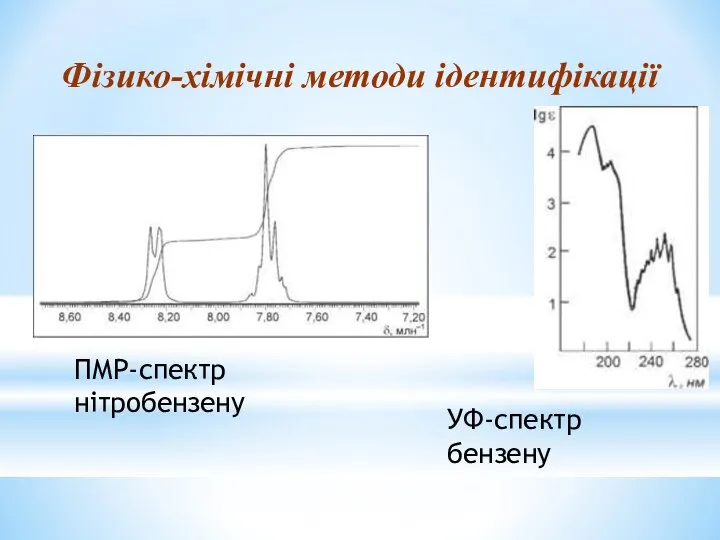
- 29. Фізико-хімічні методи ідентифікації ПМР-спектр нітробензену УФ-спектр бензену
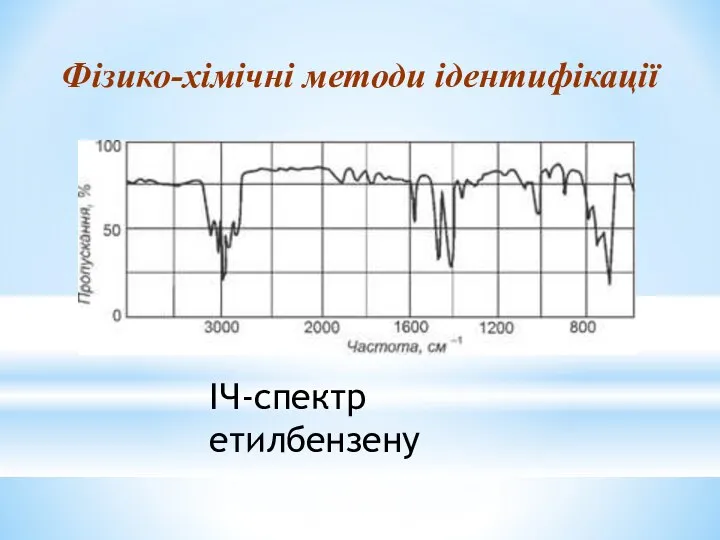
- 30. ІЧ-спектр етилбензену Фізико-хімічні методи ідентифікації
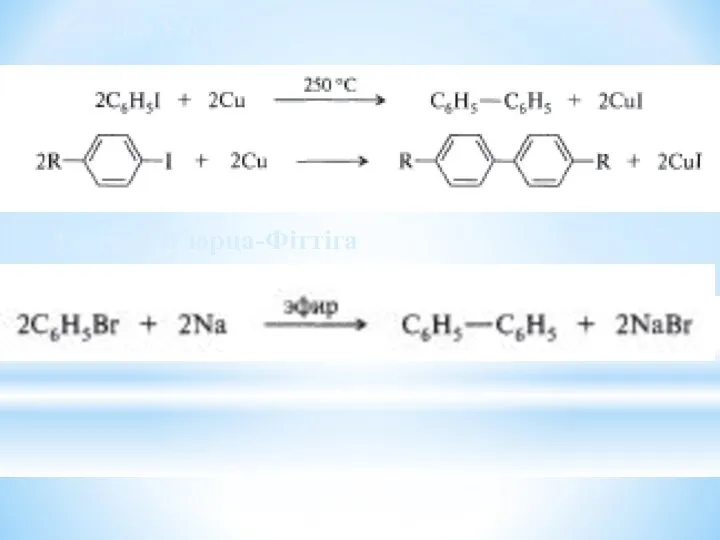
- 31. Реакція Ульмана Реакція В´юрца-Фіттіга
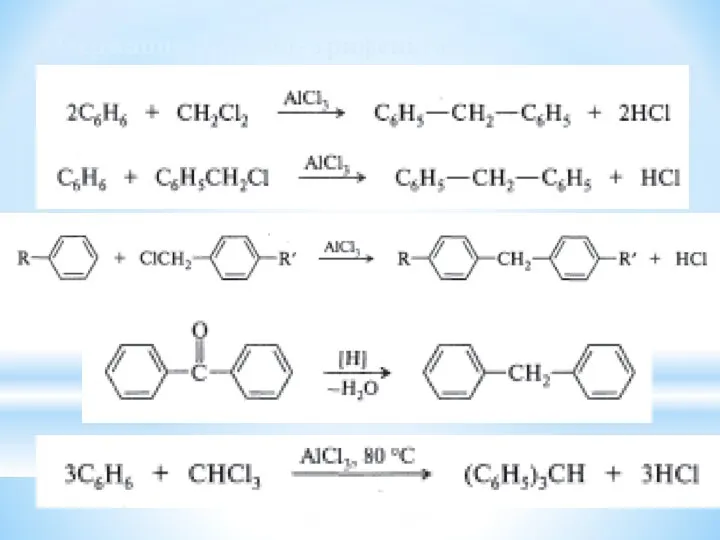
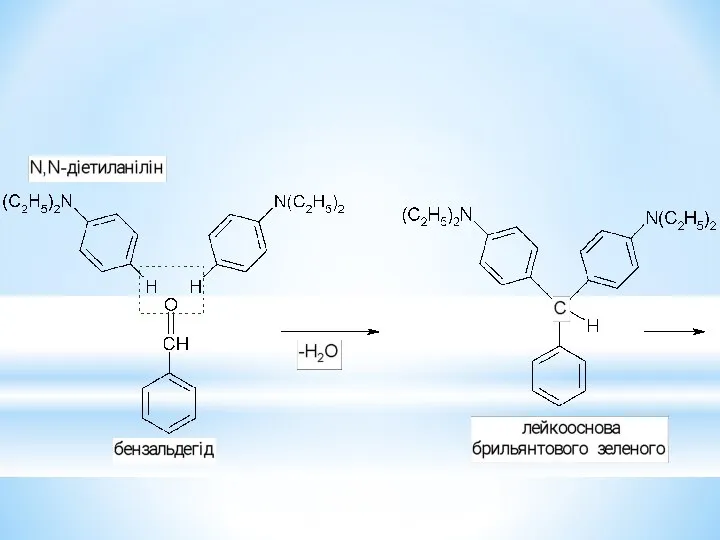
- 32. Одержання дифеніл- трифенілметану
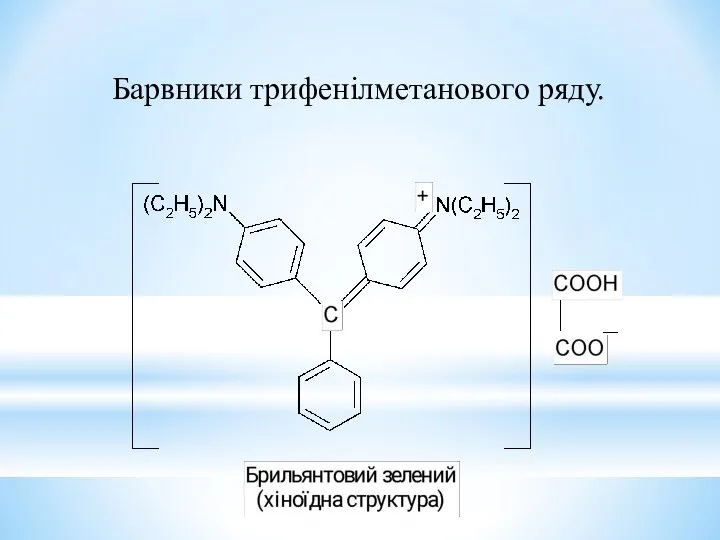
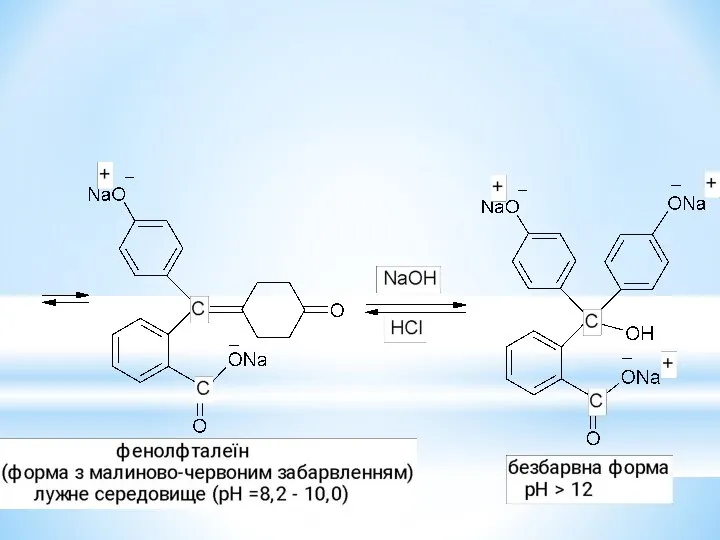
- 33. Барвники трифенілметанового ряду.
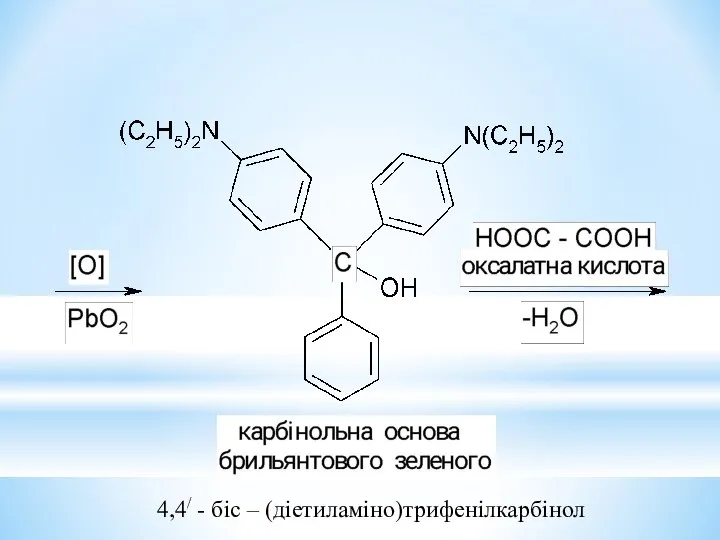
- 35. 4,4/ - біс – (діетиламіно)трифенілкарбінол
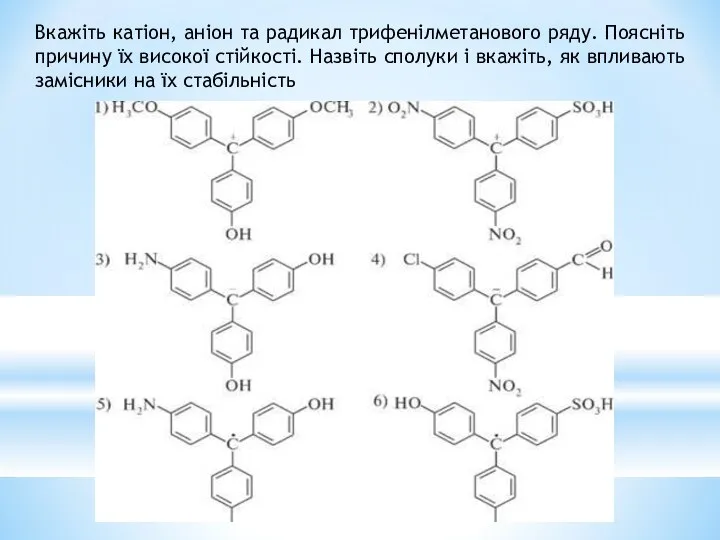
- 40. Вкажіть катіон, аніон та радикал трифенілметанового ряду. Поясніть причину їх високої стійкості. Назвіть сполуки і вкажіть,
- 42. Скачать презентацию










 Молекулы и атомы
Молекулы и атомы КИСЛОТЫ Путешествие в мир кислот Учитель: Переходцева Л.А. Учащиеся 8 а класса: Абросимов Евгений, Шемелина Яна, Шевченко Евгения
КИСЛОТЫ Путешествие в мир кислот Учитель: Переходцева Л.А. Учащиеся 8 а класса: Абросимов Евгений, Шемелина Яна, Шевченко Евгения Любовь как цепь биохимических реакций
Любовь как цепь биохимических реакций Метаморфизм. Факторы метаморфизма
Метаморфизм. Факторы метаморфизма Методы исследования структуры кристаллов
Методы исследования структуры кристаллов Растворы жидкие, твердые, газообразные
Растворы жидкие, твердые, газообразные Презентация по Химии "Решение задач по химическим уравнениям" - скачать смотреть
Презентация по Химии "Решение задач по химическим уравнениям" - скачать смотреть  Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Урок розв’язування задач
Урок розв’язування задач Арены. Бензол С6Н6
Арены. Бензол С6Н6 Ауыр металдар
Ауыр металдар Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Гетерофункциональные соединения, участвующие в процессах жизнедеятельности Биологические мембраны. Структурная организация
Биологические мембраны. Структурная организация Металлический водород
Металлический водород Основы органической химии
Основы органической химии Алюминий (лат. Aluminium)
Алюминий (лат. Aluminium) Углеводородные и неуглеводородные соединения нефти. Физические свойства нефти. Химические классификации нефти
Углеводородные и неуглеводородные соединения нефти. Физические свойства нефти. Химические классификации нефти Презентация по химии Электрофильное замещение в ароматических соединениях.
Презентация по химии Электрофильное замещение в ароматических соединениях.  Алюминий и его соединения
Алюминий и его соединения Научные фокусы. Лавовая лампа
Научные фокусы. Лавовая лампа Альдегиды и кетоны
Альдегиды и кетоны Алканы. Свойства. Строение и применение
Алканы. Свойства. Строение и применение Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены
Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены Увлекательная химия
Увлекательная химия ПИЩЕВЫЕ ДОБАВКИ-Е Выполнила ученица 10 класса Цатурова Аида Арташевна
ПИЩЕВЫЕ ДОБАВКИ-Е Выполнила ученица 10 класса Цатурова Аида Арташевна Производство аммиачной селитры под атмосферным давлением
Производство аммиачной селитры под атмосферным давлением Воспламенение (зажигание) газовых смесей
Воспламенение (зажигание) газовых смесей Растворы
Растворы