Содержание
- 2. Домашнее здание §4, тема «Алкены». Выучить конспект Письменно написать все возможные изомеры пентена.
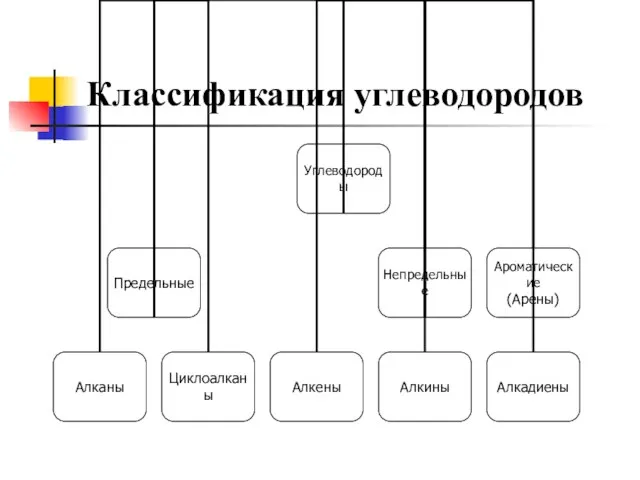
- 3. Классификация углеводородов
- 4. Алкены – ациклические углеводороды, в молекуле которых кроме одинарных связей содержится одна двойная связь между атомами
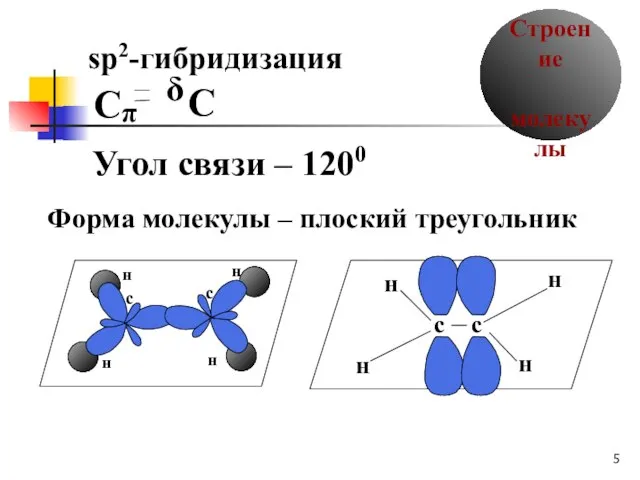
- 5. δ Строение молекулы sp2-гибридизация Угол связи – 1200 Форма молекулы – плоский треугольник C π C
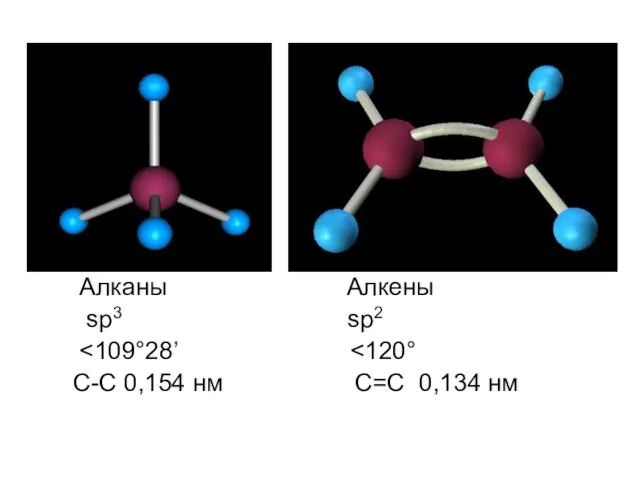
- 6. Алканы Алкены sp3 sp2 C-C 0,154 нм C=C 0,134 нм
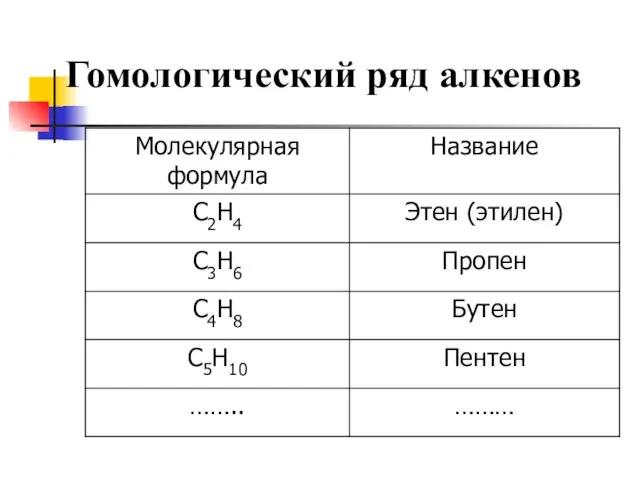
- 7. Гомологический ряд алкенов
- 8. Правила номенклатуры алкенов Выделяют в структурной формуле наиболее длинную цепь атомов углерода, включающую двойную связь, и
- 9. Виды изомерии алкенов 1. Изомерия углеродного скелета СН2=СН-СН2-СН3 и СН2=С-СН3 СН3 2. Изомерия положения кратной связи
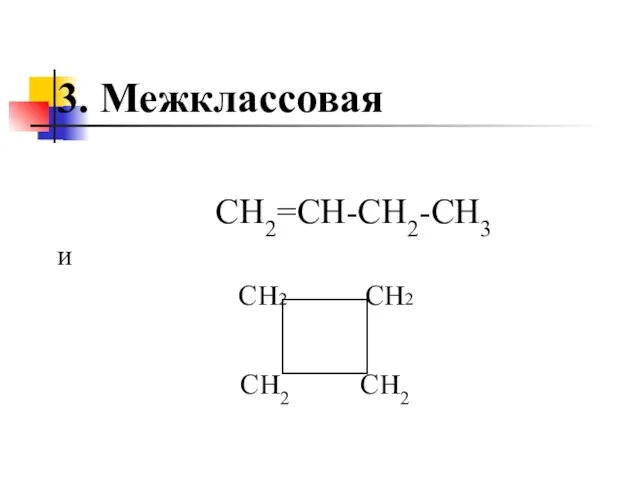
- 10. 3. Межклассовая СН2=СН-СН2-СН3 и СН2 СН2 СН2 СН2
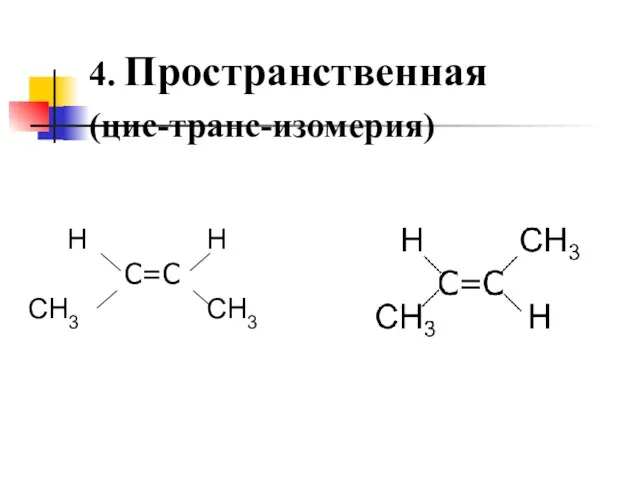
- 11. 4. Пространственная (цис-транс-изомерия)
- 12. Вещества с общей формулой СnH2n относятся к классу алканов алкинов алкенов аренов
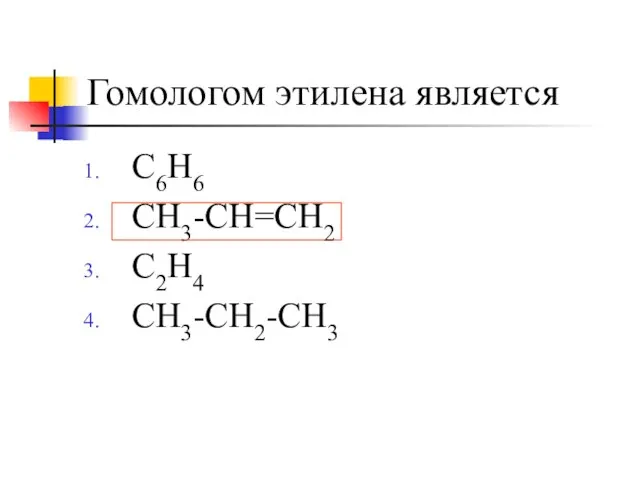
- 13. Гомологом этилена является C6H6 CH3-CH=CH2 C2H4 CH3-CH2-CH3
- 14. π-связь имеется в молекуле пентана циклопентана 2-метилпропана пропена
- 15. Углеводород с формулой СН3-СН-СН=СН-СН3 называется 2-метилпентан 2-метилпентен-3 4-метилгексен-2 4-метилпентен-2 СН3
- 16. Изомерами являются СН3-СН2-СН2СН3 и СН3-СН=СН-СН3 СН2=С-СН2-СН3 и СН3-СН=С-СН3 СН3-СН2-СН3 и СН3-СН2-СН2-СН3 СН2=СН-СН3 и СН3-СН2-СН3 СН3 СН3
- 17. Получение алкенов
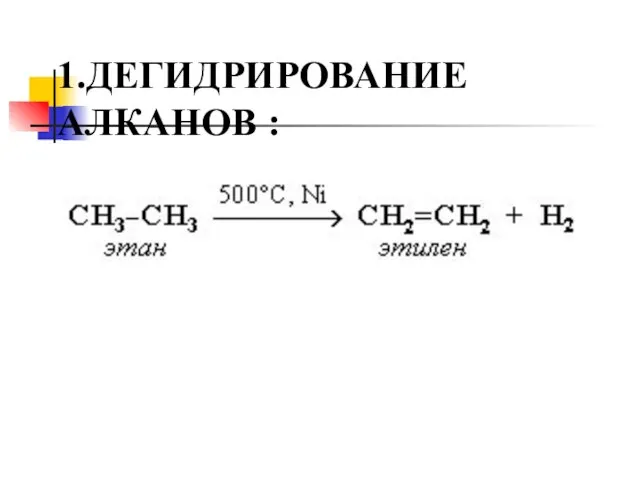
- 18. 1.ДЕГИДРИРОВАНИЕ АЛКАНОВ :
- 19. 2.КРЕКИНГ АЛКАНОВ (ПОД ВЫСОКОЙ ТЕМПЕРАТУРОЙ):
- 20. 2.КРЕКИНГ АЛКАНОВ (ПОД ВЫСОКОЙ ТЕМПЕРАТУРОЙ): C12H26 C6H14 + C6H12 Додекан гексан гексен С8Н18 С4Н10 + С4Н8
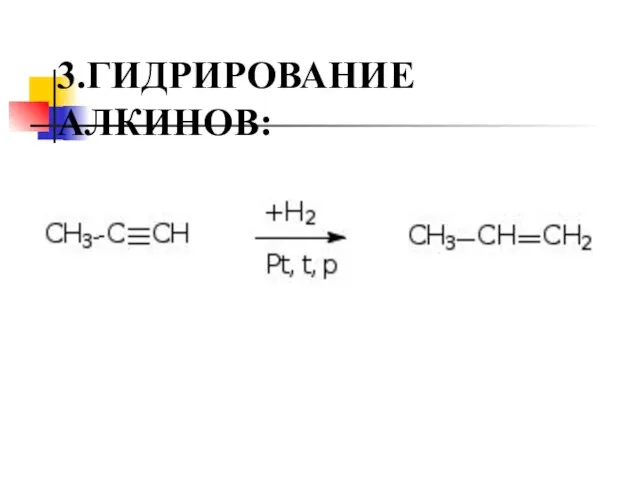
- 21. 3.ГИДРИРОВАНИЕ АЛКИНОВ:
- 22. 4.ДЕГИДРАТАЦИЯ* СПИРТОВ (ПОЛУЧЕНИЕ В ЛАБОРАТОРИИ): СН3-CH2-CH2-OH → СН3-CH=CH2 + H2O t>140°C, H2SO4(конц.) *Правило А. М. Зайцева:
- 23. 5.ДЕГИДРОГАЛОГЕНИРОВАНИЕ* ГАЛОГЕНАЛКАНОВ (ПО ПРАВИЛУ ЗАЙЦЕВА) спиртовой раствор, t CH3-CH2-CH2-Cl +NaOH → CH3-CH=CH2+NaCl+H2O C3H7Cl + NaOH =
- 24. 6.ДЕГАЛОГЕНИРОВАНИЕ ДИГАЛОГЕНАЛКАНОВ: t, спирт. раствор C2H4Cl2 + Zn → C2H4 + ZnCl2
- 26. Скачать презентацию














 Мельхіор, Нейзильбер, застосування і склад інших сплавів для приборів в ТВКП
Мельхіор, Нейзильбер, застосування і склад інших сплавів для приборів в ТВКП Предмет органической химии. Теория строения органических веществ А.М. Бутлерова
Предмет органической химии. Теория строения органических веществ А.М. Бутлерова Углеводы. Карбоновые кислоты и их производные
Углеводы. Карбоновые кислоты и их производные Презентация по Химии "Пиримидин. Пиримидиновые основания" - скачать смотреть
Презентация по Химии "Пиримидин. Пиримидиновые основания" - скачать смотреть  Метаболизм азота
Метаболизм азота Арены. Бензол. Среди 22 миллионов органических соединений немного найдется таких , которые оказали на развитие органической химии
Арены. Бензол. Среди 22 миллионов органических соединений немного найдется таких , которые оказали на развитие органической химии  Применение элетролиза в промышленности
Применение элетролиза в промышленности Тренажер Знаки Хэ
Тренажер Знаки Хэ Эукариоты
Эукариоты ФОСФОР «СВЕТОНОСНЫЙ»
ФОСФОР «СВЕТОНОСНЫЙ»  Дисперсные системы. Способы получения и очистки коллоидных систем. (Лекция 5)
Дисперсные системы. Способы получения и очистки коллоидных систем. (Лекция 5) Информационно – исследовательский проект Кристаллы вокруг нас.
Информационно – исследовательский проект Кристаллы вокруг нас. Тотығу стрестің өсімдіктерге әсері
Тотығу стрестің өсімдіктерге әсері Задача №2 «Спящий Амур». Команда гимназии №1 «Берлинская лазурь»
Задача №2 «Спящий Амур». Команда гимназии №1 «Берлинская лазурь» Шоколад. Плюсы и минусы
Шоколад. Плюсы и минусы Симметрия кристаллических решеток
Симметрия кристаллических решеток Силікагель, модифікований морином, для подальшого визначення цирконію
Силікагель, модифікований морином, для подальшого визначення цирконію Оксигеновмісні сполуки Підготувала учениця 11-Б класу Нововолинського ліцею-інтернату Волинської обласної ради Федина Вале
Оксигеновмісні сполуки Підготувала учениця 11-Б класу Нововолинського ліцею-інтернату Волинської обласної ради Федина Вале Презентация по Химии "Все о пищевых добавках класса Е" - скачать смотреть
Презентация по Химии "Все о пищевых добавках класса Е" - скачать смотреть  Строение и свойства аминокислот и белков
Строение и свойства аминокислот и белков Физические явления в химии (8 класс)
Физические явления в химии (8 класс) Карбоновые кислоты и их производные. (Лекция 11)
Карбоновые кислоты и их производные. (Лекция 11) Продукты - рекордсмены по содержанию различных минеральных компонентов
Продукты - рекордсмены по содержанию различных минеральных компонентов Что такое оксиды?
Что такое оксиды? ЗАСТОСУВАННЯ РІДКИХ КРИСТАЛІВ Виконала учениця 10 класу Гаєвська Зоряна
ЗАСТОСУВАННЯ РІДКИХ КРИСТАЛІВ Виконала учениця 10 класу Гаєвська Зоряна  Генетическая классификация горных пород
Генетическая классификация горных пород Пролекарственные стратегии в создании клинически используемых лекарственных средств
Пролекарственные стратегии в создании клинически используемых лекарственных средств Общие представления об электрохимических технологиях
Общие представления об электрохимических технологиях