Содержание
- 2. Ожирение Среди человеческой популяции ожирение представляет собой наиболее частое отклонение в обмене ТАГ. Эту патологию диагносцируют
- 3. Синтез и использование кетоновых тел В постабсорбтивный период и при голодании мобилизация ТАГ сопровождается повышением концентрации
- 4. Синтез и использование кетоновых тел Когда концентрация ацетил-КоАв матриксе митохондрий становится высокой,тиолаза катализирует обращение последней реакцииβ-окисленияи
- 5. Рис. 9.23. Метаболизм ВЖК в митохондриях печени в условиях голодания
- 6. Рис. 9.24. Синтез кетоновых тел в митохондриях печени
- 7. Синтез и использование кетоновых тел – при сахарном диабете всеми инсулин зависимыми тканями, за исключением печени.
- 8. Рис. 9.25. Окисление кетоновых тел
- 9. Метаболизм эйкозаноидов Эйкозаноиды — это группа сигнальных молекул местного действия, которые синтезируются практически во всех дифференцированных
- 10. Рис. 9.26. Освобождение арахидоновой кислоты из мембранных липидов. Связывание активаторов с рецептором плазматической мембраны активирует пути
- 11. Метаболизм эйкозаноидов В разных тканях арахидоновая и другие эйкозановые кислоты могут использоваться по трем основным направлениям:
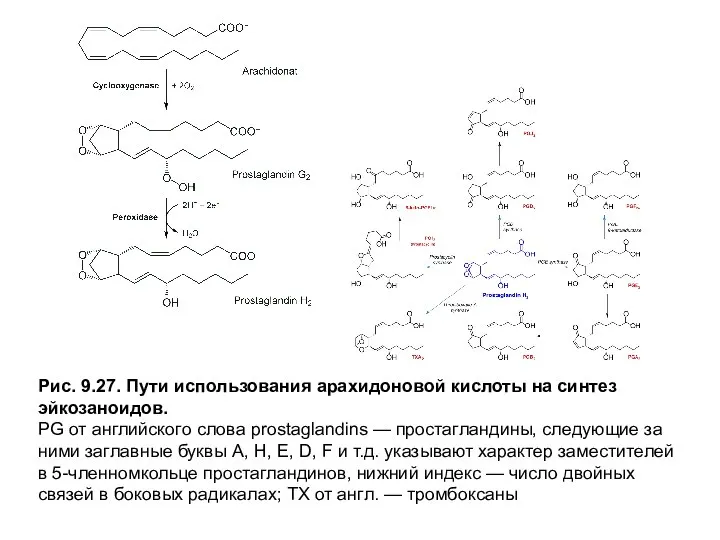
- 12. Рис. 9.27. Пути использования арахидоновой кислоты на синтез эйкозаноидов. PG от английского слова prostaglandins — простагландины,
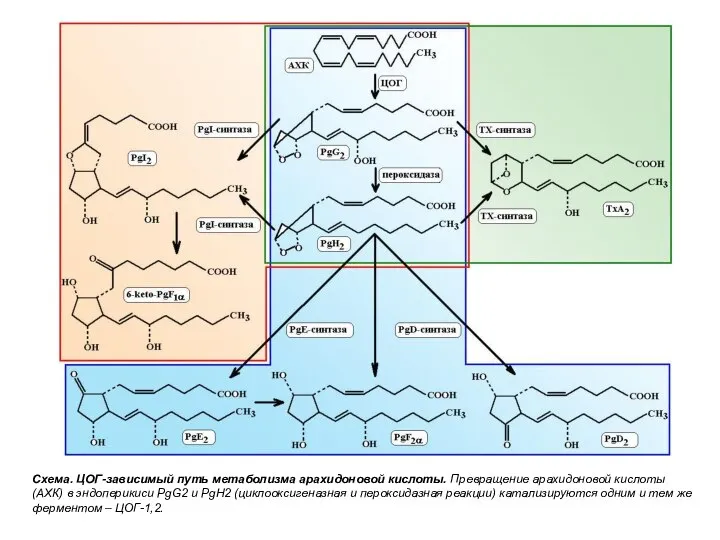
- 13. Схема. ЦОГ-зависимый путь метаболизма арахидоновой кислоты. Превращение арахидоновой кислоты (АХК) в эндоперикиси PgG2 и PgH2 (циклооксигеназная
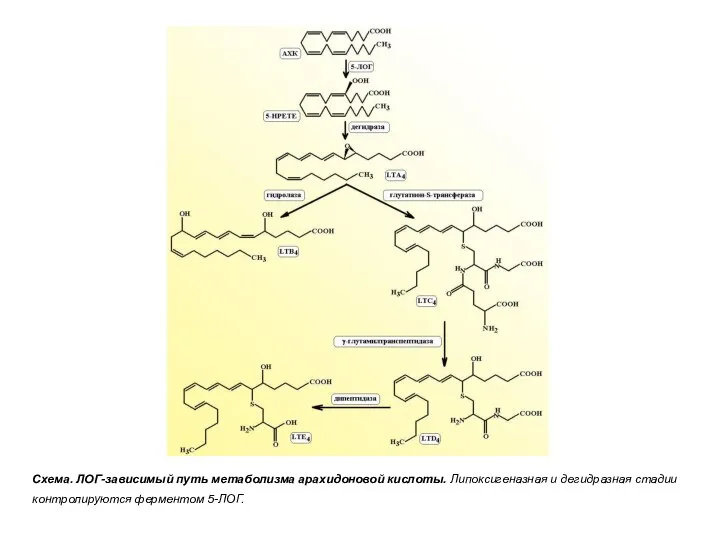
- 14. Схема. ЛОГ-зависимый путь метаболизма арахидоновой кислоты. Липоксигеназная и дегидразная стадии контролируются ферментом 5-ЛОГ.
- 15. Метаболизм эйкозаноидов Основным общим предшественником простагландинов и тромбоксанов из семейства арахидоновой кислоты является PGН2, который синтезируется
- 16. Метаболизм эйкозаноидов Другой путь превращений арахидоновой кислоты катализируют липоксигеназы — группа ферментов, присоединяющих молекулу кислорода к
- 17. Метаболизм эйкозаноидов Под влиянием монооксигеназ, работающих с участием цитохромов Р 450, образуются эпоксиды, некоторые виды ГЭТЕ,
- 18. Метаболизм эйкозаноидов
- 19. Обмен холестерола Холестерол — основной стероид организма животных. У взрослого человека содержание холестерола составляет 140–150г. Около
- 20. Обмен холестерола Путь поступления экзогенного холестерола Холестерол содержится только в жирах животного происхождения в свободном виде
- 21. Рис. 9.28. Образования эфиров холестерола: АХАТ — ацилхолестеролацилтрансфераза
- 22. Обмен холестерола Синтез холестерола de novo Ферменты синтеза холестерола имеются практически во всех клетках организма, но
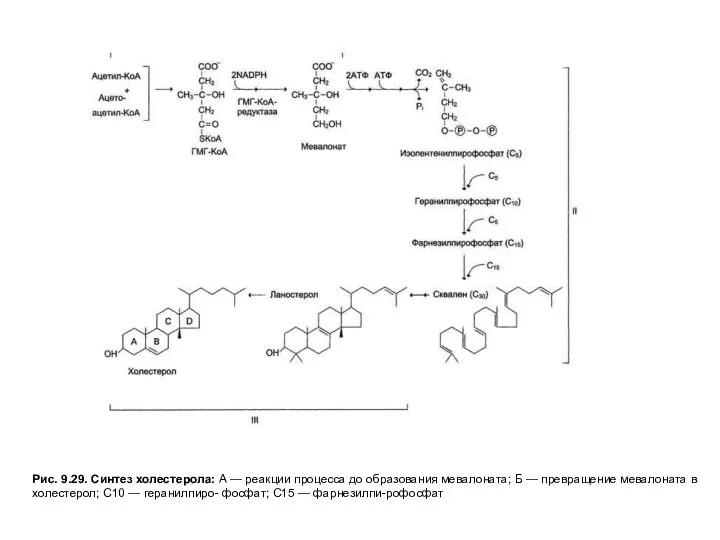
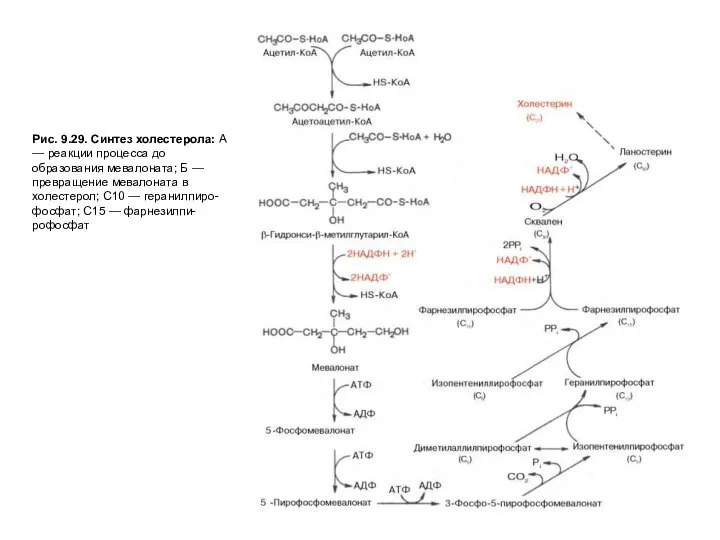
- 23. Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната; Б — превращение мевалоната в
- 24. Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната; Б — превращение мевалоната в
- 25. Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната; Б — превращение мевалоната в
- 26. Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната; Б — превращение мевалоната в
- 27. Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната; Б — превращение мевалоната в
- 28. Обмен холестерола. Синтез холестерола de novo Ключевой регуляторный фермент —ГМГ-КоА-редуктаза,активность которого в печени регулируется трояким способом
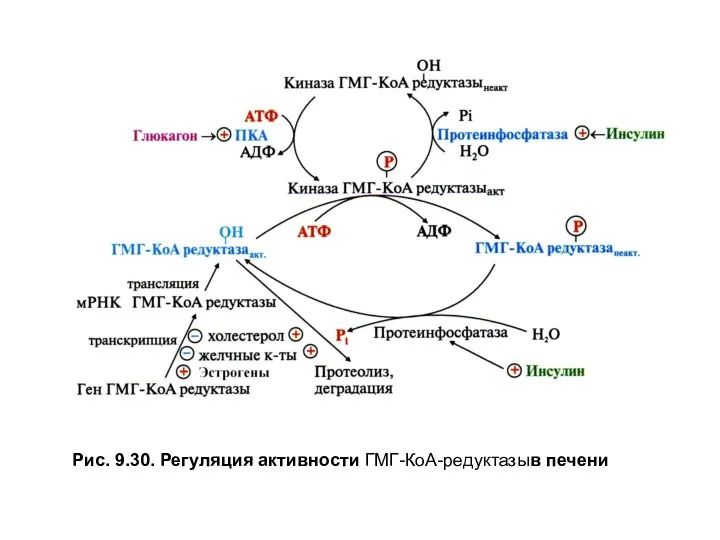
- 29. Рис. 9.30. Регуляция активности ГМГ-КоА-редуктазыв печени
- 30. Обмен холестерола. Синтез и функции желчных кислот В печени ежесуточно около 0,5 г холестерола используется на
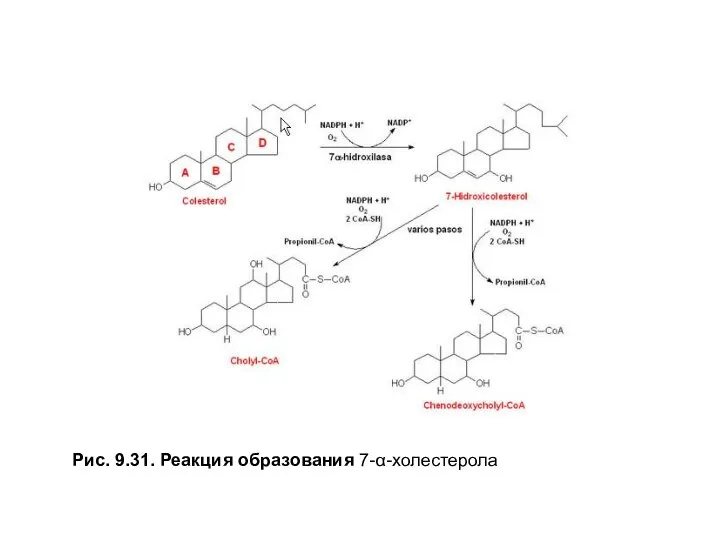
- 31. Рис. 9.31. Реакция образования 7-α-холестерола
- 32. Обмен холестерола. Синтез и функции желчных кислот Затем происходит восстановление двойной связи В-кольцаи часть молекул подвергается
- 33. Рис. 9.32. Конъюгация желчных кислот
- 34. Обмен холестерола. Синтез и функции желчных кислот Свободные и парные или конъюгированные желчные кислоты, синтезирующиеся печенью,
- 36. Рис. 9.33. Энтерогепатическая циркуляция желчных кислот
- 37. Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов В транспорте холестерола и его эфиров по
- 38. Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов Важную роль в обмене холестерола играют ЛПВП.
- 39. Рис. 9.34. Реакция, катализируемая ЛХАТ: ЛХАТ — лецитинхолестеролацилтрансфераза
- 40. Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов Второй продукт реакции — лизолецитин связывается с
- 41. Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов Ворганизме ХМ и ЛПОНП с помощью ЛП-липазыобеспечивают
- 42. Рис. 9.35. Участие ЛПВП в транспорте холестерола
- 43. Обмен холестерола. Гиперлипидемии и атеросклероз В норме общая концентрация холестерола ( свободный Хс + ЭХс )
- 44. Обмен холестерола. Гиперлипидемии и атеросклероз Таблица 9.3
- 45. Обмен холестерола. Гиперлипидемии и атеросклероз Таблица 9.3
- 46. Обмен холестерола. Гиперлипидемии и атеросклероз в норме у взрослого человека этот показатель не должен превышать 3–4.
- 48. Скачать презентацию
Ожирение
Среди человеческой популяции ожирение представляет собой наиболее частое отклонение в
Ожирение
Среди человеческой популяции ожирение представляет собой наиболее частое отклонение в
–генетические факторы (80% случаев);
–уровень физической активности;
–количество потребляемой пищи;
–эндокринные нарушения.
К генетическим факторам относят:
слабое функционирование бесполезных циклов, в которых имеет место одновременное протекание реакций гликолиза и глюконеогенеза, благодаря чему происходит нецелевое расходование энергии АТФ (рис. 9.18). В результате осуществляется сбережение и преимущественное депонирование энергоносителей, прежде всего жиров;
•прочное сопряжение дыхания и окислительного фосфорилирования, оно препятствует бесполезной трате энергии и сохраняет коэффициент Р ⁄ О на высоком уровне
•высокую эффективность работы Na+/K+ АТФазы, на долю которой приходится до 30% потребляемой клеткой энергии, это обеспечивает экономное использование АТФ;
мутации в гене obese, кодирующем строение белка лептина. Этот белок синтезируется в адипоцитах, секретируется в кровь и взаимодействует с рецепторами гипоталамуса. Связывание лептина с рецептором ингибирует секрецию нейропептида Y, ответственного за пищевое поведение, поиск и потребление пищи;
•мутации в рецепторе лептина.
Мутации в генах obese и рецептора лептина являются наиболее частой причиной ожирения. В последнем случае отмечается высокое содержание лептина в крови, а центр голода в гипоталамусе продолжает синтезировать и секретировать нейропептид Y.
Синтез и использование кетоновых тел
В постабсорбтивный период и при голодании
Синтез и использование кетоновых тел
В постабсорбтивный период и при голодании
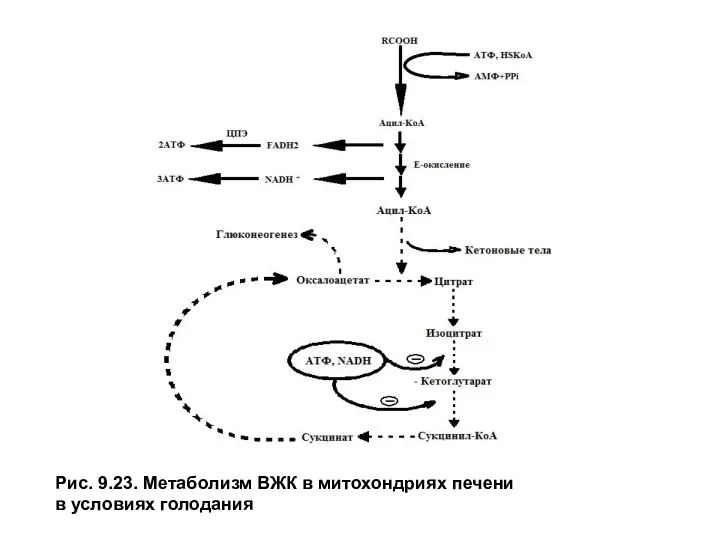
Синтез кетоновых тел осуществляется только в митохондриях гепатоцитов с использованием ацетил-КоА,образующегося приβ-окисленииВЖК. Слабое окисление ацетильного остатка в цитратном цикле объясняется тем, что β — окисление дает много АТФ и NADH + H+, которые ингибируют регуляторные реакции цитратного цикла (изоцитратдегидрогеназу иα-кето-глутаратдегидрогеназный комплекс). Оксалоацетат — исходный субстрат для синтеза цитрата, в этих условиях поступает из митохондрий в цитозоль на синтез глюкозы в процессе глюконеогенеза.
Синтез и использование кетоновых тел
Когда концентрация ацетил-КоАв матриксе митохондрий становится высокой,тиолаза катализирует
Синтез и использование кетоновых тел
Когда концентрация ацетил-КоАв матриксе митохондрий становится высокой,тиолаза катализирует
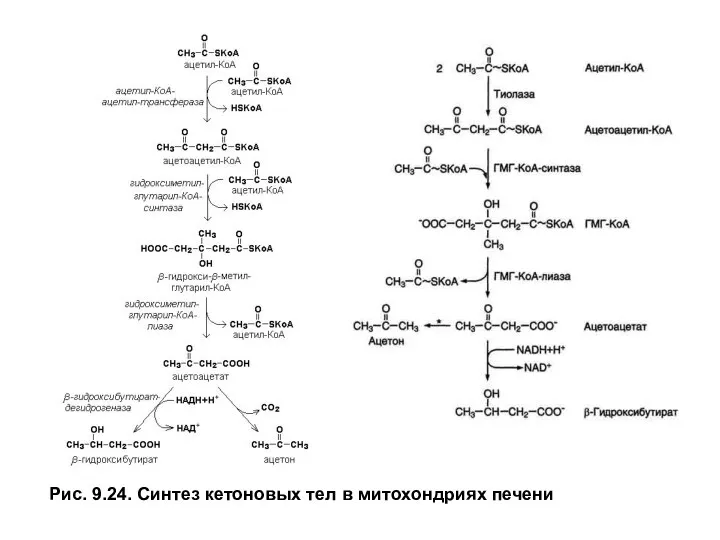
При более чем 3-дневномголодании и сахарном диабете ацетоацетат способен неферментативно декарбоксилироваться с образованием ацетона
и СО2.
Концентрация кетоновых тел повышается после ночного голодания до 1–2мг/дл, после недельного голодания она составляет20–30мг/дл , а при тяжелых формах сахарного диабета может достигать300–400мг/дл. Поскольку кетоновые тела являются органическими кислотами (рК~ 3,5), способными к диссоциации:
СН3-СО-СН2-СООН<=>СН3-СО-СН2-СОО- + Н+, их накопление может приводить к кетоацидозу и сопровождаться уменьшением щелочного резерва крови. Опасная ситуация может возникать при сахарном диабете, когда отмечается высокое содержание кетоновых тел, способное вызывать снижение рН крови (некомпенсированный ацидоз).
Кетоновые тела используются :
–в период голодания мышцами, почками, кишечником, мозгом и нервной тканью;
–при длительной физической работе мышечной тканью;
Рис. 9.23. Метаболизм ВЖК в митохондриях печени
в условиях голодания
Рис. 9.23. Метаболизм ВЖК в митохондриях печени
в условиях голодания
Рис. 9.24. Синтез кетоновых тел в митохондриях печени
Рис. 9.24. Синтез кетоновых тел в митохондриях печени
Синтез и использование кетоновых тел
– при сахарном диабете всеми инсулин
Синтез и использование кетоновых тел
– при сахарном диабете всеми инсулин
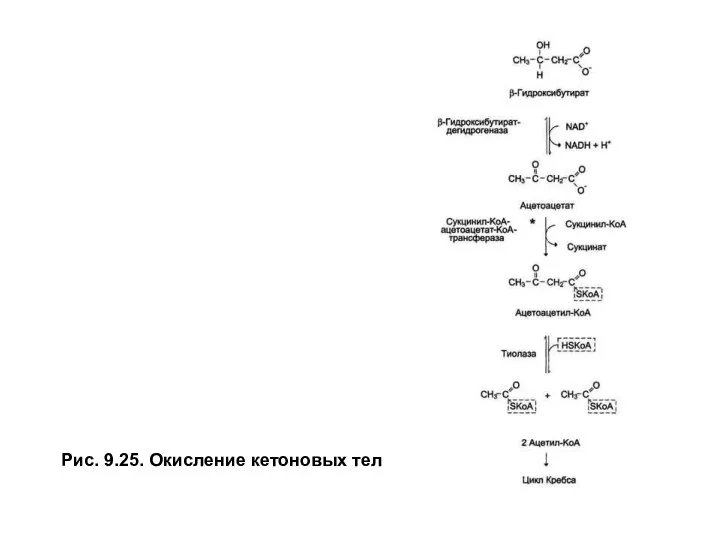
Окисление кетоновых тел — аэробный процесс, происходящий в матриксе митохондрий при участии ферментов, указанных на рис. 9.25.
β-гидроксибутиратокисляетсяβ-гидроксибутиратдегидрогеназойдо ацетоацетата, который активируется, получая остаток–КоАотсукцинил-КоА-промежуточного продукта цитратного цикла. Затемацетоацетил-КоАрасщепляется на две молекулыацетил-КоА,которые вовлекаются в цитратный цикл и полностью окисляются до СО2 и Н2О. Печень не способна использовать кетоновые тела, поскольку лишена фермента —сукцинил-КоА-ацетоацетат-КоА- трансферазы, катализирующего активацию ацетоацетата.
Кетоновые тела относятся к энергоносителям: при окислении ацетоацетата выход энергии равен 23 молям АТФ на 1 моль субстрата (2 ацетил-КоА→ 24 АТФ — 1 АТФ на активацию ) и 26 моль АТФ на 1 мольβ-гидроксибутиратаза счет участия в процессе окисленияβ-гидроксибутиратдегидрогеназы.
Рис. 9.25. Окисление кетоновых тел
Рис. 9.25. Окисление кетоновых тел
Метаболизм эйкозаноидов
Эйкозаноиды — это группа сигнальных молекул местного действия, которые синтезируются
Метаболизм эйкозаноидов
Эйкозаноиды — это группа сигнальных молекул местного действия, которые синтезируются
Основным субстратом для синтеза эйкозаноидов является арахидоновая (ω-6-эйкозатетраеновая)кислота, содержащая 4 двойные связи при углеродных атомах (∆ 5, 8, 11, 14). Она может поступать с пищей или синтезироваться из линолевой кислоты. В небольших количествах для синтеза эйкозаноидов могут использоватьсяω-6-эйкозатриеноваякислота с тремя двойными связями (∆ 5, 8, 11) иω-3-эйкозапентаеноваякислота, в составе которой имеется 5 двойных связей в положениях ∆ 5, 8, 11, 14, 17. Обе минорные эйкозановые кислоты либо поступают с пищей, либо синтезируются из олеиновый и линоленовой кислот соответственно.
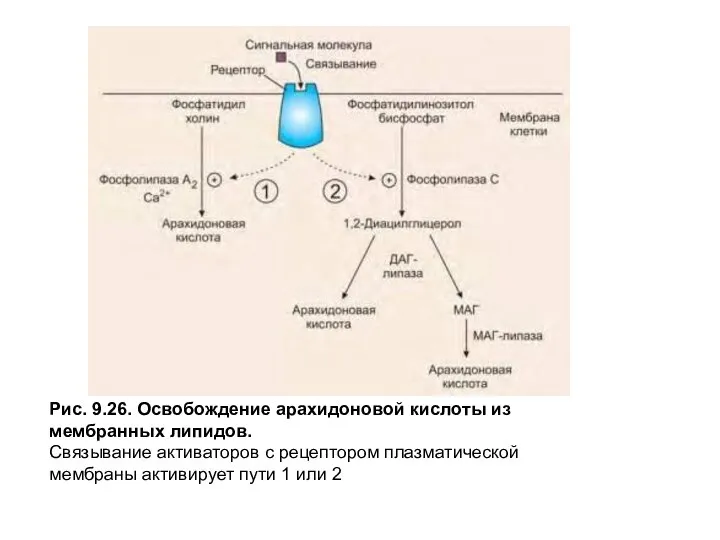
Полиненасыщенные жирные кислоты первоначально включаются в состав мембранных фосфолипидов, а затем освобождаются из них под действием фосфолипазы А 2 или фосфолипазы С, которые активируются при поступлении соответствующего сигнала на рецептор плазматической мембраны (рис. 9.26).
Рис. 9.26. Освобождение арахидоновой кислоты из мембранных липидов.
Связывание активаторов с рецептором
Рис. 9.26. Освобождение арахидоновой кислоты из мембранных липидов.
Связывание активаторов с рецептором
Метаболизм эйкозаноидов
В разных тканях арахидоновая и другие эйкозановые кислоты могут
Метаболизм эйкозаноидов
В разных тканях арахидоновая и другие эйкозановые кислоты могут
•циклооксигеназный путь ведет к образованию простагландинов и тромбоксанов;
•липоксигеназа превращает арахидоновую кислоту в лейкотриены, липоксины и гидроксиэйкозатетраеноаты (ГЭТЕ);
•система окисления с участием цитохрома Р450 ответственна за синтез эпоксидов.
Простагландины, образующиеся под действием циклооксигеназы и пероксидазы, содержат 5-членноекольцо, в состав которого входят атомы углерода с С8 по С12 эйкозановой кислоты, гидроксильную группу у С15 и от одной до трех двойных связей в боковых цепях (рис. 9.27). В С9- иС11-позицияхкольца находятся заместители — это обычно кетоили гидроксильные группы.
Номенклатура простагландинов включает следующие обозначения: PG от слова простагландин, следующие заглавные буквы А, Е, D и т.д. указывают на характер заместителей в 5-членномкольце, а нижний индекс — число двойных связей в боковых радикалах. Количество двойных связей зависит от типа эйкозановой кислоты, которая была субстратом для синтеза простагландинов. Эйкозатриеновая кислота образует семейство PG с 1 двойной связью между С13 и С14 (например, PGЕ1), арахидоновая — семейство простагландинов с 2 двойными связями в положениях С5 = С6 и С13 = С14 (PGЕ2), а эйкозапентаеновая — семейство с 3 двойными связями в участках С5 = С6 , С13 = С14 и С17 = С18 боковых цепей (PGЕ3).
Рис. 9.27. Пути использования арахидоновой кислоты на синтез эйкозаноидов.
PG от английского
Рис. 9.27. Пути использования арахидоновой кислоты на синтез эйкозаноидов.
PG от английского
Схема. ЦОГ-зависимый путь метаболизма арахидоновой кислоты. Превращение арахидоновой кислоты (АХК) в
Схема. ЦОГ-зависимый путь метаболизма арахидоновой кислоты. Превращение арахидоновой кислоты (АХК) в
Схема. ЛОГ-зависимый путь метаболизма арахидоновой кислоты. Липоксигеназная и дегидразная стадии контролируются
Схема. ЛОГ-зависимый путь метаболизма арахидоновой кислоты. Липоксигеназная и дегидразная стадии контролируются
Метаболизм эйкозаноидов
Основным общим предшественником простагландинов и тромбоксанов из семейства арахидоновой
Метаболизм эйкозаноидов
Основным общим предшественником простагландинов и тромбоксанов из семейства арахидоновой
В клетках эндотелия сосудов при участии PGI-синтазыPGН2превращается в PG I2 или простациклин, являющийся антагонистом ТХА2, он препятствует агрегации тромбоцитов и расширяет сосуды.
Метаболизм эйкозаноидов
Другой путь превращений арахидоновой кислоты катализируют липоксигеназы — группа ферментов, присоединяющих
Метаболизм эйкозаноидов
Другой путь превращений арахидоновой кислоты катализируют липоксигеназы — группа ферментов, присоединяющих
•восстанавливаться до –ОНгруппы и образовывать группу5-,12-и 15гидроксиэйкозатетраееновых (ГЭТЕ) кислот;
•превращаться в эпоксиды;
•служить субстратом для получения лейкотриенов — соединений, содержащих последовательность из 3 сопряженных двойных связей (отсюда название этой группы), хотя общее количество двойных связей может быть больше 3.
Лейкотриены участвуют в аллергических реакциях, липоксины вызывают хемотаксис и стимулируют продукцию супероксидных ионов в лейкоцитах, которые необходимы для разрушения частиц, попадающих в клетки в результате фагоцитоза.
Метаболизм эйкозаноидов
Под влиянием монооксигеназ, работающих с участием цитохромов Р 450,
Метаболизм эйкозаноидов
Под влиянием монооксигеназ, работающих с участием цитохромов Р 450,
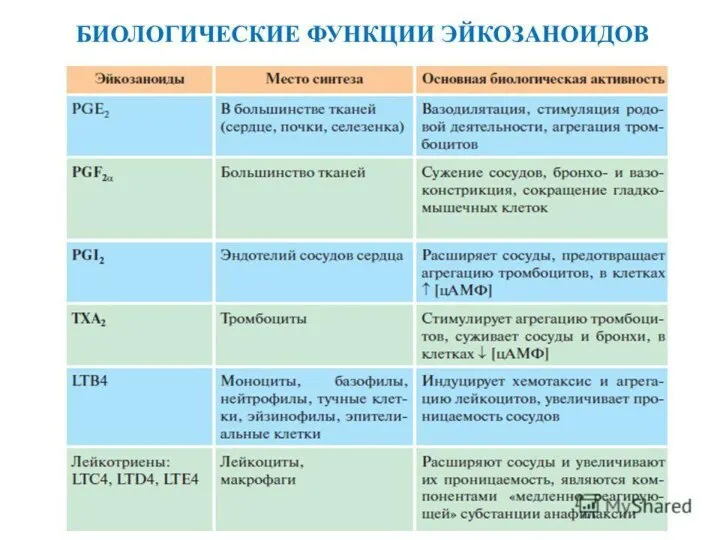
Все виды эйкозаноидов образуются в очень малых количествах и имеют короткий полупериод жизни, от нескольких секунд до нескольких минут. В разных тканях эйкозаноиды обладают разными, а иногда прямо противоположными свойствами (табл. 9.2).
Эйкозаноиды действуют на клетки-мишенипо аутоили паракринному механизму через специфические мембранные рецепторы. Присоединение эйкозаноида к рецептору включает аденилатциклазную или инозитолфосфатную систему передачи сигнала, вызывая повышение внутриклеточной концентрации вторичных вестников сигнала: цАМФ, цГМФ, или ИФ3 и Са2+.
Одним из центральных эффектов эйкозаноидов является участие в развитии воспалительной реакции, которая иногда становится продолжительной и приносит физические страдания людям. Для уменьшения воспаления используют ингибиторы синтеза простагландинов — нестероидные противовоспалительные соединения (НПВС): аспирин, ацетаминофен, индометацин, диклофенак и др. Все препараты этой группы ингибируют циклооксигеназу: аспирин — необра-тимо, и поэтому для восстановления синтеза простагландинов требуется синтез новых молекул фермента (~ 48 часов), а ипопрофен, индометацин, фенилбутазон — обратимо по конкурентному типу. НПВС не действуют на синтез лейкотриенов, образование которых может увеличиться при ингибировании циклооксигеназного пути использования арахидоновой кислоты, поэтому в ряде случаев использование этих препаратов может вызвать приступ бронхиальной астмы («аспириновую» астму).
Метаболизм эйкозаноидов
Метаболизм эйкозаноидов
Обмен холестерола
Холестерол — основной стероид организма животных. У взрослого человека
Обмен холестерола
Холестерол — основной стероид организма животных. У взрослого человека
Холестерол является предшественником всех стероидов животного организма:
•желчных кислот, содержание которых у взрослого человека составляет около 5 г;
•стероидных гормонов: кортикостероидов, образующихся в корковом слоенадпочечников, андрогенов — в семенниках и эстрагенов — в яичниках, синтез общего количества которых не превышает 40 мг ⁄с (с — сутки);
•витамина Д3, синтезирующегося в коже под действием УФО в количестве 10 мг ⁄с.
Холестериновое равновесие поддерживается благодаря тому, что с одной стороны холестерол поступает с пищей (~ 0,3 — 0,5 г ⁄ с ) и синтезируется в печени или других тканях (~ 0,5 г ⁄с ), а с другой — выводится с калом в виде желчных кислот, холестерола желчи, продуктов катаболизма стероидных гормонов, с кожным салом, в составе мембран слущенного эпителия (~ 1,0 г ⁄с ).
Обмен холестерола
Путь поступления экзогенного холестерола
Холестерол содержится только в жирах животного
Обмен холестерола
Путь поступления экзогенного холестерола
Холестерол содержится только в жирах животного
–эмульгирование пищи мицеллами желчи;
–гидролиз эфиров холестерола холестеролэстеразой панкреатического сокаикишечника;
–всасывание продуктов гидролиза в составе смешанных мицелл.
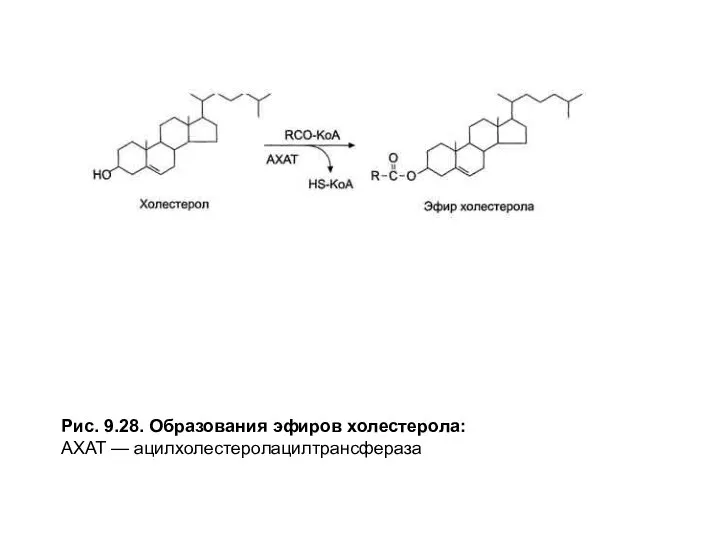
В энтероцитах часть холестерола снова этерифицируется. Этот процесс включает две стадии: активацию жирной кислоты под действием ацил-КоА-синтетазыи перенос ацильного остатка с ацил-КоАнаНО-группухолестерола в реакции, катализируемойацил-холестерол-ацилтрансферазой (АХАТ) (рис. 9.28).
В этерификации, как правило, участвуют моноили полиненасыщенные высшие жирные кислоты. Холестерол и его эфиры включаются в состав хиломикронов: эфиры холестерола — в ядро частиц, а свободный холестерол — в мембрану.
ХМ из энтероцитов через лимфу поступают в кровь, где идет созревание частиц за счет контакта и обмена белками с ЛПВП. ЛПВП передают на ХМ Апо СII и Апо Е, а ХМ на ЛПВП — АпоА1 и АпоА2. Апо СII активирует ЛПлипазу, которая гидролизует ТАГ этих частиц. Образуются ХМост, они улавливаются из кровяного русла печенью по механизму эндоцитоза с помощью рецепторов к Апо Е. Эндосомы сливаются с лизосомами, гидролитические ферменты которых расщепляют все компоненты ХМост кроме холестерола. Последний включается в общий фонд этого стероида в печени, снижая при этом синтез эндогенного холестерола иЛНП-рецепторов.
Рис. 9.28. Образования эфиров холестерола:
АХАТ — ацилхолестеролацилтрансфераза
Рис. 9.28. Образования эфиров холестерола:
АХАТ — ацилхолестеролацилтрансфераза
Обмен холестерола
Синтез холестерола de novo
Ферменты синтеза холестерола имеются практически во
Обмен холестерола
Синтез холестерола de novo
Ферменты синтеза холестерола имеются практически во
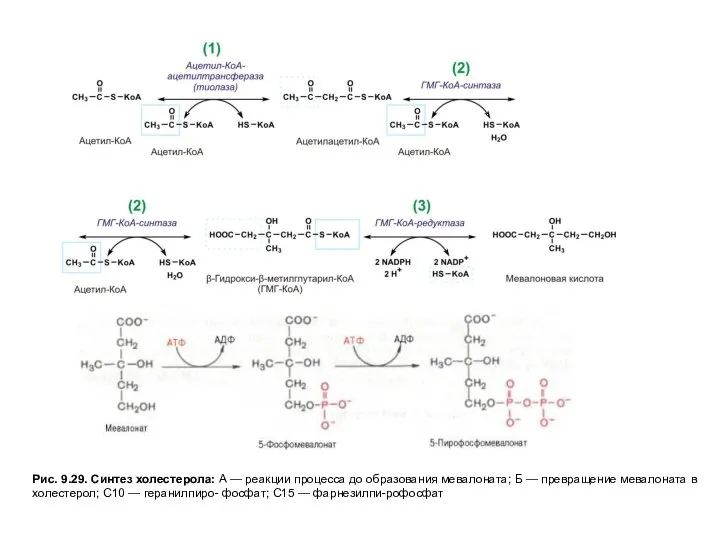
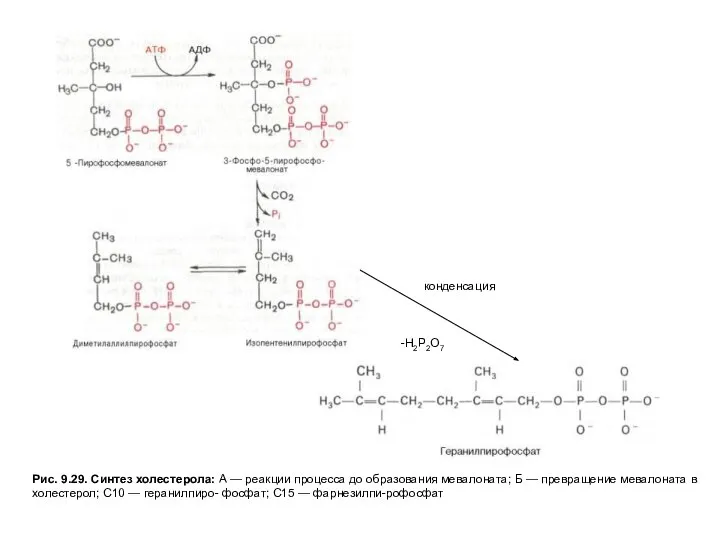
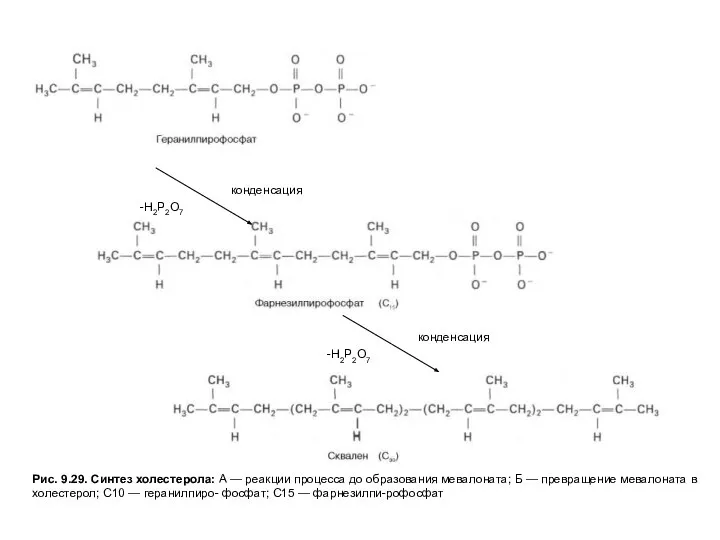
На первых стадиях процесса 18 молекул ацетил-КоАучаствуют в синтезе 6 молекулГМГ-КоА,в реакциях, сходных с реакциями синтеза кетоновых тел. Далее фермент ЭПРГМГ-КоА-редуктаза восстанавливаетГМГ-КоАвмевалоновуюкислоту с затратой 2 молекул NADPH на каждый остатокГМГ-КоА.Молекулы мевалоната фосфорилируются с помощью АТФ, декарбоксилируются и образуют 6 пятиуглеродных производных изопрена —изопентенилпирофосфаты. При последовательной конденсации этих соединений возникает симметричная линейная30-углероднаямолекуласквалена, которая через ряд стадий приобретает тетрациклическую структуруланостерола. Дальнейшие превращения ланостерола сопровождаются потерей трех метильных групп в виде СО2 и образованием холестерола, содержащего 27 углеродных атомов, из которых 8 образуют углеводородную боковую цепь, два входят в метильные группы, а остальные 17 образуют циклопентанпергидрофенантреновую структуру.
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Рис. 9.29. Синтез холестерола: А — реакции процесса до образования мевалоната;
Обмен холестерола. Синтез холестерола de novo
Ключевой регуляторный фермент —ГМГ-КоА-редуктаза,активность которого в печени
Обмен холестерола. Синтез холестерола de novo
Ключевой регуляторный фермент —ГМГ-КоА-редуктаза,активность которого в печени
•на уровне транскрипции гена ГМГ-КоА-редуктазы.Корепрессорами процесса, снижающими скорость синтеза фермента, являются холестерол, желчные кислоты и кортикостероидные гормоны, а индукторами — инсулин и тиреоидные гормоны — Т3 и Т4;
•путем фосфорилирования и дефосфорилирования, которое также регулируется гормонами. Дефосфорилирование стимулирует инсулин, которыйза счет активации протеинфосфатазы переводит фермент в дефосфорилированную активную форму, а глюкагон через аденилатциклазную систему обеспечивает механизм его фосфорилирования и инактивации;
•уменьшением количества фермента за счет протеолиза молекул, который стимулируют холестерол и желчные кислоты.
Часть вновь синтезированного холестерола этерифицируется с образованием эфиров. Эту реакцию , как и в энтероцитах, катализирует АХАТ, присоединяя к холестеролу остатки линолевой или олеиновой кислот. Эфиры холестерола (ЭХс) — гидрофобны, образуют в цитозоле капли, которые рассматривают как способ запасания стероида в клетках. Особенно интенсивно синтез и гидролиз эфиров холестерола протекают в коре надпочечников — месте синтеза стероидных гормонов.
Печень — основной поставщик холестерола другим органам и тканям.
Рис. 9.30. Регуляция активности ГМГ-КоА-редуктазыв печени
Рис. 9.30. Регуляция активности ГМГ-КоА-редуктазыв печени
Обмен холестерола.
Синтез и функции желчных кислот
В печени ежесуточно около 0,5
Обмен холестерола.
Синтез и функции желчных кислот
В печени ежесуточно около 0,5
Рис. 9.31. Реакция образования 7-α-холестерола
Рис. 9.31. Реакция образования 7-α-холестерола
Обмен холестерола. Синтез и функции желчных кислот
Затем происходит восстановление двойной связи В-кольцаи
Обмен холестерола. Синтез и функции желчных кислот
Затем происходит восстановление двойной связи В-кольцаи
Активность 7-α-гидроксилазырегулируется:
•фосфорилированием и дефосфорилированием, фермент активен в фосфорилированной форме при снижении индекса инсулин ⁄глюкагон;
•изменением количества фермента, экспрессию гена стимулируют холестерол и тиреоидные гормоны, а репрессируют желчные кислоты и эстрогены.
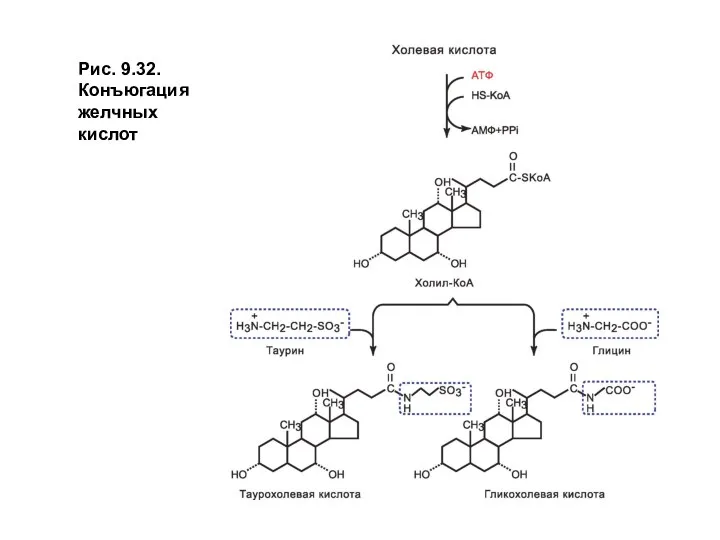
Желчные кислоты образуют производные с глицином илитаурином. Конъюгация усиливает амфифильность молекул и их эмульгирующие свойства(рис. 9.32).
Рис. 9.32. Конъюгация желчных кислот
Рис. 9.32. Конъюгация желчных кислот
Обмен холестерола. Синтез и функции желчных кислот
Свободные и парные или конъюгированные
Обмен холестерола. Синтез и функции желчных кислот
Свободные и парные или конъюгированные
Из печени желчные кислоты поступают в желчные протоки, в составе желчи хранятся в желчном пузыре и изливаются в кишечник в процессе пищеварения. Они участвуют в эмульгировании пищевых жиров и всасывании продуктов переваривания липидов.
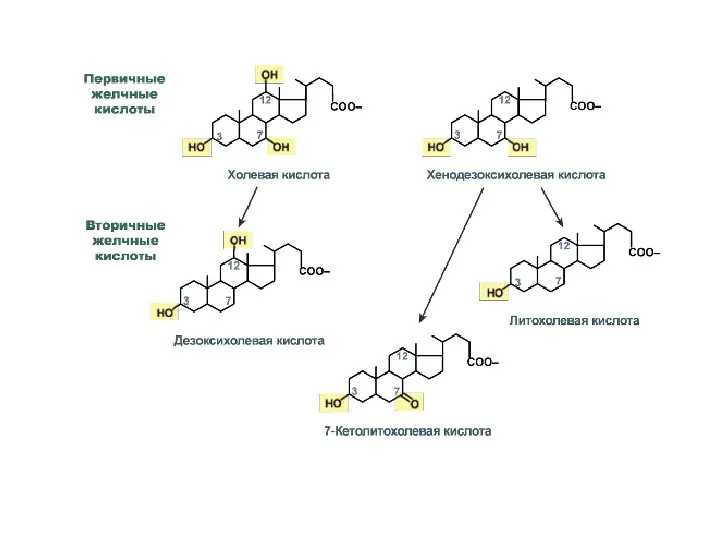
Под действием ферментов кишечной микрофлоры первичные желчные кислоты деконъюгируются и отщепляют ОН-группуиз 7 положения. Таким образом возникаютвторичные желчные кислоты: из холевой —дезоксихолевая, а из хенодезоксихолевой —литохолевая.
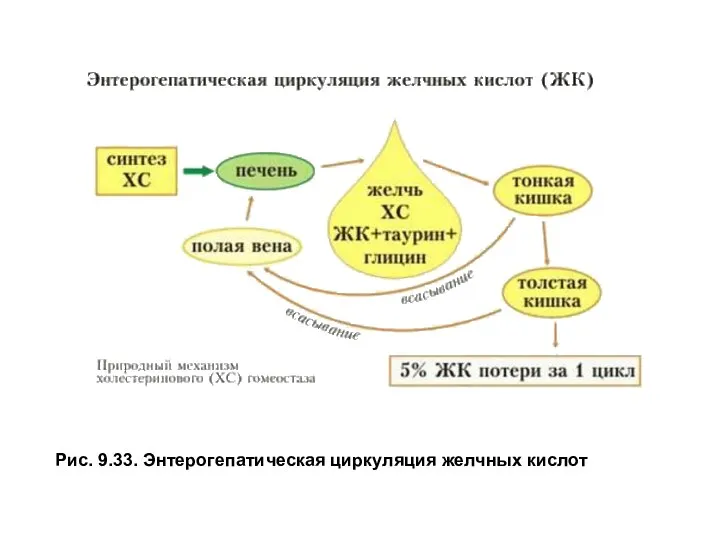
Более 95% желчных кислот всасывается из просвета кишечника, кровью воротной вены доставляется в печень и снова используется на образование желчи, участвуя в энтерогепатической циркуляции. Общее количество желчных кислот в организме составляет2–4г, за сутки они проходят энтерогепатический круг6–8раз. С калом в день выводится0,2–0,6г желчных кислот и примерно0,5–0,6г холестерола (рис. 9.33).
Снижение синтеза желчных кислот или увеличение образования холестерола в организме может приводить к относительному избытку холестерола в составе мицелл желчи и стимулировать образование холестериновых камней в желчном пузыре и протоках, т.е. к развитию желчнокаменной болезни.
Рис. 9.33. Энтерогепатическая циркуляция желчных кислот
Рис. 9.33. Энтерогепатическая циркуляция желчных кислот
Обмен холестерола.
Транспорт холестерола по крови в составе липопротеинов
В транспорте холестерола
Обмен холестерола.
Транспорт холестерола по крови в составе липопротеинов
В транспорте холестерола
ЛПНП — долгоживущие частицы и, контактируя в крови с липопротеинами, возвращают АпоСII, а иногда и АпоЕ на ЛПВП. Основными компонентами этих частиц являются холестерол и его эфиры (~ 60% ), которые ЛПНП доставляют в разные органы и ткани. Поступление ЛПНП в ткани осуществляется в помощьюЛНП-рецепторов, количество которых на клетку может варьировать от 15 000 до 70 000. Рецепторы располагаются в области белкаклатрина, выстилающего специальные участки клеточной мембраны, называемые«окаймленными ямками». При присоединении ЛПНП к рецептору окаймленная ямка втягивается в клетку, образуя эндосому. За счет кислой среды эндосомы комплексЛНП–рецептордиссоциирует, и рецептор возвращается в мембрану. Эндосома сливается с лизосомой, содержимое ЛПНП расщепляется гидролитическими ферментами, а холестерол поступает в общий фонд холестерола клетки и используется ею на собственные нужды или запасается в виде липидных капель ЭХс.
Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов
Важную роль в
Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов
Важную роль в
•обеспечивают «созревание» ХМ и ЛПОНП, отдавая на эти частицы АпоСII и АпоЕ;
•участвуют в «обратном транспорте холестерола», удаляя этот стероид из ЛП и клеточных мембран.
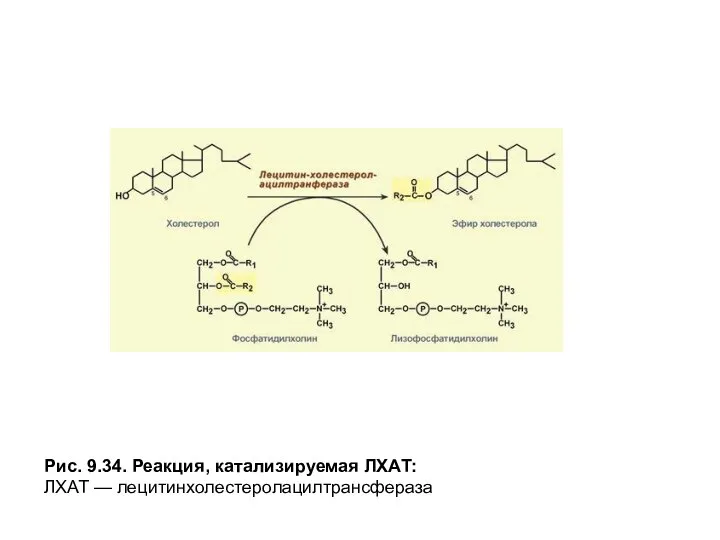
Осуществление последней функции обусловлено присутствием в мембране этих частиц фермента лецитинхолестеролацилтрансферазы (ЛХАТ), катализирующего этерификацию молекул холестерола остатками высшей жирной кислоты, входящей вβ-положениефосфатидилхолина (лецитина) (рис. 9.34).
ЛХАТ активируется белком Апо А-1,который присутствует в составе белков ЛПВП, а также поступает от ХМ и ЛПОНП в процессе обмена белками. ЭХс, образующиеся в результате этой реакции, погружаются в центральную область частицы. Места, освободившиеся в поверхностном слое, занимают новые моле-кулы холестерола, поступающие путем простой диффузии из ЛПНП и клеточных мембран. По мере накопления эфиров холестерола в ядре частицы ЛП приобретают сферическую форму и их называют зрелыми ЛПВП илиЛПВП3.
Рис. 9.34. Реакция, катализируемая ЛХАТ:
ЛХАТ — лецитинхолестеролацилтрансфераза
Рис. 9.34. Реакция, катализируемая ЛХАТ:
ЛХАТ — лецитинхолестеролацилтрансфераза
Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов
Второй продукт реакции
Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов
Второй продукт реакции
Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов
Ворганизме ХМ и
Обмен холестерола. Транспорт холестерола по крови в составе липопротеинов
Ворганизме ХМ и
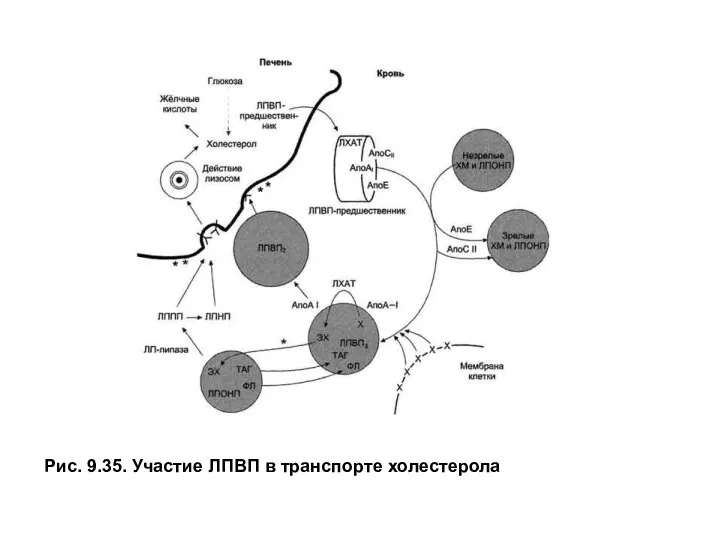
Ворганизме взрослого человека через 4–6часов после приема пищи в сыворотке крови присутствуют все основные ЛП. Через10–12часов после еды (утром натощак) отсутствуют ХМ, ЛПОНП составляют не более 15% от всех ЛП, а на долю ЛПНП и ЛПВП приходится ~ 60% и 25% от общего содержания липопротеинов крови соответственно (рис.9.35)
Рис. 9.35. Участие ЛПВП в транспорте холестерола
Рис. 9.35. Участие ЛПВП в транспорте холестерола
Обмен холестерола.
Гиперлипидемии и атеросклероз
В норме общая концентрация холестерола ( свободный Хс
Обмен холестерола.
Гиперлипидемии и атеросклероз
В норме общая концентрация холестерола ( свободный Хс
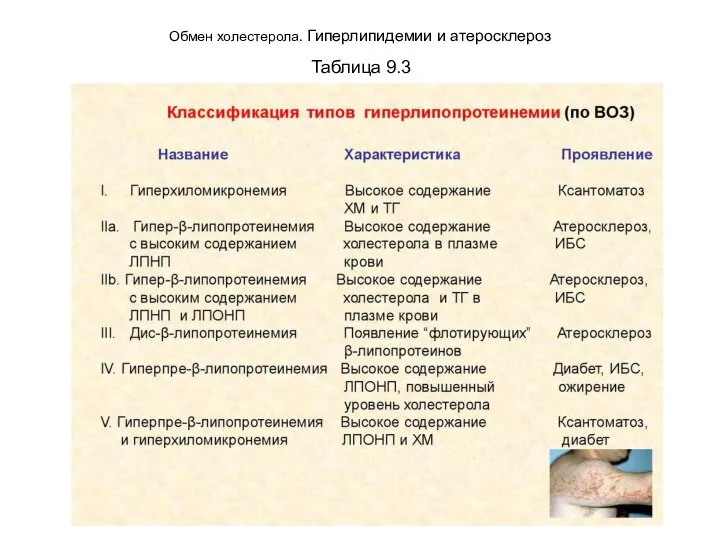
•гипертриацилглицеролемией (повышением концентрации ХМ или ЛПОНП);
•гиперхолестеролемией (повышением концентрации ЛПНП);
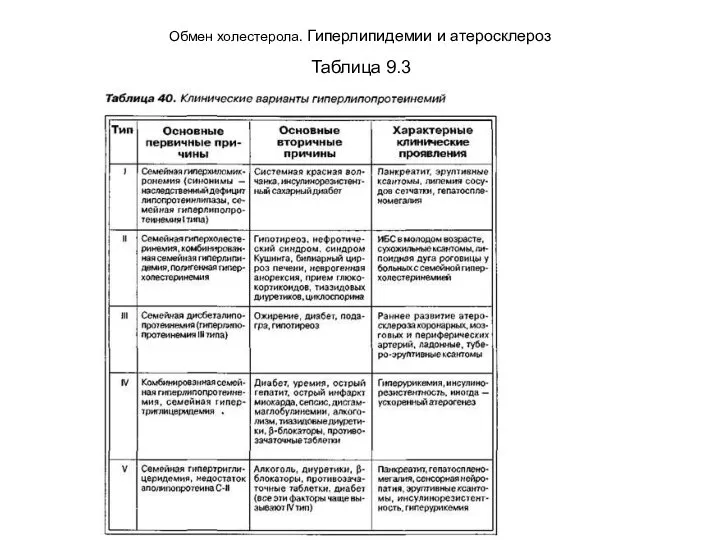
•смешанной формой: совместным повышением концентрации Хс и ТАГ. Гиперлипидемии относятся к наиболее распространенным нарушениям обме-
на веществ, от которого страдает примерно каждый десятый человек. Они могут быть вызваны изменениями в генетическом аппарате клеток или являются следствием хронических заболеваний: сахарного диабета, гепатитов, алкоголизма, поражений почек (табл. 9.3).
Обмен холестерола. Гиперлипидемии и атеросклероз
Таблица 9.3
Обмен холестерола. Гиперлипидемии и атеросклероз
Таблица 9.3
Обмен холестерола. Гиперлипидемии и атеросклероз
Таблица 9.3
Обмен холестерола. Гиперлипидемии и атеросклероз
Таблица 9.3
Обмен холестерола. Гиперлипидемии и атеросклероз
в норме у взрослого человека этот показатель
Обмен холестерола. Гиперлипидемии и атеросклероз
в норме у взрослого человека этот показатель
Развитию атеросклероза благоприятствует продолжительный полупериод жизни ЛПНП (t 1/2 =2–6суток). Экзо- и эндогенные факторы могут нарушать структуру ЛПНП и их рецепторов, снижая эффективность взаимодействия между ними в результате:
Гиперхолестеринемия провоцирует развитие атеросклероза. Вероятность развития болезни тем выше, чем выше концентрация ЛПНП и ниже концентрация ЛПВП. Для выявления предрасположенности пациента к заболеваниям, вызванным атеросклеротическими изменениями сосудов, определяют коэффициент атерогенности:
или натощак






















 Органические и неорганические вещества. Нуклеиновые кислоты
Органические и неорганические вещества. Нуклеиновые кислоты ОМЕГА 3 и ОМЕГА 6 полиненасыщенные жирные кислоты (ПНЖК) Все более популярными в ветеринарии становятся ОМЕГА 3 и ОМЕГА 6 полиненасы
ОМЕГА 3 и ОМЕГА 6 полиненасыщенные жирные кислоты (ПНЖК) Все более популярными в ветеринарии становятся ОМЕГА 3 и ОМЕГА 6 полиненасы Тест: Азот
Тест: Азот Витамины и их производные-коферменты ферментов
Витамины и их производные-коферменты ферментов Получение гидроксида никеля (II)
Получение гидроксида никеля (II) Розчини електролітів
Розчини електролітів Вода – растворитель. Растворы. Значение воды
Вода – растворитель. Растворы. Значение воды Використання кислот
Використання кислот Гелий
Гелий Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4)
Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4) Карбон қышқылдары
Карбон қышқылдары Вступ в гетерогенний катализ. Загальні положення каталізу
Вступ в гетерогенний катализ. Загальні положення каталізу Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Жиры. 9 класс
Жиры. 9 класс ОКСИДЫ АЗОТА.
ОКСИДЫ АЗОТА.  ВПР Окружающий мир 4 класс
ВПР Окружающий мир 4 класс  Урок по теме: «Жиры. Техническая переработка жиров» Пермякова Ирина Александровна Учитель химии ГБОУ СОШ № 982 г. Москва Индиф
Урок по теме: «Жиры. Техническая переработка жиров» Пермякова Ирина Александровна Учитель химии ГБОУ СОШ № 982 г. Москва Индиф Условия хранения и подготовка скоропортящихся грузов к перевозкам
Условия хранения и подготовка скоропортящихся грузов к перевозкам Инертные газы
Инертные газы Агрегатные состояния вещества
Агрегатные состояния вещества Нанопористые материалы
Нанопористые материалы Предельные углеводороды. Химические свойства. 10 класс
Предельные углеводороды. Химические свойства. 10 класс Природные и синтетические красители и ароматизаторы
Природные и синтетические красители и ароматизаторы Химические свойства фурана, пиррола, тиофена. Биологически активные производные ряда фурана, пиррола, тиофена. (Лекция 3)
Химические свойства фурана, пиррола, тиофена. Биологически активные производные ряда фурана, пиррола, тиофена. (Лекция 3) МОУ «Каратунская СОШ с углубленным изучением отдельных предметов» Выполнила : учитель химии второй квалификационной категор
МОУ «Каратунская СОШ с углубленным изучением отдельных предметов» Выполнила : учитель химии второй квалификационной категор Элективный курс "Решение задач по химии повышенного уровня сложности"
Элективный курс "Решение задач по химии повышенного уровня сложности" Сложные эфиры R-COOR'
Сложные эфиры R-COOR' Оценка опасности взрыва горючих газов
Оценка опасности взрыва горючих газов