Содержание
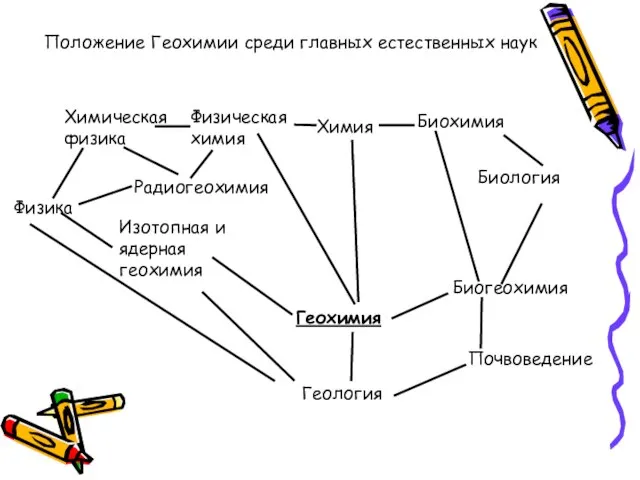
- 2. Положение Геохимии среди главных естественных наук
- 3. Вернадский Владимир Иванович (1863–1945) Русский минералог, кристаллограф, геолог, геохимик, историк и организатор науки, философ, общественный деятель.
- 4. ГЕОХИМИЯ – наука, изучающая химический состав Земли, распространенность в ней химических элементов и их стабильных изотопов,
- 5. Поведение и формы нахождения химических элементов в различных оболочках Земли (геосферах и при различных геологических процессах).
- 6. Изучение изоморфных смесей; типоморфизм минералов. Изучение геохимии отдельных регионов земной коры. Дальнейшее повышение чувствительности и точности
- 7. Геохимическая зональность. Законы дифференциации вещества Земли. Взаимодействие вещества мантии и коры. Геохимия мантии Земли. Кинетика и
- 8. Происхождение химических элементов. Рациональное (комплексное) использование земных ресурсов. Гипергенное минералообразование. Геохимия ноосферы. Сохранение среды жизнеобитания. Геохимия
- 9. Методы исследования: Химические методы Физические методы Геологические методы Методы составления диаграмм Методика петрохимических модулей Геохимическое картирование
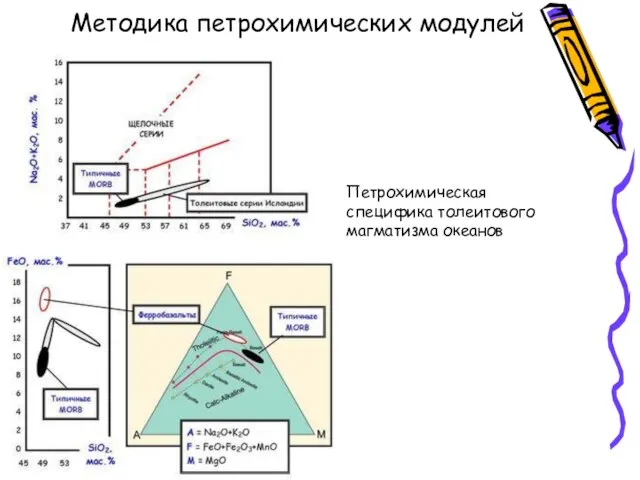
- 10. Методика петрохимических модулей Петрохимическая специфика толеитового магматизма океанов
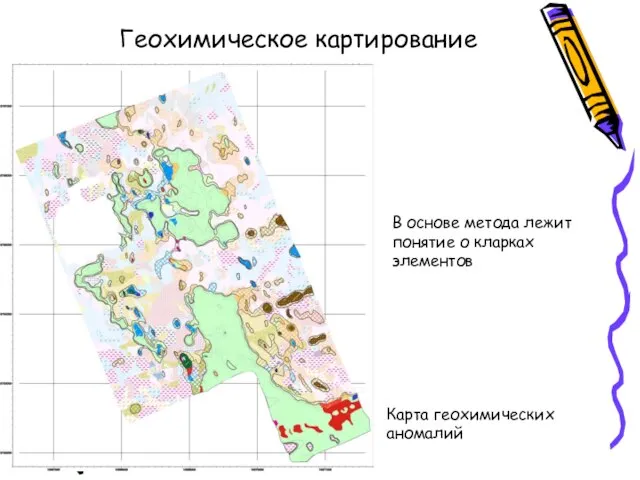
- 11. Геохимическое картирование Карта геохимических аномалий В основе метода лежит понятие о кларках элементов
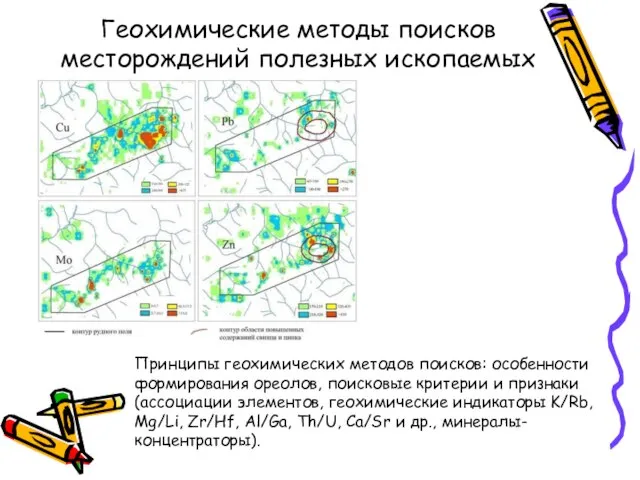
- 12. Геохимические методы поисков месторождений полезных ископаемых Принципы геохимических методов поисков: особенности формирования ореолов, поисковые критерии и
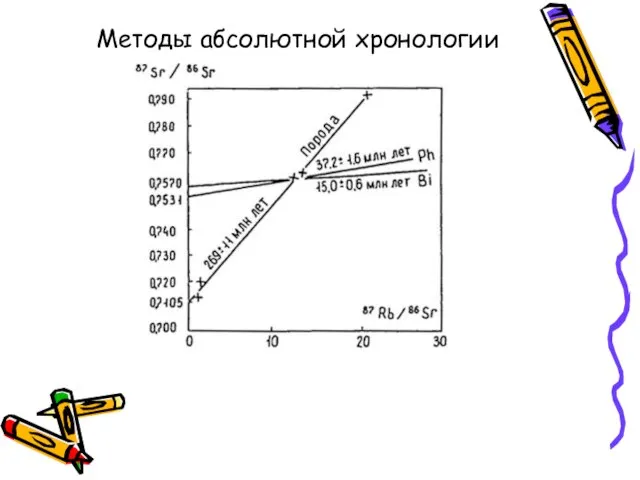
- 13. Методы абсолютной хронологии
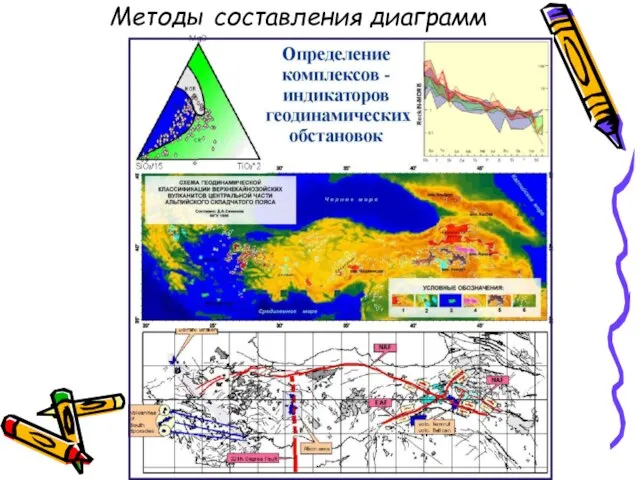
- 14. Методы составления диаграмм
- 15. Александр Евгеньевич Ферсман (1883 - 1945) – Дата рождения:27 октября (8 ноября) 1883) Место рождения:Санкт-Петербург Научная
- 16. 1. Физико-химические исследования процессов формирования минералов, горных пород и руд, земной коры и мантии. Физическая геохимия
- 17. 2. Прикладная геохимия Геохимические методы поисков месторождений полезных ископаемых, геохимические основы металлогении и прогноза, индикаторные свойства
- 18. 3. Геохимия элементов Объектом исследования является конкретный элемент, его поведение и миграция в разных процессах и
- 19. Кристаллохимическое направление Расшифровка структур минералов, изоморфизм, типоморфизм, энергия кристаллических построек. Совершенствование методов и методик исследования: рентгено-структурный
- 20. Химический состав природных геохимических систем Химический элемент — совокупность однотипных атомов, имеющих единый атомный номер в
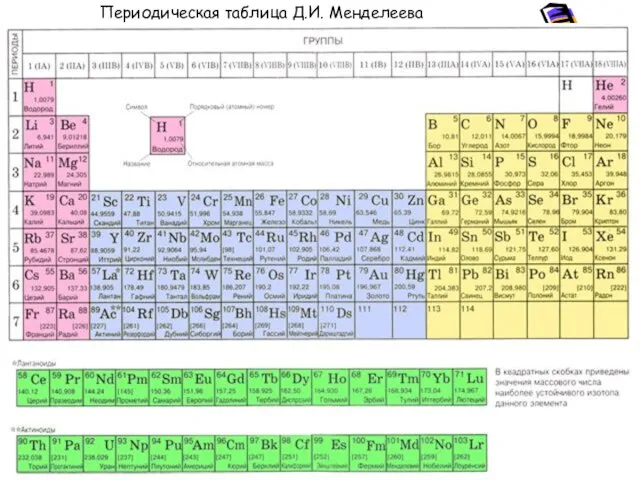
- 21. Периодическая таблица Д.И. Менделеева
- 22. Природные вещества могут состоять как из одного химического элемента (простое веществ), так и из разных (сложное
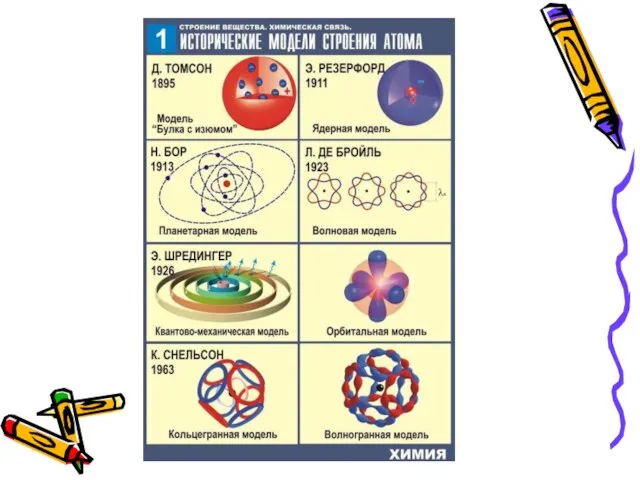
- 23. Атом - это качественно своеобразная сложная материальная микросистема, обладающая индивидуальностью, но изменчивая, способная к превращениям. Элементарные
- 25. «Нуклоны» - это мельчайшие частицы, способных к взаимопревращениям. Атомные ядра состоят из элементарных частиц – протонов
- 26. Строение электронной оболочки Способность атомов вступать в соединения, образовывать минералы определяется свойствами электронов, их энергетическим состоянием,
- 27. Принцип исключения (или запрета) Паули: в атоме не может быть двух электронов с одинаковыми четырьмя квантовыми
- 28. Основные моменты: главное квантовое число n определяет номер периода, который включает ряд элементов, имеющих разное количество
- 29. на внешней (наружной) электронной оболочке, как уже указывалось, может находиться 2n2 электронов, т.е. 2, 8, 18
- 30. Элементы, которые имеют устойчивую 8-электронную оболочку, аналогичную внешнему слою инертных газов, названы элементами типа благородных газов
- 31. элементы, имеющие достроенный до 18 электронов предпоследний слой, называют элементами 18-электронного типа, а в геохимии -
- 32. элементы, у которых не полностью достроена подгруппа (n-1)d предпоследнего слоя подгруппы (n-2)f третьего снаружи слоя (n-2),
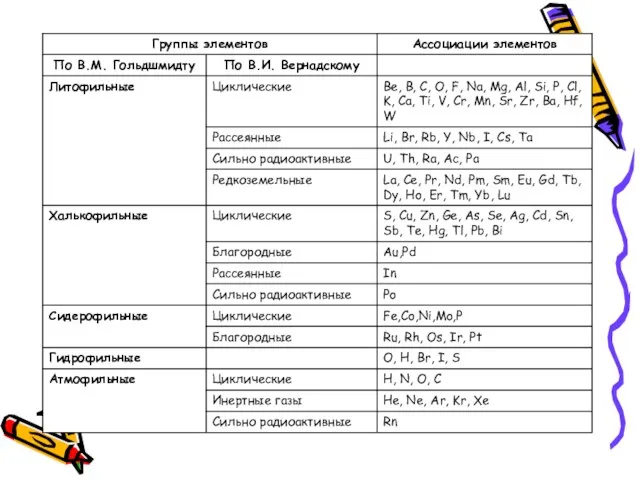
- 33. ГЕОХИМИЧЕСКАЯ КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- 34. Геохимическая классификация В.М. Гольдшмидта Геохимическая классификация В.М. Гольдшмидта учитывает электронное строение атомов, положение элемента на кривой
- 35. Литофильные - это породообразующие элементы, имеющие 2- и 8-электронную достроенную оболочку по типу инертного газа; характеризуются
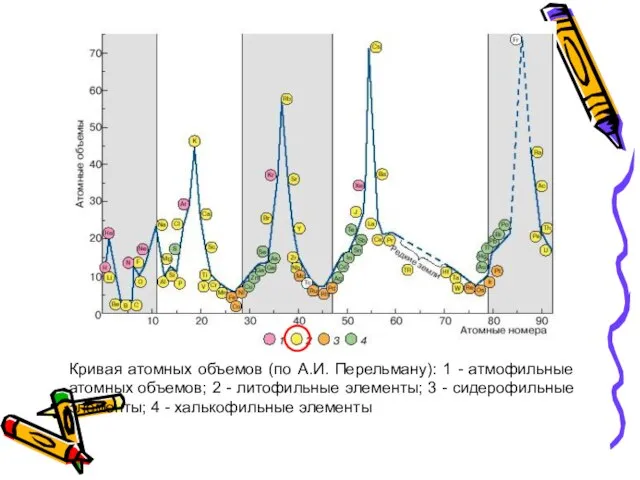
- 36. Кривая атомных объемов (по А.И. Перельману): 1 - атмофильные атомных объемов; 2 - литофильные элементы; 3
- 37. Халькофильные - это элементы 18-электронного типа; характеризуются сродством к сере (к Se, Те-элементам 8-электронного типа), т.е.
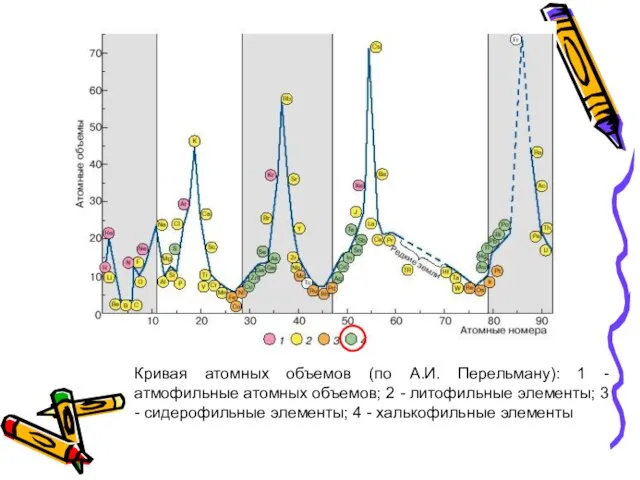
- 38. Кривая атомных объемов (по А.И. Перельману): 1 - атмофильные атомных объемов; 2 - литофильные элементы; 3
- 39. Сидерофильные элементы дают переходные ионы 9 – 17-электронной конфигурации на внешнем слое; обнаруживают сродство как к
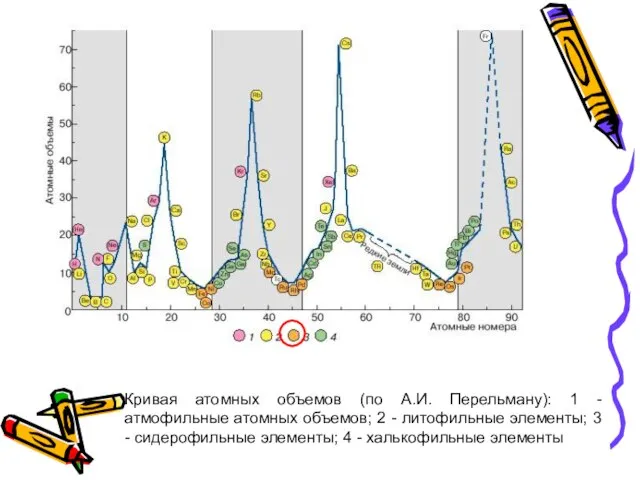
- 40. Кривая атомных объемов (по А.И. Перельману): 1 - атмофильные атомных объемов; 2 - литофильные элементы; 3
- 41. Атмофильные - это элементы, входящие в состав атмосферы: инертные газы (8-электронного типа), N, и Н. На
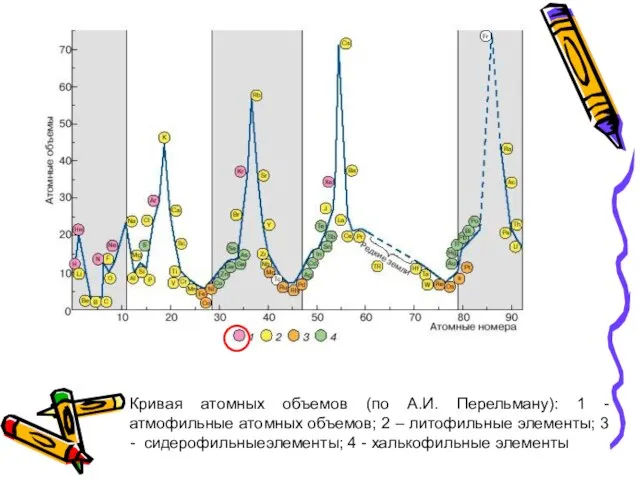
- 42. Кривая атомных объемов (по А.И. Перельману): 1 - атмофильные атомных объемов; 2 – литофильные элементы; 3
- 43. Гидрофильные элементы - это наиболее характерные элементы для гидросферы. Некоторые элементы могут относиться к разным группам,
- 44. В основе классификации В.И. Вернадского лежат геохимические факты: история химических элементов в земной коре, форма нахождения
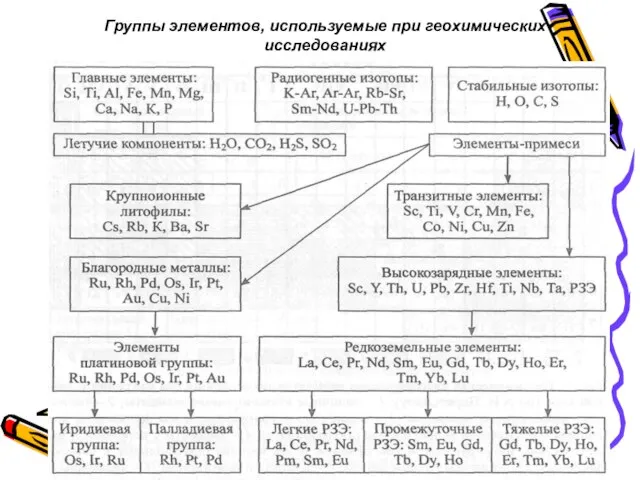
- 46. Группы элементов, используемые при геохимических исследованиях
- 47. Франк Уиглсуорт Кларк 19 марта 1847- 23 мая 1931 Представление о распространенности химических элементов в природе
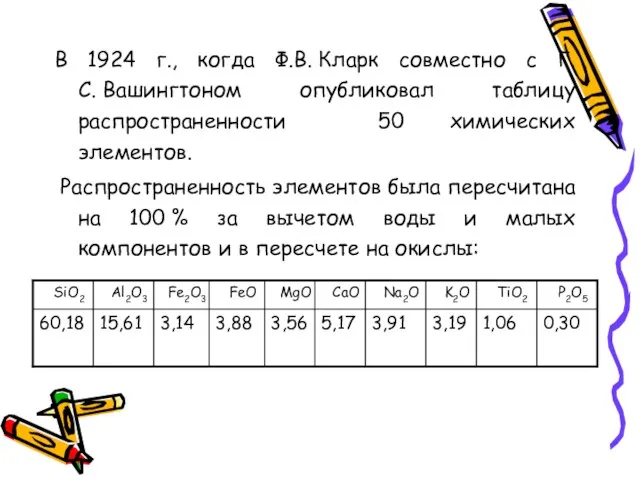
- 48. В 1924 г., когда Ф.В. Кларк совместно с Г.С. Вашингтоном опубликовал таблицу распространенности 50 химических элементов.
- 49. В 1923 г. А.Е. Ферсман предложил термин кларк Кларк – среднее содержание химических элементов в земной
- 50. Закон Кларка-Вернадского - Все элементы есть везде и всюду - Для всех химических элементов характерно повсеместное
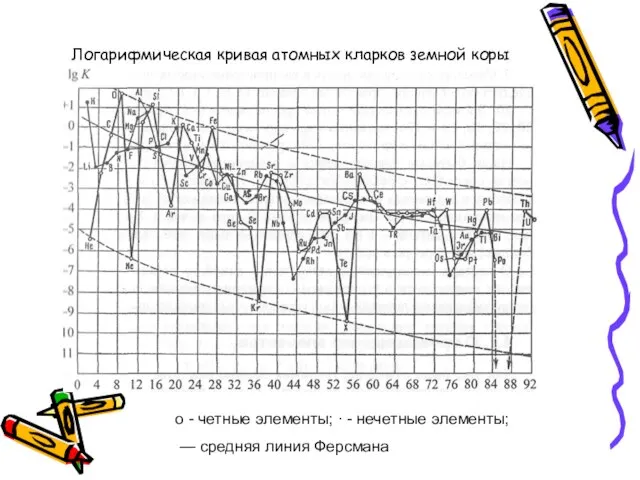
- 51. Общие закономерности распространения элементов на Земле В целом распространенность элементов падает от начала к концу таблицы
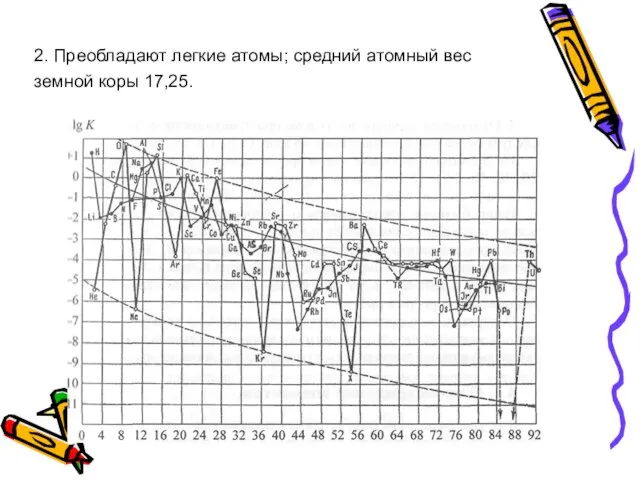
- 52. о - четные элементы; ∙ - нечетные элементы; — средняя линия Ферсмана Логарифмическая кривая атомных кларков
- 53. 2. Преобладают легкие атомы; средний атомный вес земной коры 17,25.
- 54. 3. По весовым кларкам наиболее распространенными элементами земной коры являются следующие (по А.Е. Ферсману): O -
- 55. 4. Кислород - абсолютно преобладающий элемент. 5. После Fe (№ 26) нет ни одного широко распространенного
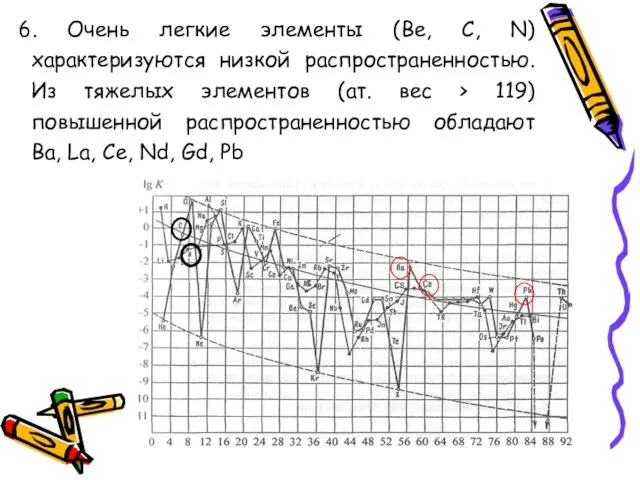
- 56. 6. Очень легкие элементы (Be, С, N) характеризуются низкой распространенностью. Из тяжелых элементов (ат. вес >
- 57. 7. Четные элементы распространены шире нечетных в 5 – 10 раз (закон Оддо–Гаркинса). Для первых по
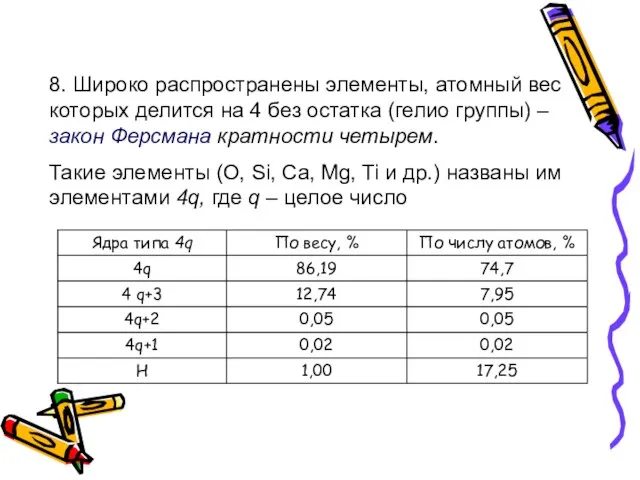
- 58. 8. Широко распространены элементы, атомный вес которых делится на 4 без остатка (гелио группы) – закон
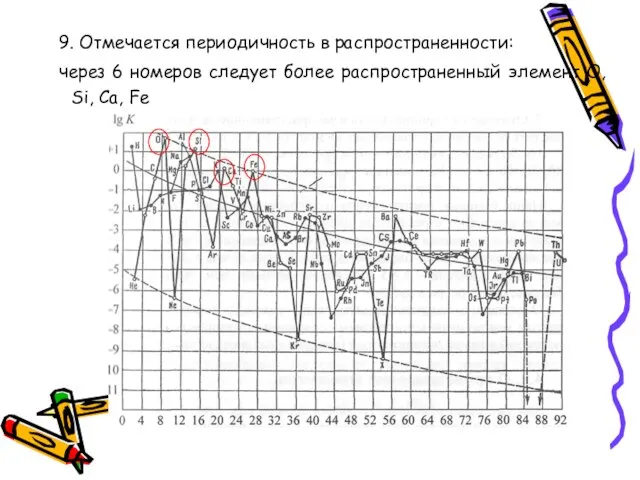
- 59. 9. Отмечается периодичность в распространенности: через 6 номеров следует более распространенный элемент О, Si, Ca, Fe
- 60. 10. Элементы, имеющие числа протонов или нейтронов, равные 2, 8, 20, 28, 50, 82 и 126,
- 61. Основной закон геохимии (В.М. Гольдшмидт) : Содержания химических элементов зависят от строения их атомного ядра, а
- 63. Скачать презентацию








































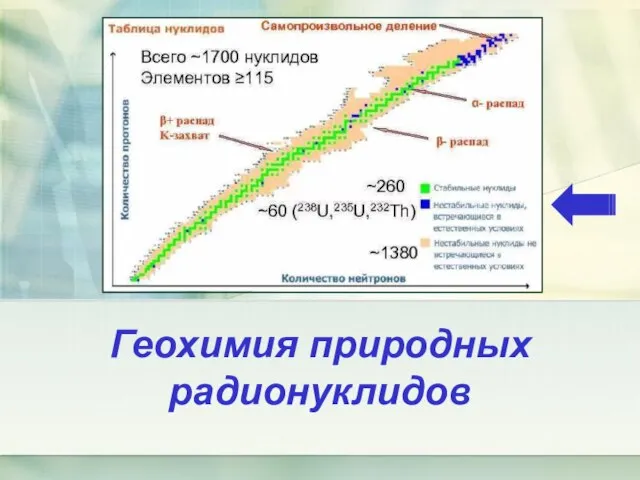 Геохимия природных радионуклидов (тема 1)
Геохимия природных радионуклидов (тема 1) Группа веществ, изолируемых экстракцией органическими растворителями (пестициды или ядохимикаты) (продолжение)
Группа веществ, изолируемых экстракцией органическими растворителями (пестициды или ядохимикаты) (продолжение) Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева
Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева Теория сильных электролитов. Закон действующих масс и его применение к гетерогенным равновесиям
Теория сильных электролитов. Закон действующих масс и его применение к гетерогенным равновесиям Параметры токсичности продуктов горения материала. (Задача 3)
Параметры токсичности продуктов горения материала. (Задача 3) Облик и габитус кристаллов
Облик и габитус кристаллов Иерархия основных классов технологических процессов. Выражение составов фаз
Иерархия основных классов технологических процессов. Выражение составов фаз Презентация по Химии "Типы химических реакций в органической и неорганической химии" - скачать смотреть
Презентация по Химии "Типы химических реакций в органической и неорганической химии" - скачать смотреть  Основные биогеохимические циклы. Цикл углерода
Основные биогеохимические циклы. Цикл углерода Презентация по Химии "Углекислый газ" - скачать смотреть
Презентация по Химии "Углекислый газ" - скачать смотреть  Химический элемент платина
Химический элемент платина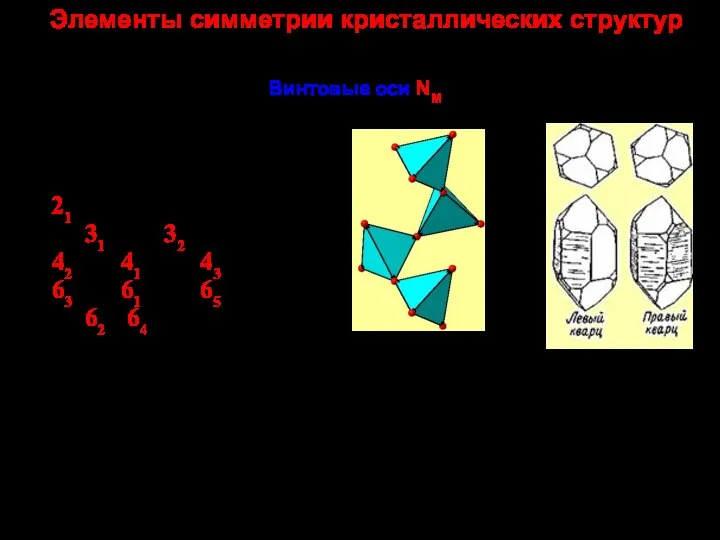 Элементы симметрии кристаллических структур
Элементы симметрии кристаллических структур Происхождение жизни на Земле. Процесс химической эволюции
Происхождение жизни на Земле. Процесс химической эволюции Топлива, применяемые на воздушных судах и наземной технике. Эксплуатационные свойства топлив. (Тема 2.1)
Топлива, применяемые на воздушных судах и наземной технике. Эксплуатационные свойства топлив. (Тема 2.1) Состав, строение, классификация кислот
Состав, строение, классификация кислот Ассортимент и свойства тканей из синтетических волокон (9 класс)
Ассортимент и свойства тканей из синтетических волокон (9 класс) Sources of alkanes and cycloalkanes. Crude oil
Sources of alkanes and cycloalkanes. Crude oil Коррозия металлов
Коррозия металлов Влияние этилового спирта на организм человека
Влияние этилового спирта на организм человека Амиды кислот. Азо- и диазосоединения
Амиды кислот. Азо- и диазосоединения Изучаем химию с Агатой Кристи
Изучаем химию с Агатой Кристи Презентация по Химии "Агрегатное состояние вещества. Плавление и отвердевание кристаллических тел" - скачать смотреть
Презентация по Химии "Агрегатное состояние вещества. Плавление и отвердевание кристаллических тел" - скачать смотреть  Дмитрий Иванович Менделеев
Дмитрий Иванович Менделеев Соединения алифатического ряда
Соединения алифатического ряда Добування кисню та вивчення його властивостей
Добування кисню та вивчення його властивостей Биохимияның зерттеу әдістері
Биохимияның зерттеу әдістері Электрохимические методы анализа: потенциометрия. Потенциометрическое титрование
Электрохимические методы анализа: потенциометрия. Потенциометрическое титрование Аналитическая химия. Количественный анализ (ч.1. титриметрия)
Аналитическая химия. Количественный анализ (ч.1. титриметрия)