Содержание
- 2. Теория окислительно-восстановительных реакций: Реакции, протекающее с изменением степени окисления атомов, входящих в состав реагирующих веществ, называются
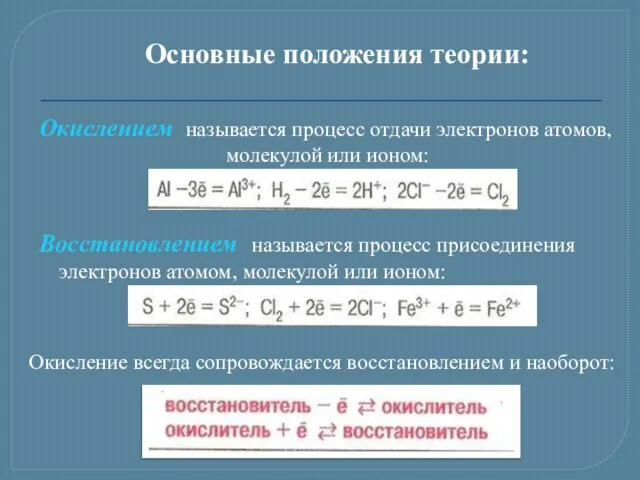
- 3. Основные положения теории: называется процесс отдачи электронов атомов, молекулой или ионом: называется процесс присоединения электронов атомом,
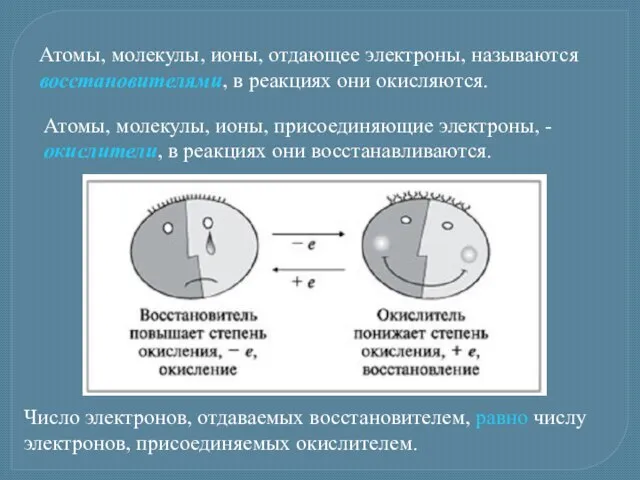
- 4. Атомы, молекулы, ионы, отдающее электроны, называются восстановителями, в реакциях они окисляются. Атомы, молекулы, ионы, присоединяющие электроны,
- 5. Важнейшие восстановители и окислители
- 6. Из истории происхождения окислительно-восстановительных реакций: Издавна ученые полагали, что окисление — это потеря флогистона (особого невидимого
- 7. Составление уравнений окислительно-восстановительных реакций Метод электронного баланса (тв.+тв., тв.+газ) Ионно-электронный метод (в растворах)
- 8. Метод электронного баланса +1 +7 –2 +1 –1 +1 –1 +2 –1 0 +1 –2 KMnO4
- 9. Классификация окислительно-восстановительных реакций Межмолекулярные Внутримолекулярные 2Al+Fe2O3=2Fe+Al2O3 2KClO3=2KCl+3O2 Атомы разных элементов, изменяющие степени окисления, находятся в одной
- 10. МЕЖМОЛЕКУЛЯРНЫЕ +1 +5 –2 0 +1 –1 +5 –2 5 KClO3 + 6P = 5KCl +
- 11. Классификация окислительно-восстановительных реакций РЕАКЦИИ ДИСПРОПОРЦИОНИРОВАНИЯ РЕАКЦИИ КОНПРОПОРЦИОНИРОВАНИЯ 4K2SO3=3K2SO4+K2S Процессы, в результате которых происходит изменение степени окисления
- 12. Диспропорционирование(дисмутация, самоокисление-самовосстановление) +1 +5 –2 Δ +1 –1 +1 +7 –2 4KClO3 = KCl + 3KClO4
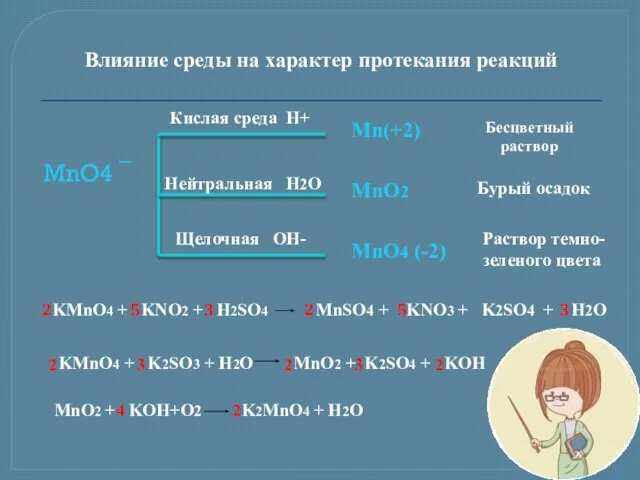
- 13. Влияние среды на характер протекания реакций MnO4 ¯ Кислая среда H+ Нейтральная H2O Щелочная OH- Mn(+2)
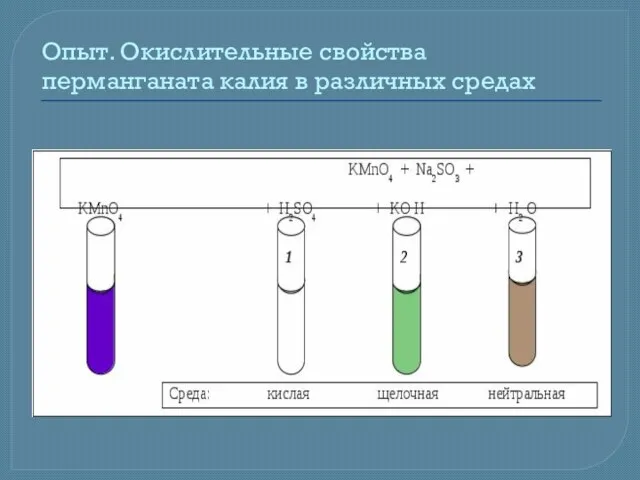
- 14. Опыт. Окислительные свойства перманганата калия в различных средах
- 15. Окислительные свойства перманганата калия в различных средах Расставить коэффициенты в молекулярном уравнении реакции: а) в кислой
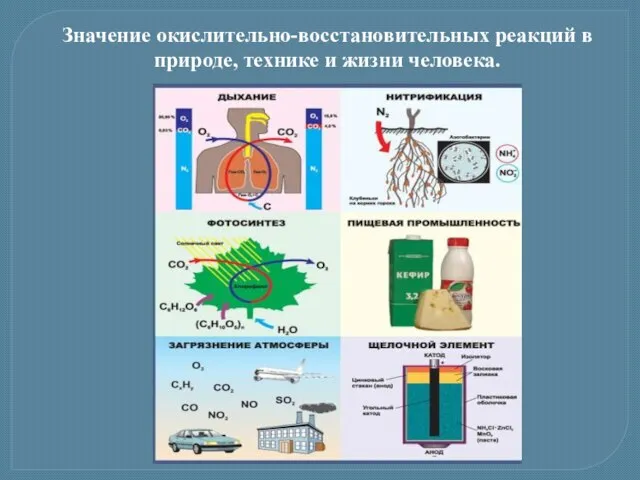
- 16. Значение окислительно-восстановительных реакций в природе, технике и жизни человека.
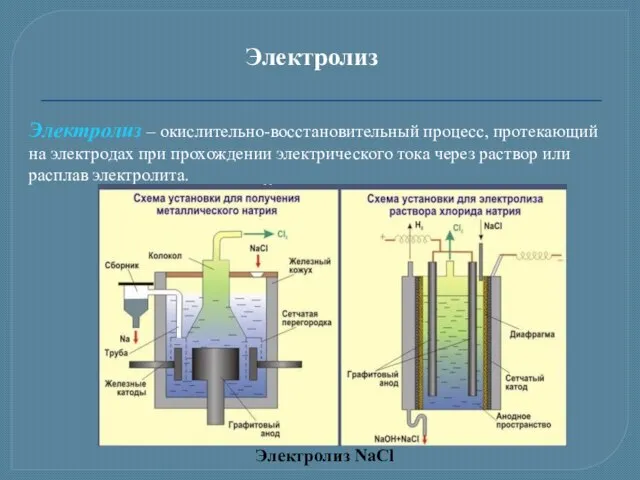
- 17. Электролиз Электролиз – окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через раствор или расплав
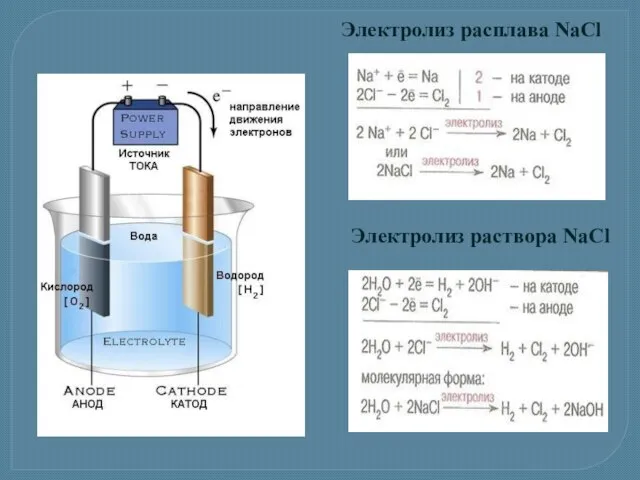
- 18. Электролиз расплава NaCl Электролиз раствора NaCl
- 20. Скачать презентацию










 Ізогіпсичні перетворення функціональних груп. Реакції заміщення та елімінування
Ізогіпсичні перетворення функціональних груп. Реакції заміщення та елімінування Презентация по Химии "Разрешите вам представить - иод" - скачать смотреть
Презентация по Химии "Разрешите вам представить - иод" - скачать смотреть  Строение белков и их значение для организма “Жизнь – форма существования белковых тел.”
Строение белков и их значение для организма “Жизнь – форма существования белковых тел.” Кремний (Silicium). Химические свойства
Кремний (Silicium). Химические свойства Предельные углеводороды
Предельные углеводороды Нефть. Состав и свойства
Нефть. Состав и свойства Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Неорганические полимеры
Неорганические полимеры Атоми і хімічні елементи. Молекули, їх рух. Дифузія
Атоми і хімічні елементи. Молекули, їх рух. Дифузія Понятие об ЭДС Электролиты и неэлектролиты электролитическая диссоциация
Понятие об ЭДС Электролиты и неэлектролиты электролитическая диссоциация Электрофизические и электрохимические методы обработки материалов
Электрофизические и электрохимические методы обработки материалов Представники d-елементів (перехідних елементів) періодичної системи елементів
Представники d-елементів (перехідних елементів) періодичної системи елементів Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения Шкала рН
Шкала рН Кислородосодержащие соединения - спирты
Кислородосодержащие соединения - спирты Твердое тело и его характеристики. Закон Гука. Плавление и кристаллизация. Лекция №26
Твердое тело и его характеристики. Закон Гука. Плавление и кристаллизация. Лекция №26 Методика проведения исследовательской части работы по химии и экологии учитель химии и биологии высшей
Методика проведения исследовательской части работы по химии и экологии учитель химии и биологии высшей Metode cromatografice
Metode cromatografice Типы окисления. Понятие об антиоксидантной системе
Типы окисления. Понятие об антиоксидантной системе  Алкены. Химические свойства этилена
Алкены. Химические свойства этилена Хімічні властивості карбонових кислот
Хімічні властивості карбонових кислот Общий путь катаболизма. (Лекция 9)
Общий путь катаболизма. (Лекция 9) Галогены. История открытия галогенов
Галогены. История открытия галогенов Репликация ДНК и РНК
Репликация ДНК и РНК Горение топлива
Горение топлива Основи прийняття рішень, щодо захисту населення під час різних фаз радіаційної аварії. Критерії для прийняття рішень
Основи прийняття рішень, щодо захисту населення під час різних фаз радіаційної аварії. Критерії для прийняття рішень Общая характеристика неметаллов
Общая характеристика неметаллов Термодинамика и термохимия процессов горения и взрыва
Термодинамика и термохимия процессов горения и взрыва