Содержание
- 2. «─» степень окисления имеют атомы, которые приняли электроны от других атомов или в их сторону смещены
- 3. Правила определения степени окисления самый электроотрицательный элемент, во всех соединениях -1. за исключением гидридов металлов постоянная
- 4. В пероксидах и дисульфидах содержатся двухатомные мостики [-O-O-], [-S-S-] - степени окисления атомов O и S
- 5. Атомы элементов главных подгрупп IV-VI групп могут проявлять несколько степеней окисления. Высшую «+», равную номеру группы
- 6. Атомы металлов могут иметь только «+» степень окисления. Атомы элементов VII группы, главной подгруппы –галогены (кроме
- 7. Окислители и восстановители Окислением называется процесс отдачи электронов, степень окисления атома при этом повышается: Al0 -
- 8. Вещества, атомы которых присоединяют электроны, называются окислителями. В процессе реакции окислители восстанавливаются. Вещества, атомы которых отдают
- 9. Окислителями могут быть: Неметаллы в свободном состоянии; Неметаллы и металлы в высшей степени окисления; Восстановителями могут
- 10. Вещества, в состав которых входит элемент в промежуточной степени окисления, проявляют окислительно – восстановительную двойственность: по
- 11. Классификация ОВР 1. Реакции межмолекулярного и межатомного окисления-восстановления (атомы повышающие и понижающие степень окисления входят в
- 12. 3. Реакции диспропорционирования (повышает и понижает степень окисления атом одного и того же элемента): Cl20 +
- 13. Составление уравнений ОВР методом электронного баланса Пример 1. MnS +HNO3 → MnSO4 + NO + H2O
- 14. 2. Составляют схемы процессов окисления и восстановления. 3. Записывается число отданных и число принятых электронов, для
- 15. 4. Найденные коэффициенты (основные коэффициенты) проставляются в левую часть уравнения (межмолекулярная ОВР), затем уравнивают элементы изменившие
- 16. 6. Для проверки - подсчитывают число атомов кислорода в левой и правой частях уравнения. В левой
- 17. Пример 2. При составлении полуреакций окисления и восстановления следует исходить из общего числа атомов, изменивших степень
- 18. Sn+2 - 2ē → Sn+4 2 6 3 - окисление 2Cr+6 + 2∙3ē → 2Cr+3 6
- 19. 3Sn+2Cl2 + 1K2Cr2+6O7 + 14HCl → 3Sn+4Cl4 + 2Cr+3Cl3 + 2KCl + 7H2O
- 20. Пример 3. Если число атомов, изменивших степень окисления больше 2, то коэффициенты определяют по сумме отданных
- 21. As2+3S3―2 + HCl+5O3 + Н2О → H3As+5O4 +H2S+6O4 + HCl― Степень окисления изменяют 3 атома :
- 22. 2As+3 - 2•2ē → 2 As+5 4 28 84 3 – ок-ие 3S―2 - 3•8ē →
- 23. Если погрузить Ме в водный раствор его соли, то «+» ионы, находящиеся на поверхности металла, гидратируются
- 24. Между металлом и раствором устанавливается равновесие: МТВ + nН2О - z ē ↔ М(Н2О)nz+ Катионы, притягиваясь
- 25. Раствор вблизи поверхности Ме приобретает заряд, противоположный по знаку заряду металла – образуется двойной электрический слой
- 26. Значение электродного потенциала зависит: От природы металла – чем большей химической активностью обладает металл, тем легче
- 27. 2. От концентрации ионов металла в растворе – с увеличением концентрации катионов в растворе потенциал становится
- 28. Уравнение Нернста φ0 – стандартный электродный потенциал металла при стандартных условиях (Т=298 К, [Mez+]=1моль/л) характеризует химическую
- 29. R – универсальная газовая постоянная, R=8,314 Дж/(моль К); Т- абсолютная температура, К; z – число электронов,
- 30. R=8,314 Дж/(моль К) Т = 298 К
- 31. Измерение электродных потенциалов. Стандартный водородный электрод Измерить абсолютную величину электродного потенциала невозможно. Относительные значения измеряют в
- 32. Стандартный водородный электрод Платиновая пластина, покрытая для увеличения поверхности электрода платиновой чернью, и погруженная в водный
- 33. Часть поглощенного платиной водорода переходит в атомарное состояние и в поверхностном слое платины устанавливается равновесие: Н2
- 34. Водородный электрод ведет себя подобно металлу, погруженному в раствор своей соли. Металлическая платина выполняет роль носителя
- 35. Не стандартные условия: φ 2Н+/Н2 = 0,059 lg[H+] = -0,059рН
- 36. Электрохимический ряд напряжений металлов По отношению к стандартному водородному электроду выражают потенциалы всех других электродов -
- 37. Расположив все металлы в порядке возрастания значений стандартных электродных потенциалов получают электрохимический ряд напряжений металлов:
- 38. Положение металла в Ряду характеризует его способность к окислительно - восстановительному взаимодействию в водных растворах при
- 39. Восстановительная активность катионов металлов возрастает слева направо; Каждый металл вытесняет из растворов солей все другие металлы,
- 40. Металлы, стоящие в Ряду от Mg до Н, вытесняют водород из разбавленных растворов кислот (за исключением
- 41. Гальванические элементы ОВР связаны с переносом электронов, поэтому их можно использовать для получения электрического тока. Приборы,
- 42. ХИЭЭ: Гальванические элементы; Аккумуляторы; Топливные элементы. ГЭ – система, в которой происходит самопроизвольная ОВР (ΔG
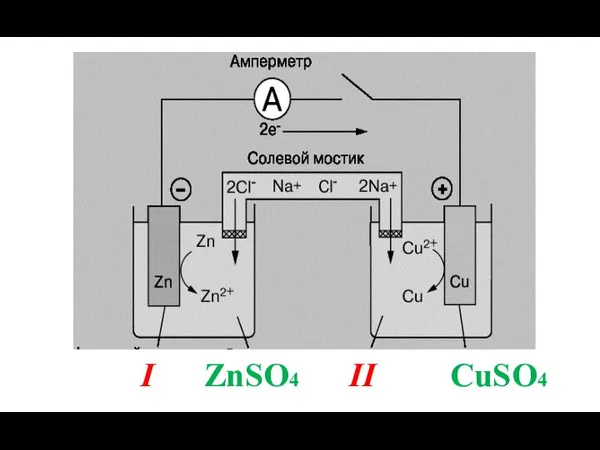
- 43. ГЭ - электрохимическая система, из 2 электродов, растворы которых между собой соединены с помощью солевого мостика
- 44. I ZnSO4 II CuSO4
- 45. Медно-цинковый гальванический элемент (элемент Якоби-Даниэля) Если электрическая цепь замкнута, то в области I происходит окисление цинка,
- 46. Электрод, на котором протекает процесс окисления, называется анодом. Zn0 ↔ Zn+2 + 2ē – анодный процесс
- 47. В области II, на медном электроде, происходит восстановление ионов меди. Электроны, переходящие по внешней цепи от
- 48. Электрод, на котором протекают процессы восстановления, называется катодом. Cu+2 + 2ē ↔ Cu0 – катодный процесс
- 49. Суммарное уравнение токообразующей реакции: Cu+2 + Zn0 ↔ Cu0 + Zn+2 CuSO4 + Zn0 ↔ Cu0
- 50. При работе ГЭ область II обедняется катионами меди, область I обогащается катионами цинка. Раствор в области
- 51. При схематической записи ГЭ вертикальными линиями разделяют те фазы, на границе раздела которых возникают скачки потенциалов,
- 52. Максимальное значение напряжения ГЭ, соответствующее обратимому проведению процесса, называется электродвижущей силой (ЭДС) гальванического элемента (Е, В).
- 53. Если соблюдаются стандартные условия, ЭДС элемента называется стандартной (Е0, В): Е0= φ0(катода) – φ0(анода)
- 54. Электролиз Электролиз - окислительно-восстановительные процессы, которые протекают под действием постоянного электрического тока, проходящего через раствор или
- 55. Электролиз расплава хлорида магния MgCl2↔ Mg2+ + 2Cl— «-« Катод: Mg2+ + 2ē → Mg0 «+»
- 56. Электрод, на котором происходит восстановление, называется катодом, но в электролизе он заряжен «-». Электрод, на котором
- 57. Электролиз водных растворов электролитов На катоде будут восстанавливаться окисленные формы тех систем, которые имеют наибольшее значение
- 58. Катодные процессы При рассмотрении этих процессов необходимо учитывать потенциал процесса восстановления водорода 2Н+ + 2ē →
- 59. Металлы, стоящие в ряду напряжений до Al (Ti) включительно не восстанавливаются при электролизе водных растворов, т.к.
- 60. Металлы, стоящие в Ряду от Sn до конца , имеют φ0 > - 0,41В, и из
- 61. Анодные процессы Различают электролиз с активным (растворимым) и электролиз с инертным (материал, которого не претерпевает изменений
- 62. Анионы образуют собственный ряд напряжений, в котором слева направо увеличивается значение стандартного электродного потенциала: Cl— S—2
- 63. При электролизе водных растворов щелочей, кислородсодержащих кислот и их солей, фтороводорода и фторидов происходит электрохимическое выделение
- 64. При электролизе водных растворов безкислородных кислот и их солей у анода будут разряжаться анионы этих кислот.
- 65. Электролиз раствора CuCl2 с инертным анодом Катод «-» 1) Cu2+ + 2ē → Cu0 ; φ01=0,34В
- 66. Суммарное уравнение электролиза: CuCl2 + Н2О → Cu0 + Cl20 + Н2О
- 67. Электролиз раствора CuCl2 с медным анодом Катод «-» 1) Cu2+ + 2ē → Cu0 ; φ01=0,34В
- 68. Анод (Cu) «+» 1)2Cl— - 2ē→ Cl20 ; φ01 2)2Н2О - 4ē → О2 + 4Н+;
- 69. Суммарное уравнение электролиза: Cu0 + CuCl2+ Н2О →Cu0 + CuCl2+ Н2О Электролиз сводится к переносу меди
- 70. Законы электролиза С количественной стороны процесс электролиза был впервые изучен в 30-х гг. 19 века английским
- 71. Первый закон Фарадея: Масса вещества, выделившегося при электролизе, пропорциональна количеству электричества, прошедшего через электролит.
- 72. Второй закон Фарадея: Одинаковые количества электричества выделяют на электродах эквивалентные массы различных веществ. Для выделения на
- 73. МЭ – эквивалентная масса, г/моль; I - сила тока, А; t – время проведения процесса, с;
- 74. 1 F = 96500 Кл = 96500 А•с= 26,8 А•час 1Фарадей – это заряд, который несет
- 75. Количественной характеристикой полноты использования тока является выход по току (η):
- 76. Применение электролиза Получение металлов – выделение в чистом виде алюминия и щелочных, щелочноземельных металлов производится электролизом
- 77. Очистка металлов – электролиз проводят с активным (растворимым) анодом. Получение различных химических веществ Зарядка аккумулятора –
- 78. Получение металлических покрытий – в декоративных целях, для защиты от коррозии, повышения твердости и электропроводности производят
- 79. Защита от коррозии – защита основана на электролизе, при котором защищаемый объект играет роль катода, на
- 80. Коррозия металлов Коррозия - разрушение металлов под воздействием окружающей среды. Коррозия металлов - процесс окисления: Ме
- 81. По механизму коррозия делится на химическую и электрохимическую. Химическая коррозия – разрушение металлов в результате химического
- 82. Химическая коррозия делится: газовая (протекает при высоких температурах на воздухе, в присутствии газов-галогенов); коррозия в агрессивных
- 83. При нагревании стальных изделий на воздухе их поверхность покрывается темным слоем окалины – продуктов окисления (оксида
- 84. Пример: Предметы из меди и ее сплавов при длительном хранении покрываются зеленым налетом основной соли: 2Cu
- 85. Скорость химической коррозии зависит от свойств пленки и окислителя, и температуры. Сплошную оксидную пленку, предотвращающую дальнейшую
- 86. Электрохимическая коррозия – разрушение металла под действием окружающей среды в результате возникновения гальванических пар. Характерна для
- 87. Чаще всего причиной электрохимической коррозии является вода и растворенный в ней кислород, электродный потенциал этой системы
- 88. Закономерности электрохимической коррозии: разрушается более активный металл; в кислой среде на поверхности менее активного металла выделяется
- 89. Используемые в технике металлы, как правило, химически неоднородны, содержат примеси других металлов. Это является причиной возникновения
- 90. Пример: коррозии железа в контакте с медью в кислой среде. Образуется ГЭ: (-) Fe | HCl
- 91. Пример: коррозия (ржавление) железа в нейтральной среде Анод: Fe - 2ē → Fe2+ Катод: О2 +
- 92. Методы защиты от коррозии: Окраска металлических изделий, покрытие полимерными пленками (полиэфирными, эпоксидными); Оксидирование – получение на
- 93. Нанесение металлических покрытий – катодные покрытия - покрытие менее активным металлом, для железа используют покрытия оловом,
- 94. Протекторная защита – для защиты подземных трубопроводов, паровых котлов, корпусов кораблей – на некотором расстоянии от
- 96. Скачать презентацию


![В пероксидах и дисульфидах содержатся двухатомные мостики [-O-O-], [-S-S-] - степени](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394594/slide-3.jpg)














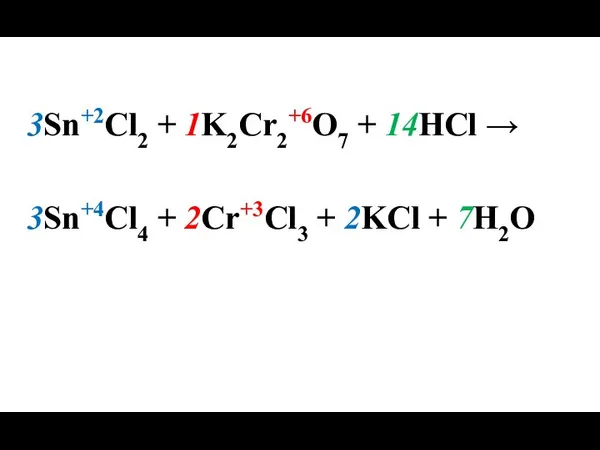















![Не стандартные условия: φ 2Н+/Н2 = 0,059 lg[H+] = -0,059рН](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394594/slide-34.jpg)


























































 Ізогіпсичні перетворення функціональних груп. Реакції заміщення та елімінування
Ізогіпсичні перетворення функціональних груп. Реакції заміщення та елімінування Презентация по Химии "Разрешите вам представить - иод" - скачать смотреть
Презентация по Химии "Разрешите вам представить - иод" - скачать смотреть  Строение белков и их значение для организма “Жизнь – форма существования белковых тел.”
Строение белков и их значение для организма “Жизнь – форма существования белковых тел.” Кремний (Silicium). Химические свойства
Кремний (Silicium). Химические свойства Предельные углеводороды
Предельные углеводороды Нефть. Состав и свойства
Нефть. Состав и свойства Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Неорганические полимеры
Неорганические полимеры Атоми і хімічні елементи. Молекули, їх рух. Дифузія
Атоми і хімічні елементи. Молекули, їх рух. Дифузія Понятие об ЭДС Электролиты и неэлектролиты электролитическая диссоциация
Понятие об ЭДС Электролиты и неэлектролиты электролитическая диссоциация Электрофизические и электрохимические методы обработки материалов
Электрофизические и электрохимические методы обработки материалов Представники d-елементів (перехідних елементів) періодичної системи елементів
Представники d-елементів (перехідних елементів) періодичної системи елементів Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения Шкала рН
Шкала рН Кислородосодержащие соединения - спирты
Кислородосодержащие соединения - спирты Твердое тело и его характеристики. Закон Гука. Плавление и кристаллизация. Лекция №26
Твердое тело и его характеристики. Закон Гука. Плавление и кристаллизация. Лекция №26 Методика проведения исследовательской части работы по химии и экологии учитель химии и биологии высшей
Методика проведения исследовательской части работы по химии и экологии учитель химии и биологии высшей Metode cromatografice
Metode cromatografice Типы окисления. Понятие об антиоксидантной системе
Типы окисления. Понятие об антиоксидантной системе  Алкены. Химические свойства этилена
Алкены. Химические свойства этилена Хімічні властивості карбонових кислот
Хімічні властивості карбонових кислот Общий путь катаболизма. (Лекция 9)
Общий путь катаболизма. (Лекция 9) Галогены. История открытия галогенов
Галогены. История открытия галогенов Репликация ДНК и РНК
Репликация ДНК и РНК Горение топлива
Горение топлива Основи прийняття рішень, щодо захисту населення під час різних фаз радіаційної аварії. Критерії для прийняття рішень
Основи прийняття рішень, щодо захисту населення під час різних фаз радіаційної аварії. Критерії для прийняття рішень Общая характеристика неметаллов
Общая характеристика неметаллов Термодинамика и термохимия процессов горения и взрыва
Термодинамика и термохимия процессов горения и взрыва