Содержание
- 2. План лекции Оптические свойства коллоидных растворов Строение коллоидной частицы Условия получения коллоидных растворов Электрокинетические явления
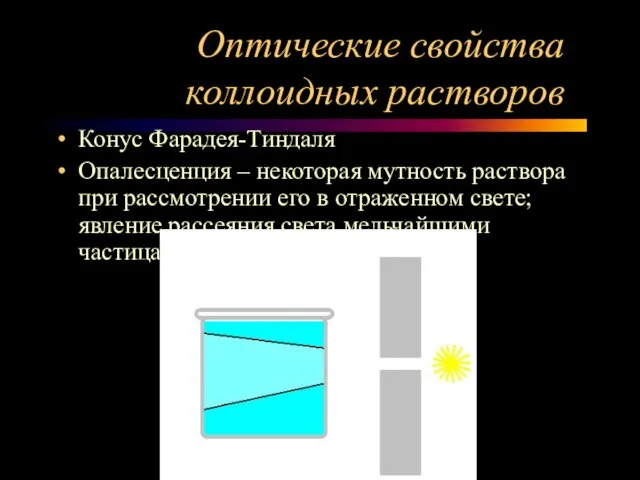
- 3. Оптические свойства коллоидных растворов Конус Фарадея-Тиндаля Опалесценция – некоторая мутность раствора при рассмотрении его в отраженном
- 4. Дихроизм Зависит: От природы вещества (поглощение света) От степени дисперсности Окраска драгоценных камней (рубинов, изумрудов, сапфиров)
- 5. Интенсивность рассеянного света I Закон Релея С · V2 I = I0 · K--------- λ4 I0
- 6. Значение волны видимого света Цвет сигнальных огней Цвет моря Цвет неба К О Ж З Г
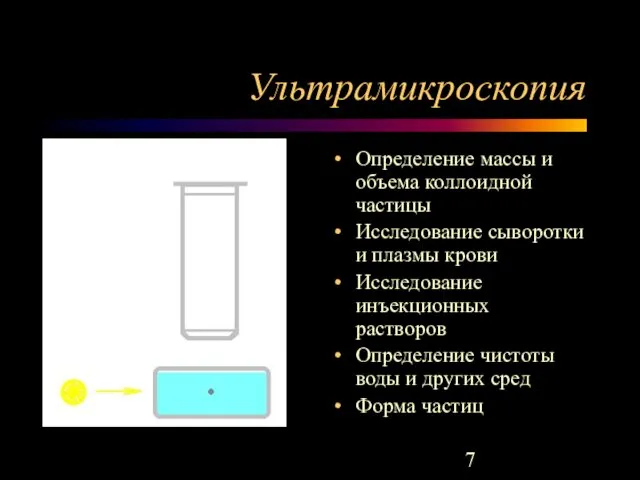
- 7. Ультрамикроскопия Определение массы и объема коллоидной частицы Исследование сыворотки и плазмы крови Исследование инъекционных растворов Определение
- 8. Строение коллоидной частицы Внутренняя нейтральная часть, содержащая большую часть массы частицы Внешний ионный слой (оболочка), в
- 9. Получение коллоидного раствора реакцией осаждения KJ + AgNO3 = AgJ↓ + KNO3 избыток Молекулы AgJ объединяются
- 10. Противоионы – ионы противоположного знака (К+). Их адсорбируется меньше, чем потенциалопределяющих Потенциалопределяющие ионы + большая часть
- 11. Агрегат + адсорбционный слой – гранула (имеет заряд) Гранула + диффузный слой – мицелла (электронейтральна) Электрокинетический
- 12. Строение коллоидной частицы Можно изображать мицеллярными формулами
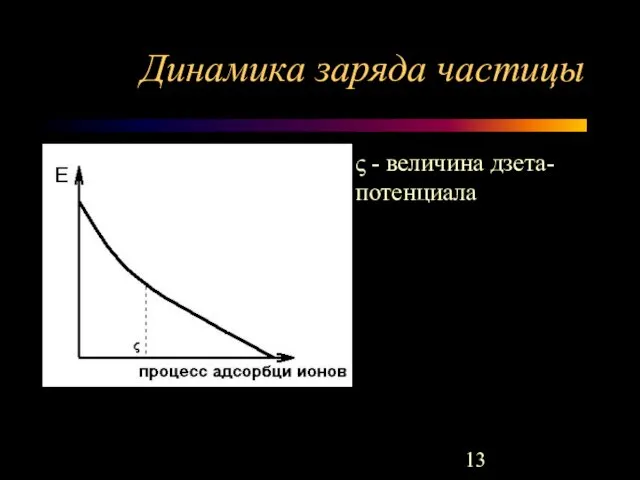
- 13. Динамика заряда частицы ς - величина дзета-потенциала
- 14. На величину ς-потенциала влияют Добавление к коллоидному раствору электролитов (сжимают диффузный слой, часть ионов из него
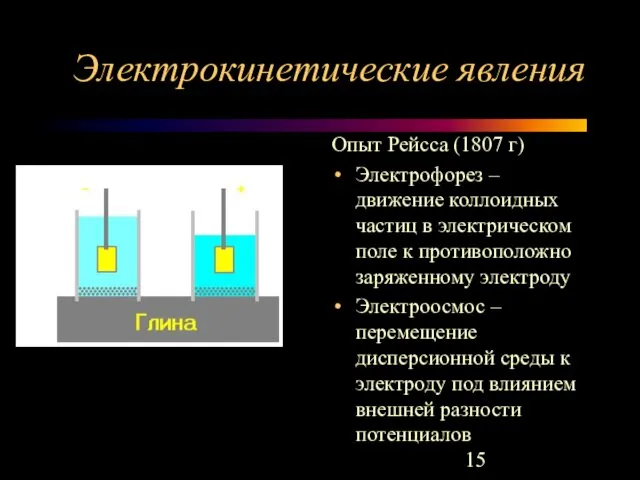
- 15. Электрокинетические явления Опыт Рейсса (1807 г) Электрофорез – движение коллоидных частиц в электрическом поле к противоположно
- 16. Применение электрофореза и электроосмоса В технике и различных производствах: Фарфоровое дело Очистка воздуха Покрытие изделий защитными
- 17. Уравнение Гельмгольца-Смолуховского Расчет скорости движения коллоидных частиц в электрическом поле (U): Нeς U = ---------- 4πη
- 18. Обратные электрокинетические явления Смещение заряженной частицы по отношения к дисперсионной среде вызывает потенциал оседания (эффект Дорна)
- 20. Скачать презентацию













 Презентация по Химии "Органические вещества: Классификация" - скачать смотреть
Презентация по Химии "Органические вещества: Классификация" - скачать смотреть  Топливо и его свойства
Топливо и его свойства Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов.
Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов. Нефть. Общие сведения
Нефть. Общие сведения Средства для борьбы с насекомыми
Средства для борьбы с насекомыми Мінеральні добрива
Мінеральні добрива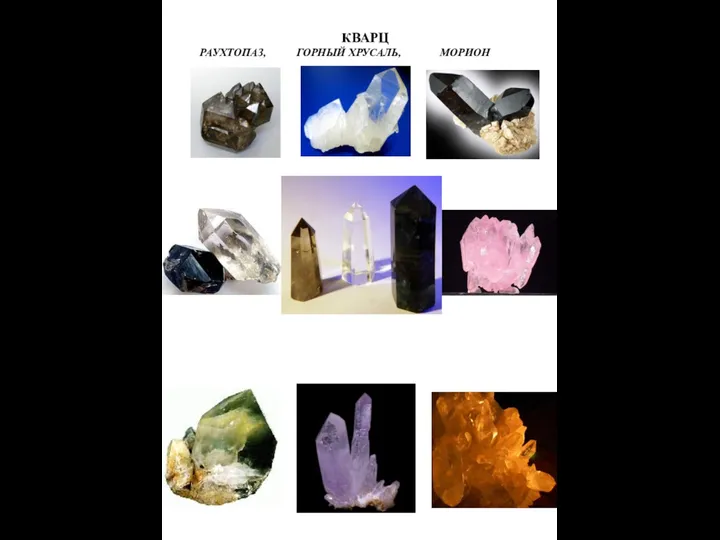 Кварц
Кварц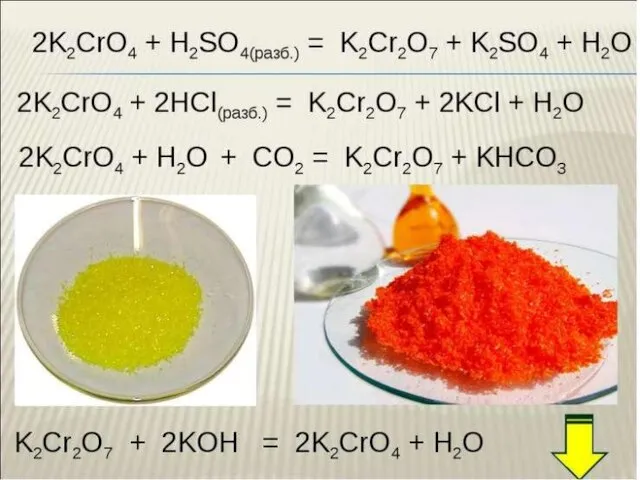 Хром. Соединения хрома
Хром. Соединения хрома Презентация Принципы гормональной и нейромедиаторной регуляции
Презентация Принципы гормональной и нейромедиаторной регуляции  Классификация минералов + самородные элементы. Занятие 5
Классификация минералов + самородные элементы. Занятие 5 Карбоновые кислоты
Карбоновые кислоты Эколого-биохимическая характеристика почв и подорожника большого (Plantago Major) из районов г. Самары
Эколого-биохимическая характеристика почв и подорожника большого (Plantago Major) из районов г. Самары Синтез ультрадисперсного мела для различных эффективных использований
Синтез ультрадисперсного мела для различных эффективных использований Презентация по Химии "Белки" - скачать смотреть бесплатно_
Презентация по Химии "Белки" - скачать смотреть бесплатно_ Презентация по Химии "М.В. Ломоносов и химия" - скачать смотреть
Презентация по Химии "М.В. Ломоносов и химия" - скачать смотреть  Соляная кислота и её соли
Соляная кислота и её соли Презентация по Химии "Межпредметные связи химии" - скачать смотреть
Презентация по Химии "Межпредметные связи химии" - скачать смотреть  Використання кислот в будівництві і побуті. 8 клас
Використання кислот в будівництві і побуті. 8 клас Этиленовые, олефины, непредельные алкены
Этиленовые, олефины, непредельные алкены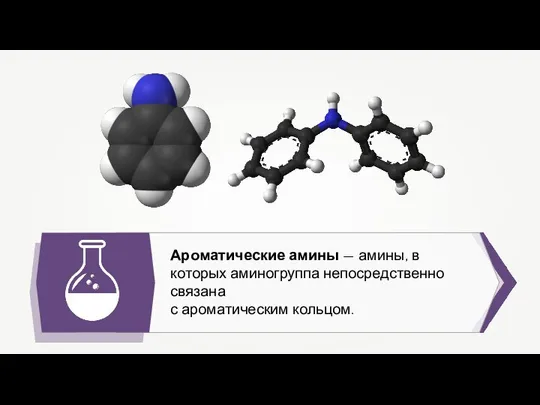 Ароматические амины
Ароматические амины Презентация по Химии "Металлическая связь" - скачать смотреть
Презентация по Химии "Металлическая связь" - скачать смотреть  Масла автомобильные
Масла автомобильные Сплав Вуда
Сплав Вуда Топливо и топливосжигающие устройства
Топливо и топливосжигающие устройства Изучение геохимических свойств редкоземельных элементов
Изучение геохимических свойств редкоземельных элементов Презентация по Химии "МАССОВАЯ ДОЛЯ ВЕЩЕСТВА В РАСТВОРЕ" - скачать смотреть бесплатно
Презентация по Химии "МАССОВАЯ ДОЛЯ ВЕЩЕСТВА В РАСТВОРЕ" - скачать смотреть бесплатно Презентация по Химии "Алкены" - скачать смотреть бесплатно__
Презентация по Химии "Алкены" - скачать смотреть бесплатно__ Основные физико-химические процессы очистки воды. Опыт исследования коагулянтов и флокулянтов
Основные физико-химические процессы очистки воды. Опыт исследования коагулянтов и флокулянтов