Содержание
- 2. История: Мало кому известно, что химическое соединение со сложной формулой NH4OH под названием гидроксид аммония выступает
- 3. Физические свойства: Бесцветный газ с резким запахом аммиак NH3 не только хорошо растворяется в воде с
- 4. Химические свойства: Реакции с изменением степени окисления атома азота (реакции окисления) N-3 → N0 → N+2
- 5. Получение: Для получения аммиака в лаборатории используют действие сильных щелочей на соли аммония: NH4Cl + NaOH
- 7. Скачать презентацию
Слайд 2
История:
Мало кому известно, что химическое соединение со сложной формулой NH4OH под
История:
Мало кому известно, что химическое соединение со сложной формулой NH4OH под
названием гидроксид аммония выступает в нашей обыденной жизни под многими ипостасями. Это и удобрение для картошки и свеклы, это и нашатырный спирт, это и пищевая добавка, скрывающаяся в фабричных продуктах питания под таинственным псевдонимом Е527, и даже… антифриз. Для химической промышленности раствор этого химического соединения добывают синтетическим образом. И сырьем для него служит обычный каменный уголь. В коксовых печах уголь выделяет аммиак, которым и насыщают воду в различных пропорциях
Слайд 3
Физические свойства:
Бесцветный газ с резким запахом аммиак NH3 не только хорошо
Физические свойства:
Бесцветный газ с резким запахом аммиак NH3 не только хорошо
растворяется в воде с выделением тепла. Вещество активно взаимодействует с молекулами H2O с образованием слабой щелочи. Раствор получил несколько названий, одно из них — аммиачная вода. Соединение обладает удивительными свойствами, которые заключаются в способе образования, составе и химических реакциях.
Слайд 4
Химические свойства:
Реакции с изменением степени окисления атома азота (реакции окисления)
N-3 →
Химические свойства:
Реакции с изменением степени окисления атома азота (реакции окисления)
N-3 →
N0 → N+2
NH3 – сильный восстановитель.
с кислородом
1. Горение аммиака (при нагревании)
4NH3 + 3O2 → 2N2 + 6H20
2. Каталитическое окисление амииака (катализатор Pt – Rh, температура)
4NH3 + 5O2 → 4NO + 6H2O
Видео - Эксперимент " Окисление аммиака в присутствии оксида хрома" с оксидами металлов
2 NH3 + 3CuO = 3Cu + N2 + 3 H2O
с сильными окислителями
2NH3 + 3Cl2 = N2 + 6HCl (при нагревании)
аммиак – непрочное соединение, при нагревании разлагается
2NH3↔ N2 + 3H2
NH3 – сильный восстановитель.
с кислородом
1. Горение аммиака (при нагревании)
4NH3 + 3O2 → 2N2 + 6H20
2. Каталитическое окисление амииака (катализатор Pt – Rh, температура)
4NH3 + 5O2 → 4NO + 6H2O
Видео - Эксперимент " Окисление аммиака в присутствии оксида хрома" с оксидами металлов
2 NH3 + 3CuO = 3Cu + N2 + 3 H2O
с сильными окислителями
2NH3 + 3Cl2 = N2 + 6HCl (при нагревании)
аммиак – непрочное соединение, при нагревании разлагается
2NH3↔ N2 + 3H2
Слайд 5
Получение:
Для получения аммиака в лаборатории используют действие сильных щелочей на соли
Получение:
Для получения аммиака в лаборатории используют действие сильных щелочей на соли
аммония:
NH4Cl + NaOH = NH3↑ + NaCl + H2O
(NH4)2SO4 + Ca(OH)2 = 2NH3↑ + CaSO4 + 2H2O
Внимание! Гидроксид аммония неустойчивое основание, разлагается: NH4OH ↔ NH3↑ + H2O
При получении аммиака держите пробирку - приёмник дном кверху, так как аммиак легче воздуха:
NH4Cl + NaOH = NH3↑ + NaCl + H2O
(NH4)2SO4 + Ca(OH)2 = 2NH3↑ + CaSO4 + 2H2O
Внимание! Гидроксид аммония неустойчивое основание, разлагается: NH4OH ↔ NH3↑ + H2O
При получении аммиака держите пробирку - приёмник дном кверху, так как аммиак легче воздуха:
Промышленный способ получения аммиака основан на прямом взаимодействии водорода и азота:
N2(г) + 3H2(г) ↔ 2NH3(г) + 45,9 кДж
Условия:
катализатор – пористое железо
температура – 450 – 500 ˚С
давление – 25 – 30 МПа
Это так называемый процесс Габера (немецкий физик, разработал физико-химические основы метода).
- Предыдущая
Сплав золота и серебра - электрумСледующая -
Кислоты. Серная кислота-H₂SO₄



 Фотоэлектрические и информационные свойства фоточувствительных карбазолилсодержащих олигомерных пленочных композитов
Фотоэлектрические и информационные свойства фоточувствительных карбазолилсодержащих олигомерных пленочных композитов Диеновые углеводороды (алкадиены)
Диеновые углеводороды (алкадиены) Правила оформления лабораторных работ
Правила оформления лабораторных работ Фосфонсірке қыщқылының антипирендік қасиеттерін зерттеу
Фосфонсірке қыщқылының антипирендік қасиеттерін зерттеу Фосфор. Элемент жизни и мысли
Фосфор. Элемент жизни и мысли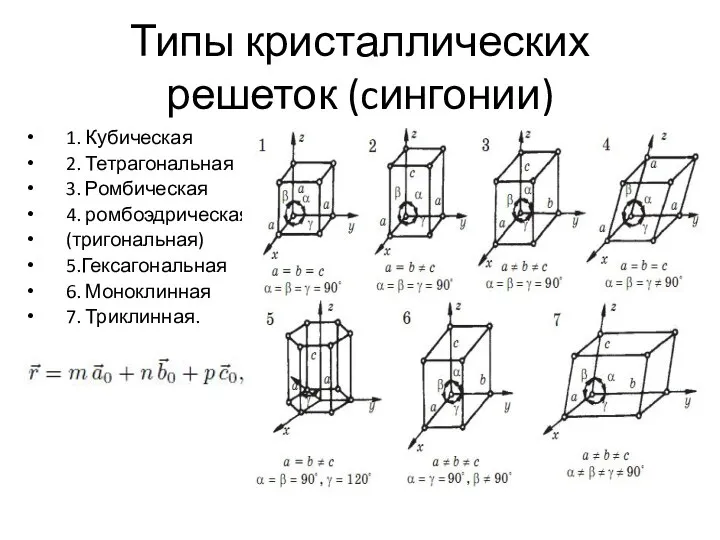 Типы кристаллических решеток, cингонии. (Лекция 2)
Типы кристаллических решеток, cингонии. (Лекция 2) Химическая промышленность Беларуси
Химическая промышленность Беларуси Взаимодействие кислоты с основанием (реакция нейтрализации)
Взаимодействие кислоты с основанием (реакция нейтрализации) Конструкционные материалы
Конструкционные материалы Химическая викторина Оксиды
Химическая викторина Оксиды Оксиды азота (II и IV). Азотная кислота. Строение молекулы
Оксиды азота (II и IV). Азотная кислота. Строение молекулы Мое любимое химическое вещество: Серебро
Мое любимое химическое вещество: Серебро Структурный тип
Структурный тип Доказательство амфотерности аминокислот. Продукты, содержащие аминокислоты и их соли
Доказательство амфотерности аминокислот. Продукты, содержащие аминокислоты и их соли Минеральные вещества. Микроэлементы и макроэлементы
Минеральные вещества. Микроэлементы и макроэлементы М.В.Ломоносов- великий сын России Презентацию подготовила учитель химии МОУ «Куженерская средняя общеобразовательная школа №
М.В.Ломоносов- великий сын России Презентацию подготовила учитель химии МОУ «Куженерская средняя общеобразовательная школа № . Зонная модель электронной проводимости металлов С точки зрения электропроводности все вещества могут быть разделены на металлы (61036105)Ом-1 см-1, полупроводники = 102109 Ом1· см1 и диэлектрики 10101022 Ом1· см1. Качественное ра
. Зонная модель электронной проводимости металлов С точки зрения электропроводности все вещества могут быть разделены на металлы (61036105)Ом-1 см-1, полупроводники = 102109 Ом1· см1 и диэлектрики 10101022 Ом1· см1. Качественное ра Химия и здоровье
Химия и здоровье Материаловедение и методы диагностики микро- и наноструктурных материалов
Материаловедение и методы диагностики микро- и наноструктурных материалов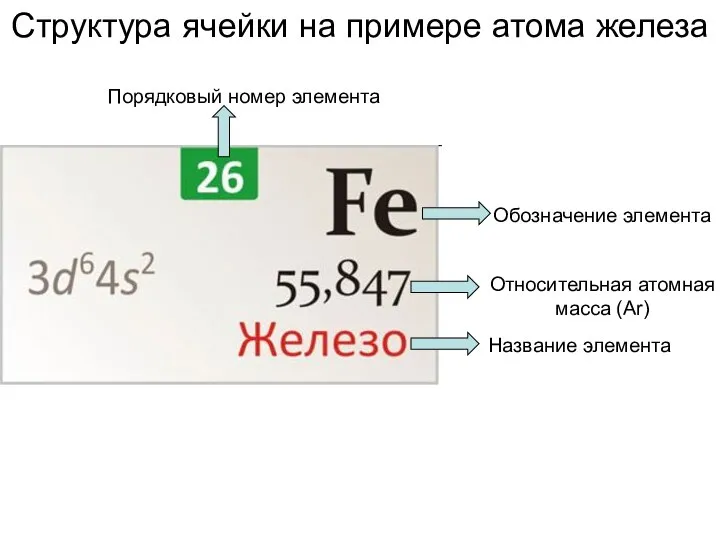 Структура ячейки на примере атома железа
Структура ячейки на примере атома железа Бавовник – біле золото Середньої Азії Підготував: Кійко Едуард
Бавовник – біле золото Середньої Азії Підготував: Кійко Едуард  Структура материала. Лекция 5
Структура материала. Лекция 5 Применение 3D-принтеров для решения химических задач
Применение 3D-принтеров для решения химических задач Мыс айналымы
Мыс айналымы Уравнение материального баланса для элементарного объема проточного химического реактора
Уравнение материального баланса для элементарного объема проточного химического реактора Проект соль
Проект соль Словарь просторечных молодёжных слов
Словарь просторечных молодёжных слов Возможности подготовки учащихся 9 и 11 классов к ГИА-9 и ЕГЭ по химии с использованием пособий издательства «Интеллект-Центр» Дмит
Возможности подготовки учащихся 9 и 11 классов к ГИА-9 и ЕГЭ по химии с использованием пособий издательства «Интеллект-Центр» Дмит