Содержание
- 2. ЧТО ТАКОЕ ОСНОВАНИЯ? Основания- сложные вещества, состоящие из атома металла, связанного с одной или несколькими гидроксогруппами
- 3. Общая формула оснований: Ме(ОН)n, где Ме - металл n-число гидроксогрупп и одновременно валентность металла.
- 4. Номенклатура оснований Название оснований= Гидроксид + название металла в родительном падеже + валентность римскими цифрами (переменная)
- 5. Номенклатура оснований
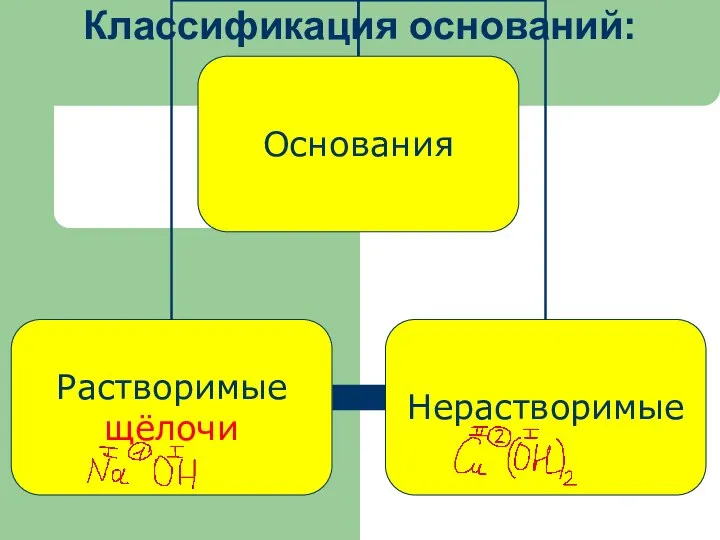
- 6. Классификация оснований:
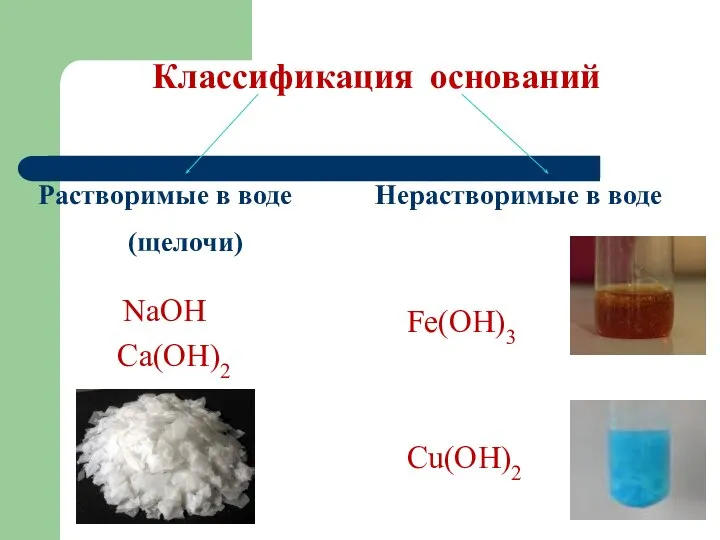
- 7. Классификация оснований Растворимые в воде (щелочи) Нерастворимые в воде NaOH Ca(OH)2 Fe(OH)3 Сu(OH)2
- 8. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ Взаимодействие с кислотами: NaOH + H2SO4 = Реакция нейтрализации – это реакция обмена
- 9. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ Взаимодействие с кислотными оксидами KOH+CO2=
- 10. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ Взаимодействие с солями, если образуется малорастворимая соль или малорастворимое основание NaOH+CuCl2=
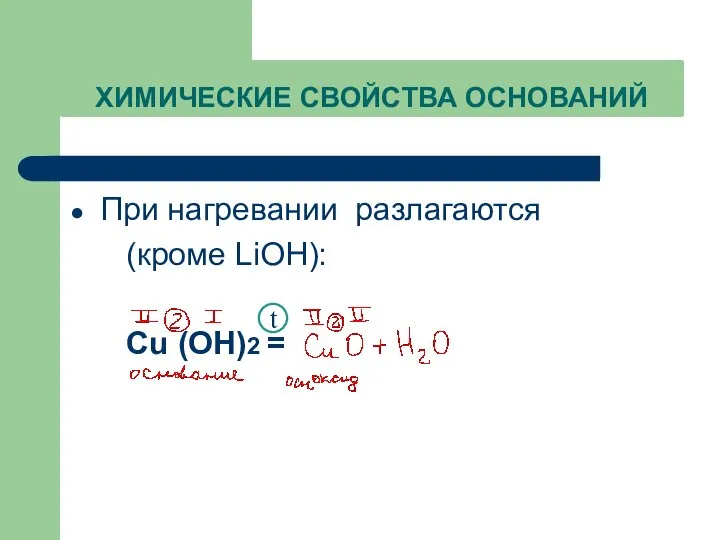
- 11. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ При нагревании разлагаются (кроме LiOH): Cu (OH)2 = t
- 13. Скачать презентацию






 Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Элементоорганические мономеры (соединения)
Элементоорганические мономеры (соединения) Природные и синтетические красители и ароматизаторы
Природные и синтетические красители и ароматизаторы Презентация по Химии "Свойства воды — презентация" - скачать смотреть
Презентация по Химии "Свойства воды — презентация" - скачать смотреть  Химическая связь
Химическая связь Хлор. Способы получения и применение
Хлор. Способы получения и применение Cкорость химической реакции
Cкорость химической реакции ДНК і РНК - нуклеїнові кислоти
ДНК і РНК - нуклеїнові кислоти Эндогенная серия. Карбонатитовая группа
Эндогенная серия. Карбонатитовая группа Классификация химических реакций
Классификация химических реакций Липидтер, жіктелуі (қарапайым және күрделі липидтер), қызметі, май қышқылдары
Липидтер, жіктелуі (қарапайым және күрделі липидтер), қызметі, май қышқылдары Защитные материалы
Защитные материалы Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов
Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов Строение вещества
Строение вещества Расшифровка структуры гликозидов
Расшифровка структуры гликозидов Полимеры, пластмассы и товары на их основе
Полимеры, пластмассы и товары на их основе Что такое полупроводники
Что такое полупроводники Показатель активности водородных ионов. Лабораторная работа №4
Показатель активности водородных ионов. Лабораторная работа №4 Смесители. Пропеллерная мешалка
Смесители. Пропеллерная мешалка Растворы. Часть 1
Растворы. Часть 1 Топливо. Механические топки
Топливо. Механические топки Пятичленные гетероциклы с двумя гетероатомами - азолы
Пятичленные гетероциклы с двумя гетероатомами - азолы Нефть как дисперсная система
Нефть как дисперсная система Решение задач. Органическая химия
Решение задач. Органическая химия Этилен. Действие этилена на рост проростков гороха
Этилен. Действие этилена на рост проростков гороха Александрит
Александрит Своя Игра Химия
Своя Игра Химия Классификация и номенклатура органических соединений
Классификация и номенклатура органических соединений