Содержание
- 3. Структура дисциплины Лекция1. Введение в общую химию: основные понятия и законы. Химический эквивалент. Классификация неорганических соединений.
- 4. Лекция 3. Основные закономерности протекания химических реакций. Термодинамическое описание системы. Формулировки законов термодинамики. Применение законов термодинамики.
- 5. Лекция 5. Растворы. Определение и классификация растворов. Способы выражения концентрации. Электролиты, неэлектролиты, электролитическая диссоциация. Причины распада
- 6. Метод электронного баланса.Метод полуреакции. Уравнение Нернста. Стандартные потенциалы электродных реакций. Лекция 8. Направленность окислительно-восстановительных реакций в
- 7. Литература 1) Курс общей химии под ред. Н.В. Коровина. М.: Высшая школа,1983. 2) Глинка Н.Л. Общая
- 8. Взаимосвязь химических наук
- 11. Основные понятия Химия – наука о свойствах вещества и его превращениях. Простые вещества образованы атомами одного
- 12. Атом - наименьшая частица химического элемента, неделимая химичеки, но делимая физически, сохраняющая все его химические свойства.
- 13. Атомное ядро – положительно заряженная субатомная частица, состоящая из нуклонов – протонов, нейтронов – связанных сильным
- 14. Валентность (от лат. valentia – сила), способность атома присоединять или замещать определенное число других атомов или
- 15. Энергия ионизации – энергия, которую нужно затратить, чтобы оторвать электрон от атома или иона. Энергия сродства
- 16. Молекулярная химическая формула – отражает состав и истинное соотношение атомов в молекуле (например, С2Н5ОН). Структурная химическая
- 17. Относительная молекулярная масса (Mr) - безразмерная величина, показывающая, во сколько раз масса молекулы данного вещества больше
- 18. Количество вещества, моль - означает определенное число структурных элементов (молекул, атомов, ионов). Обозначается n, измеряется в
- 19. Основные стехиометрические законы Закон сохранения массы веществ (М.В.Ломоносов, 1748 г.; А.Лавуазье, 1789 г.): Масса всех веществ,
- 20. Закон постоянства состава Впервые сформулировал Ж.Пруст (1808 г): Все индивидуальные химические вещества имеют постоянный качественный и
- 21. Закон Авогадро ди Кваренья (1811 г.) В равных объемах различных газов при одинаковых условиях (температура, давление
- 22. Закон кратных отношении (Дальтон, 1808). Если два элемента образуют между собой несколько химических соединений, то количества
- 23. Закон взаимосвязи массы и энергии (Эйнштейн): Энергия вещества прямо пропорциональна его массе, умноженной на квадрат скорости
- 24. Химическим эквивалентом элемента называется такое его количество, которое соединяется или замещает 1 весовую часть (1,008 г)
- 25. Химическим эквивалентом сложного вещества называют такое его количество (массу), которая соответствует массе формульной единицы, отнесенной к
- 26. Для простых и сложных веществ, если не приведена химическая реакция:
- 27. Число эквивалентов вещества (z) соответствует количеству разрушенных (измененных) химических связей или числу отданных/принятых электронов Фактор эквивалентности
- 28. Основные классы неорганических соединений Сложные вещества обычно делят на четыре важнейших класса: оксиды, основания (гидроксиды), кислоты,
- 29. К основным относятся оксиды типичных металлов, им соответствуют гидроксиды, обладающие свойствами оснований (CuO, ZnO, PbO, Na2O).
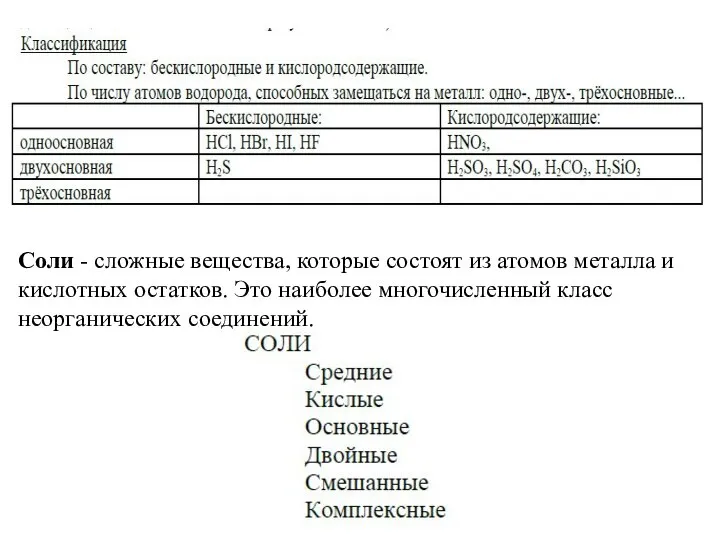
- 30. Соли - сложные вещества, которые состоят из атомов металла и кислотных остатков. Это наиболее многочисленный класс
- 31. Средние - при диссоциации дают только катионы металла (или NH4+) Кислые - при диссоциации дают катионы
- 32. Смешанные - образованы одним катионом и двумя анионами Комплексные - содержат сложные катионы или анионы.
- 35. Скачать презентацию































 Информационные технологии на уроках химии
Информационные технологии на уроках химии Способы переработки нефти
Способы переработки нефти Пластические массы
Пластические массы Правила безпечного використання засобів побутової хімії
Правила безпечного використання засобів побутової хімії  Теория электролитической диссоциации
Теория электролитической диссоциации Тема: «Самородные металлы».
Тема: «Самородные металлы». Энергетика химических процессов
Энергетика химических процессов Вплив фосфатної побутової хімії на організм людини.
Вплив фосфатної побутової хімії на організм людини.  Решение задач по теме «Растворы»
Решение задач по теме «Растворы» Химическая термодинамика и кинетика
Химическая термодинамика и кинетика соединения АЗОТА Материал для повторения и подготовки к ГИА Учитель химии МОУ «Гимназия №1»г. Саратова Шишкина И.Ю.
соединения АЗОТА Материал для повторения и подготовки к ГИА Учитель химии МОУ «Гимназия №1»г. Саратова Шишкина И.Ю. Основные свойства кристаллов
Основные свойства кристаллов Презентация по Химии "Етери та естери" - скачать смотреть бесплатно
Презентация по Химии "Етери та естери" - скачать смотреть бесплатно Поліетелен. Застосування поліетилену
Поліетелен. Застосування поліетилену Гипер-гипофосфатемия
Гипер-гипофосфатемия Ультразвук к в химической технологии. Лекция 5
Ультразвук к в химической технологии. Лекция 5 Класифікація пластмас
Класифікація пластмас  Дисциплина: Химия. Лекция 1. Растворы
Дисциплина: Химия. Лекция 1. Растворы Подготовка к ГИА. Тренажер по химии
Подготовка к ГИА. Тренажер по химии Ферменттер. Зерттелу тарихы
Ферменттер. Зерттелу тарихы Важнейшие кислоты и кислотные остатки. (Леция 1)
Важнейшие кислоты и кислотные остатки. (Леция 1) Углеводы. Строение углеводов
Углеводы. Строение углеводов Презентация по Химии "Горение кислорода" - скачать смотреть
Презентация по Химии "Горение кислорода" - скачать смотреть  Застосування нових сучасних матеріалів з оригінльними властивостями
Застосування нових сучасних матеріалів з оригінльними властивостями  Непредельные углероды. Алкены
Непредельные углероды. Алкены Синтетические моющие средства
Синтетические моющие средства Конденсация. Капельная и пленочная конденсация
Конденсация. Капельная и пленочная конденсация Імунопатологія. Імунопрофілактика і імунотерапія інфекційних захворювань. Засоби імунокорекції
Імунопатологія. Імунопрофілактика і імунотерапія інфекційних захворювань. Засоби імунокорекції