Основные понятия и законы химии. Периодический закон и периодическая система элементов Д. И. Менделеева. Теория строения веществ
Содержание
- 2. План: Введение. Основные понятия и законы химии. Периодический закон и периодическая система химических элементов Д.И. Менделеева.
- 3. 1. Введение Окружающий человека мир материален и, несмотря на все богатство его проявлений, в настоящее время
- 4. Введение Химия, как и всякая наука, есть в одно время и средство, и цель. Она есть
- 5. 2. Основные понятия и законы химии. 1. Все вещества (химические соединения) Вселенной состоят из молекул, а
- 6. Основные понятия и законы химии. 4. При протекании любой химической реакции массы реагирующих веществ и продуктов
- 7. 3. Периодический закон Д.И. Менделеева. «свойства простых веществ, а также свойства и формы соединений элементов находятся
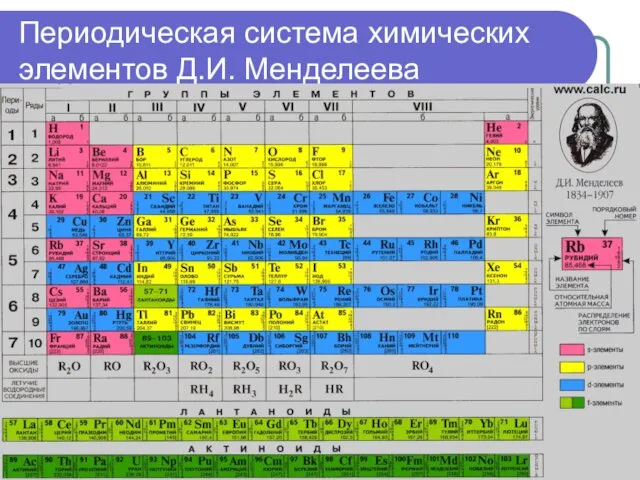
- 8. Периодическая система химических элементов Д.И. Менделеева это наглядное графическое изображение периодического закона. Химический элемент – это
- 9. В структуре таблицы (системы) выделяют периоды, группы и подгруппы. Периодом называют горизонтальную совокупность элементов, расположенных в
- 10. Периодическая система химических элементов Д.И. Менделеева
- 11. Характер изменения некоторых свойств элементов Энергия ионизации –это энергия, затраченная на отрыводного электрона от нейтрального атома,
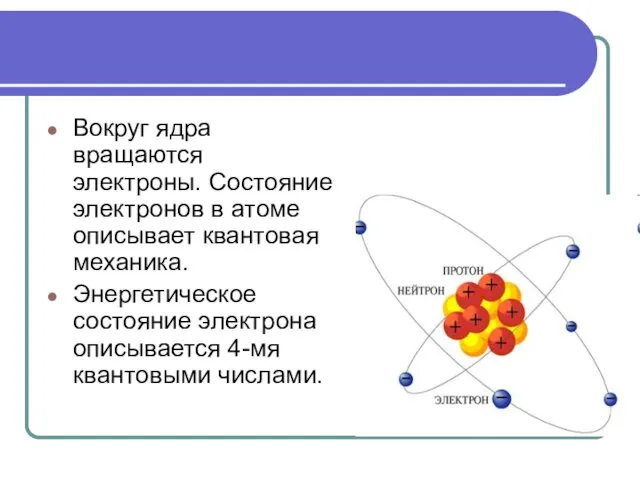
- 12. 3. Теория строения атомов. Атом любого элемента состоит из положительно заряженного ядра и отрицательно заряженных электронов,
- 13. Вокруг ядра вращаются электроны. Состояние электронов в атоме описывает квантовая механика. Энергетическое состояние электрона описывается 4-мя
- 14. n- главное квантовое число определяет энергию АО и номер энергетического уровня, на котором находится электрон и
- 15. Орбитальное квантовое число – l Орбитальное квантовое число – l определяет форму АО и энергетический подуровень
- 16. Магнитное квантовое число – ml ориентацию данной АО относительно направления магнитного поля и может принимать значения
- 17. Спиновое квантовое число- ms. характеризует вращение электрона вокруг своей оси. Спиновое квантовое число может принимать всего
- 18. Построение электронных формул атомов хим. Элементов базируется на 3 основных положениях принцип Паули согласно которому в
- 19. правило Хунда устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное
- 20. Принцип наименьшей энергии Первыми заполняются орбитали с наименьшей энергией Шкала энергии 1 s ® 2 s
- 21. Электронная конфигурация элементов Принадлежность элемента к электронному семейству определяется характером заполнения энергетических подуровней: s- элементы –
- 22. 4. Виды химической связи Атомы металлов способны отдавать электроны, атомы неметаллов- принимать. Образование химической связи объясняется
- 23. Выделяют следующие типы хим. связи: Ионная Ковалентная(полярная и не полярная) Водородная Металлическая
- 24. Ионная связь Образуется между атомами элементов металла с неметаллом. .. Na. + .Cl: = Na+Cl- ..
- 25. Ковалентная связь Образуется между атомами элементов неметаллов. CI2 –каждый из атомов хлора делится одним из своих
- 26. Ковалентная полярная связь Возникает между атомами элементов неметаллов с разной электроотрицательностью. Самый электроотрицательный элемент – F.
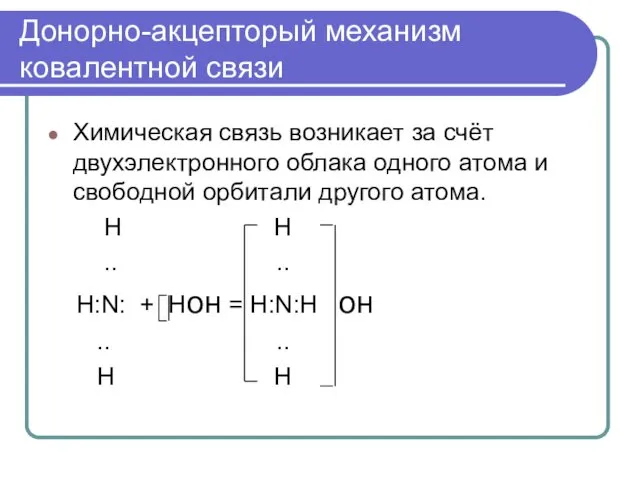
- 27. Донорно-акцепторый механизм ковалентной связи Химическая связь возникает за счёт двухэлектронного облака одного атома и свободной орбитали
- 28. Водородная связь(межмолекулярная) Возникает между молекулами в состав которых входит водород и сильно электроотрицательный элемент (F, O,
- 29. Металлическая связь В твердом состоянии металлы отличаются от всех остальных веществ своими характерными свойствами - очень
- 30. Металлическая связь Эти свойства обусловлены металлической связью. У металлов имеется избыток орбиталей и недостаток электронов. Валентные
- 32. Скачать презентацию


























 Синтетические каучуки, строение, свойства, применение.
Синтетические каучуки, строение, свойства, применение. Введение. Развитие химической технологии как науки
Введение. Развитие химической технологии как науки Фотоэлектрические и информационные свойства фоточувствительных карбазолилсодержащих олигомерных пленочных композитов
Фотоэлектрические и информационные свойства фоточувствительных карбазолилсодержащих олигомерных пленочных композитов Химия и проблемы экологии. Кислотные дожди
Химия и проблемы экологии. Кислотные дожди Сероводород. Сернистый водород, сульфид водорода, дигидросульфид
Сероводород. Сернистый водород, сульфид водорода, дигидросульфид Кремний – бог неорганической природы
Кремний – бог неорганической природы Неметаллы: общая характеристика
Неметаллы: общая характеристика Новые катализаторы
Новые катализаторы Презентация по Химии "Пищевые добавки. Е - коды" - скачать смотреть
Презентация по Химии "Пищевые добавки. Е - коды" - скачать смотреть  Инструментальные методы анализа
Инструментальные методы анализа Глюкоза Презентацію виконали учениці 11-Б класу Христинівської спеціалізованої школи І – ІІІ ступенів № 1 ім. О. Є. Корнійчука В
Глюкоза Презентацію виконали учениці 11-Б класу Христинівської спеціалізованої школи І – ІІІ ступенів № 1 ім. О. Є. Корнійчука В Формирование системы знаний о веществе. Лекция 14-15
Формирование системы знаний о веществе. Лекция 14-15 Спектроскопія ямр на ядрах 13с
Спектроскопія ямр на ядрах 13с Презентация по химии Фосфор
Презентация по химии Фосфор  Аллотропия углерода
Аллотропия углерода Презентация по Химии "Презентація на тему : «Фосфатні добрива у нашому житті»" - скачать смотреть бесплатно
Презентация по Химии "Презентація на тему : «Фосфатні добрива у нашому житті»" - скачать смотреть бесплатно Строение атома. Периодический закон
Строение атома. Периодический закон Углеводы. Моносахариды. Дисахариды
Углеводы. Моносахариды. Дисахариды Аминокилоты. Получение и применение
Аминокилоты. Получение и применение Производные дигидропиридина (нефидипин, амлодипин, форидон) и пиридина (супрастин)
Производные дигидропиридина (нефидипин, амлодипин, форидон) и пиридина (супрастин) Минералогическая шкала твёрдости Мооса
Минералогическая шкала твёрдости Мооса Занятие по познавательному развитию на тему: «Где спрятался воздух?» в средней группе.
Занятие по познавательному развитию на тему: «Где спрятался воздух?» в средней группе.  Етиловий спирт та його вплив на організм людини
Етиловий спирт та його вплив на організм людини Машиностроительные материалы
Машиностроительные материалы Типы химических реакций в органической химии. Типы реакций в органике
Типы химических реакций в органической химии. Типы реакций в органике Нуклеозиды и нуклеотиды. Нуклеиновые кислоты. (Лекция 50.15)
Нуклеозиды и нуклеотиды. Нуклеиновые кислоты. (Лекция 50.15) Структура периодической системы химических элементов
Структура периодической системы химических элементов Презентация по Химии "Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение" - скачать смотреть бесплат
Презентация по Химии "Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение" - скачать смотреть бесплат