Содержание
- 2. Законы стехиометрии Закон сохранения массы (1748 г., М.В.Ломоносов, 1789 г., Лавуазье). Закон постоянства состава (1801 г.,
- 6. Пруст Жозеф Луи (1754-1828 г.)
- 8. Стехиометрия - это совокупность расчетов, основанных на химических формулах и уравнениях реакций. Правило, вытекающее из законов
- 9. Следствие из правила Для расчета концентрации вещества, вступившего или образовавшегося, необходимо и достаточно знать концентрацию какого-либо
- 16. Cильные электролиты Кислоты: HCl, HBr, HI, HNO3, H2SO4 (по 1-ой ступени). Основания: NaOH, KOH, Ca(OH)2, Sr(OH)2,
- 17. Теория ионных равновесий Теория электролитической диссоциации С.Аррениуса (1887 г.). Теория сильных электролитов (П.Дебай, Э.Хюккель, 1923 г.).
- 19. Закон начальной концентрации Концентрация любого вещества в растворе равна сумме равновесных концентраций всех ионов, образованных данным
- 20. Закон сохранения заряда Сумма произведений концентрации каждого иона на его заряд равна нулю. Пример: Cr2O72- +
- 21. Теория сильных электролитов (1923 г, Дебай, Хюккель) 1. Сильные электролиты в водных растворах диссоциируют полностью, т.е.
- 22. ДЕБАЙ (Debye), Петер Джозеф Уильям 24 марта 1884 г. – 2 ноября 1966 г. Нобелевская премия
- 23. ХЮККЕЛЬ (Hückel), Эрих Арманд Артур Йозеф 9 августа 1896 г. – 16 февраля 1980 г.
- 24. Теория сильных электролитов K+ + m H2O → [K(OH2)m]+ катионный гидрат A– + n H2O →
- 25. Количество ионных пар зависит от: силы электролита; концентрации электролита; заряда ионов; степени симметрии электролита. NaCl ZnSO4
- 26. Ионная сила раствора Является мерой электростатического взаимодействия всех ионов в растворе, обозначается I (или μ). I
- 27. Формула Льюиса-Рендалла (1921 г.) Активность (действующая концентрация) ai = Ci ⋅ fi С – истинная концентрация
- 28. Значение I: 0 – 0,05 – 0,1 – 1 2 3 1. I → 0 I=0,05-0,1
- 29. Закон Рендалла (закон ионной силы): при значениях ионной силы ≤ 0,05 коэффициент активности не зависит от
- 30. КОЭФФИЦИЕНТЫ АКТИВНОСТИ f
- 31. Зависимость f от I
- 32. Закон действующих масс и его использование в расчетах
- 35. КТ - термодинамическая константа КТ = f (природа вещества, природа растворителя, Т, Р), не зависит от
- 36. Кf - функция активности Кf
- 37. fi известны не только для ионов, но и для молекул сильных электролитов, они называются среднеионными:
- 38. Применение теории сильных электролитов в аналитических расчетах Для раствора, содержащего 0,1 М СаСl2, 0,2 М КСl
- 39. Расчет концентрационной константы CH3COOH CH3COO- + H+ f1 f1 Kk = KT/f12 Kk = 1,7.10-5/(0,84)2=2,4.10-5
- 41. Скачать презентацию






















![Теория сильных электролитов K+ + m H2O → [K(OH2)m]+ катионный гидрат](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397141/slide-23.jpg)



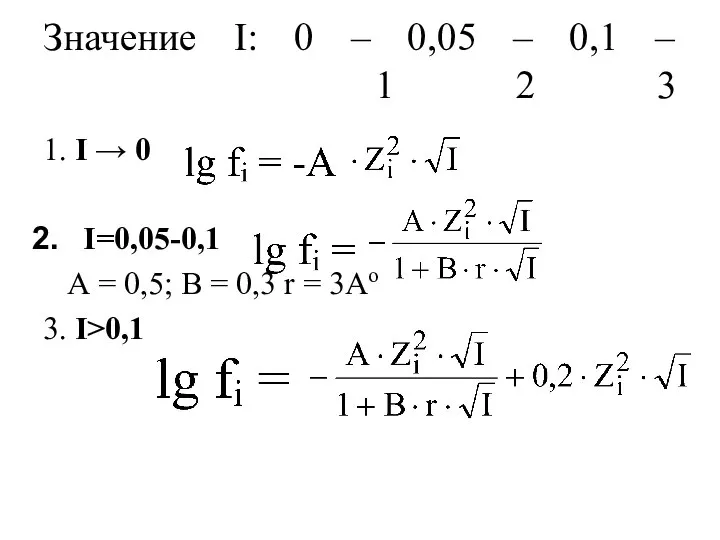











 Серная кислота. (9 класс)
Серная кислота. (9 класс) Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Atomic number, Mass number and Isotopes
Atomic number, Mass number and Isotopes Ароматические углеводороды
Ароматические углеводороды Каталитикалық крекинг
Каталитикалық крекинг Аттестационная работа. Проектно-исследовательская деятельность учащихся на уроках химии и во внеурочной работе
Аттестационная работа. Проектно-исследовательская деятельность учащихся на уроках химии и во внеурочной работе Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Характеристика элементов VI-В группы. Хром
Характеристика элементов VI-В группы. Хром Строение атома. Периодичность свойств элементов и их соединений
Строение атома. Периодичность свойств элементов и их соединений Вольфрам және молибден
Вольфрам және молибден КРАХМАЛ и ЦЕЛЛЮЛОЗА (С6Н10О5)n
КРАХМАЛ и ЦЕЛЛЮЛОЗА (С6Н10О5)n  Ш. Мәрҗани исемендәге Комыргуҗа урта мәктәбе Физика укытучысы Шәрәфетдинова Р.З. 2012 ел
Ш. Мәрҗани исемендәге Комыргуҗа урта мәктәбе Физика укытучысы Шәрәфетдинова Р.З. 2012 ел Познаваемость мира. Сведения о клетке. Подготовила ученица 11 класса Шапаренко Екатерина
Познаваемость мира. Сведения о клетке. Подготовила ученица 11 класса Шапаренко Екатерина Химия элементов IVA группы
Химия элементов IVA группы Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия
Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия Органическое топливо. Теплота сгорания топлива
Органическое топливо. Теплота сгорания топлива Химические свойства и получение алканов
Химические свойства и получение алканов Кислород и его применение
Кислород и его применение Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Алюминий және оның қосылыстары
Алюминий және оның қосылыстары Кремний и его соединения
Кремний и его соединения Характеристика металу Ферум
Характеристика металу Ферум Виды присадок к моторному топливу. Керосин
Виды присадок к моторному топливу. Керосин Предмет химии. Вещества и их физические свойства. (8 класс)
Предмет химии. Вещества и их физические свойства. (8 класс) Эпоксидная смола
Эпоксидная смола Материя и цвет. Свет
Материя и цвет. Свет Способы выражения состава раствора. Решение задач
Способы выражения состава раствора. Решение задач Метаболизм источников энергии
Метаболизм источников энергии