Содержание
- 2. где A,B,M,N – химические символы реагирующих веществ, α, β, γ, δ - стехиометрические коэффициенты, показывающие число
- 3. и найти стехиометрические коэффициенты α, β, γ, δ из уравнений баланса атомов С, Н и О
- 4. Химические реакции горения и газификации протекают с выделением или поглощением тепла, которое называется теплотой реакции. Всякая
- 5. Если энергия, выделяющаяся при образовании новых связей, больше энергии, затрачиваемой на разрушение связей в исходных молекулах,
- 6. Лекция 5 Согласно 1-му началу термодинамики, изменение внутренней энергии dU или энтальпии dH = d(U+pV) реагентов
- 7. Лекция 6 Если реакция протекает при постоянном объёме (V,Т = const , изохорно-изотермический процесс), и при
- 8. Лекция 5 Теплота реакций при р,Т = const или при V,T = const не зависит от
- 9. Лекция 5 Теплота реакции равна сумме теплот сгорания исходных реагентов за вычетом суммы теплот сгорания продуктов
- 10. Компоненты горючей смеси могут находиться в одном агрегатном состоянии, например, – газообразном при сжигании газов в
- 11. Энтальпия образования сложного вещества есть энтальпия реакции его синтеза из простых в-в, взятых в наиболее устойчивых
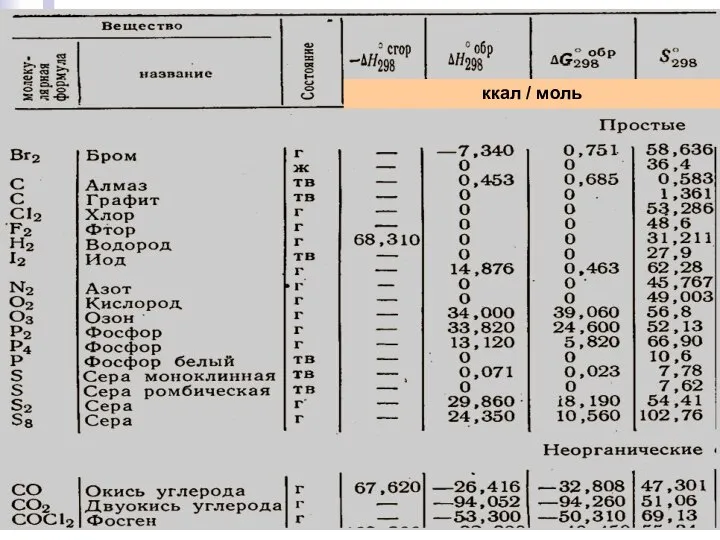
- 12. Энтальпия сгорания простого и сложного вещества есть энтальпия реакции его полного окисления кислородом до образования высших
- 13. Лекция 6 ккал / моль
- 14. Лекция 5
- 15. Лекция 6
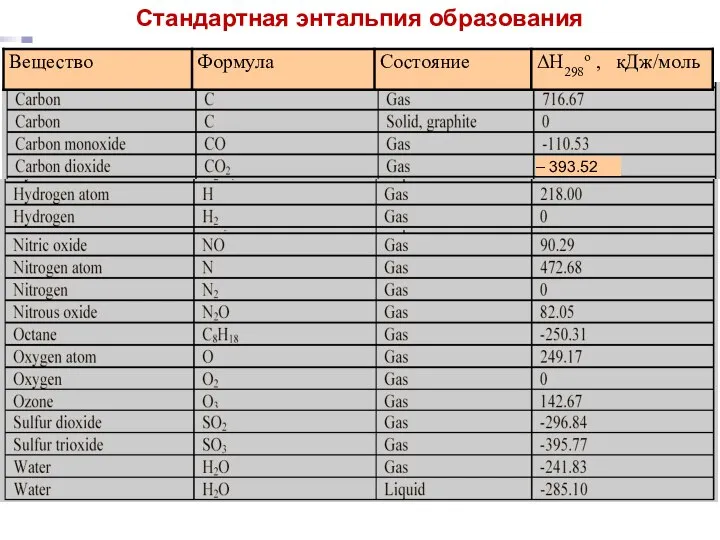
- 16. Лекция 5 – 393.52 Стандартная энтальпия образования
- 17. (11.28 = 3 × (0.79/0.21). Лекция 5 Предполгается, что смесь находится в стехиометрическом соотношении при стандартных
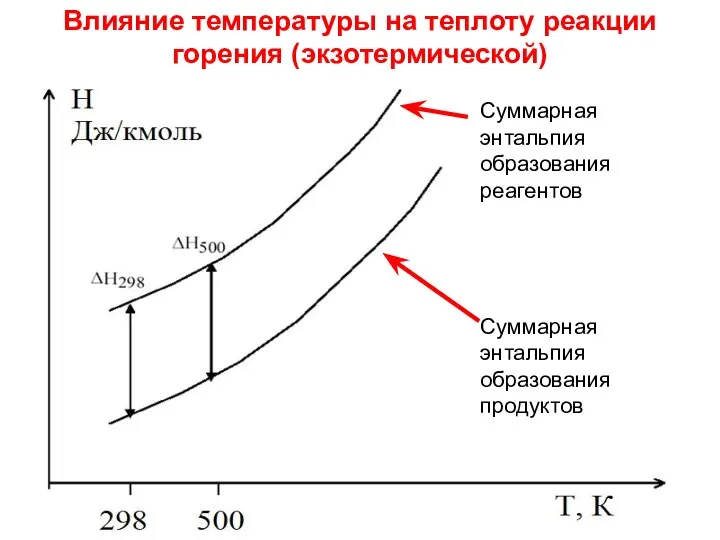
- 18. Лекция 6 Суммарная энтальпия образования продуктов Суммарная энтальпия образования реагентов Влияние температуры на теплоту реакции горения
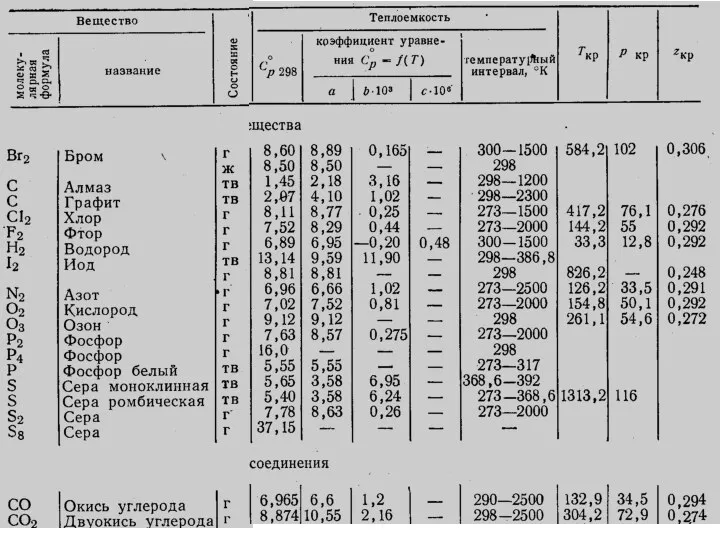
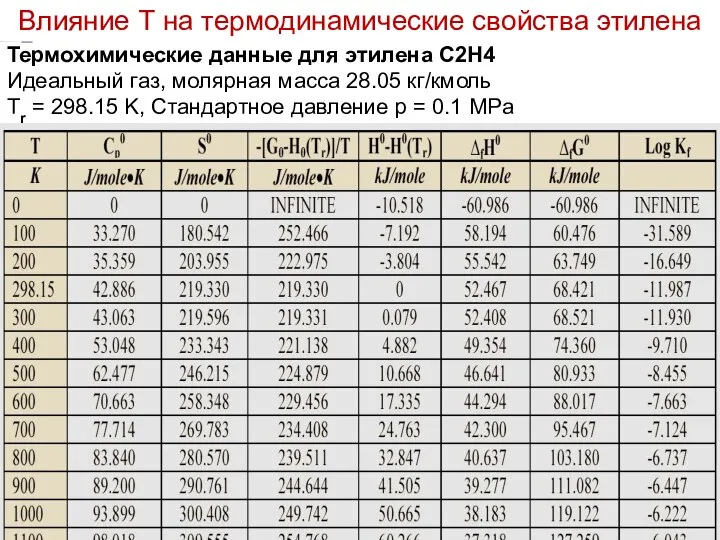
- 19. Лекция 6 Термохимические данные для этилена C2H4 Идеальный газ, молярная масса 28.05 кг/кмоль Tr = 298.15
- 20. Лекция 5 Предполгается, что смесь находится в стехиометрическом соотношении при р = 1 атм, Т =
- 21. Экспериментально установлено, что химические реакции не всегда протекают до полного превращения исходных веществ. Наряду с продуктами
- 22. Скорость химической реакции, как будет показано далее, пропорциональна концентрациям (количество вещества в единице объёма) участвующих в
- 23. В зависимости от условий (Т, р) равновесие может быть, например, сильно смещено в сторону продуктов реакции.
- 24. Скорость протекания химических реакций и положение равновесия зависят от химической природы реагирующих веществ, концентрации реагирующих веществ,
- 25. Лекция 6 Скорость прямой реакции в любой момент времени: а скорость обратной реакции Закон действующих масс
- 26. Здесь CA ,CB ,CM ,CN – текущие концентрации реагирующих веществ, моль/м3, k1 и k2 – коэффициенты
- 27. Результирующая скорость реакции, равная разности скоростей прямой и обратной реакций, в ходе превращения уменьшается и становится
- 28. Лекция 6 КС – безразмерная величина, называемая константой равновесия (по концентрациям). Отсюда следует выражение для концентраций
- 29. Так как k1 и k2 при данной температуре являются постоянными, то и константа равновесия КС является
- 30. Лекция 6 поэтому константу равновесия Кp можно выразить через парциальные давления газов в смеси. Для эквимолярной
- 31. Если в газовой смеси может происходить несколько различных реакций, то закон действующих масс применяется к каждой
- 32. Скорости обратных реакций разложения (диссоциации) продуктов сгорания при топочных температурах (1600-18000С и ниже) весьма малы (например,
- 33. Строго говоря, область применения закона действующих масс ограничивается идеальными газами, однако с достаточной для практики точностью,
- 34. Для процессов горения важное значение имеют гетерогенные реакции в системах, в частности, состоящих из твердого топлива
- 35. Если на систему в состоянии равновесия воздействовать извне, изменяя термодинамические параметры состояния (р, V, Т), то
- 36. Например, если прямая реакция экзотермична (протекает с выделение теплоты), как в случае реакций горения (следовательно, обратная
- 37. Лекция 6 Если из системы выводится какой-либо продукт, то равновесие сдвигается в сторону увеличения его концентрации.
- 38. Давление воздействует на положение равновесия в том случае, если реакция протекает с изменением объема газов и
- 39. Принцип Ле Шателье-Брауна указывает только направление смещения равновесия, но не дает возможности провести количественные расчеты. Соотношения,
- 40. При очень высоких температурах реакции горения вообще не протекают. Следовательно, за счет горения нельзя достичь очень
- 41. Зависимость химического равновесия реакций горения от температуры При внешнем изменении температуры равновесие системы смещается в ту
- 42. Знак "–" в правой части показывает, что: если Q = ΔrH если Q = ΔrH >
- 43. Лекция 5 G0, H0, S0– стандартные значения (р=1 атм, Т = 298 К) энергии Гиббса, энтальпии
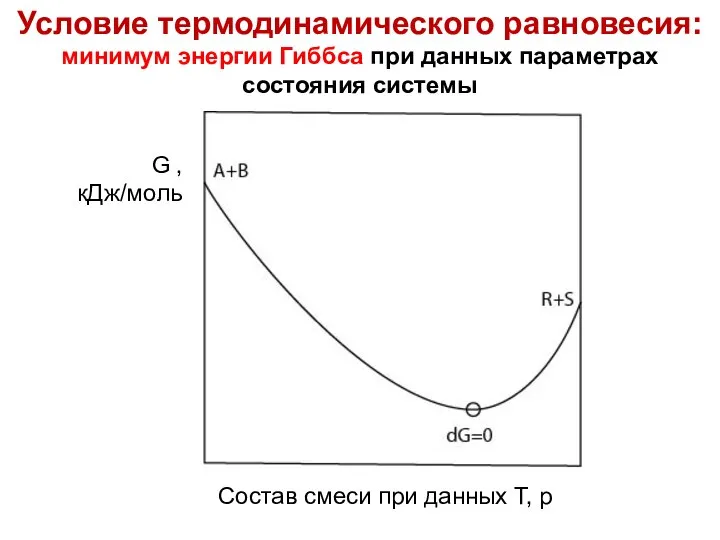
- 44. Лекция 6 Условие термодинамического равновесия: минимум энергии Гиббса при данных параметрах состояния системы
- 45. Лекция 5 Сжигание топлива при высоких температурах (Т > 1300 К) сопровождается окислением азота воздуха с
- 47. Скачать презентацию






































 Окисно-відновні реакції та їхнє значення
Окисно-відновні реакції та їхнє значення Квантовая механика – теоретическая основа современной химии
Квантовая механика – теоретическая основа современной химии Типы ингибирования и их характерные черты
Типы ингибирования и их характерные черты Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Строение молекул некоторых широко распространенных гербицидов
Строение молекул некоторых широко распространенных гербицидов Голубое золото
Голубое золото Кремний. Основа неживой природы
Кремний. Основа неживой природы Химия в нашей жизни
Химия в нашей жизни Клетка элементарная единица живого
Клетка элементарная единица живого Ферменты в пищевой промышленности
Ферменты в пищевой промышленности Фосфор
Фосфор Кислоты и основания
Кислоты и основания Природні джерела органічних речовин Підготувала Учениця 11-Б класу Білик Вікторія
Природні джерела органічних речовин Підготувала Учениця 11-Б класу Білик Вікторія  Классификация химических элементтов
Классификация химических элементтов Геохимия. Геохимическая система элементов
Геохимия. Геохимическая система элементов Классификация аминокислот в зависимости от природы радикалов. (Лекция 3)
Классификация аминокислот в зависимости от природы радикалов. (Лекция 3) Исследовательская работа по теме: « Волшебные жидкости – вещества определители или как определить вкус веществ не пробуя их»
Исследовательская работа по теме: « Волшебные жидкости – вещества определители или как определить вкус веществ не пробуя их»  Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Качественные реакции на функциональные группы
Качественные реакции на функциональные группы Жири. Склад жирів, їх утворення. Жири у природі. Біологічна роль жирів.
Жири. Склад жирів, їх утворення. Жири у природі. Біологічна роль жирів.  Операции термической обработки
Операции термической обработки Состав и основные свойства янтаря и древесных смол
Состав и основные свойства янтаря и древесных смол Горные породы и минералы. Камни-самоцветы
Горные породы и минералы. Камни-самоцветы Презентация по химии Карбоновые кислоты и их производные
Презентация по химии Карбоновые кислоты и их производные  Пигменті в реставрации декоративно-прикладного искусства
Пигменті в реставрации декоративно-прикладного искусства Презентация по Химии "Волшебный сад" - скачать смотреть
Презентация по Химии "Волшебный сад" - скачать смотреть  Система инактивации лекарственных средств в организме человека
Система инактивации лекарственных средств в организме человека Згубний вплив спиртів на організм людини Підготувала Гуцал Наталія 9-Б клас
Згубний вплив спиртів на організм людини Підготувала Гуцал Наталія 9-Б клас