Содержание
- 2. Функциональная группа – это атом или группа атомов неуглеводородного характера, которые определяют принад-лежность соединения к определённому
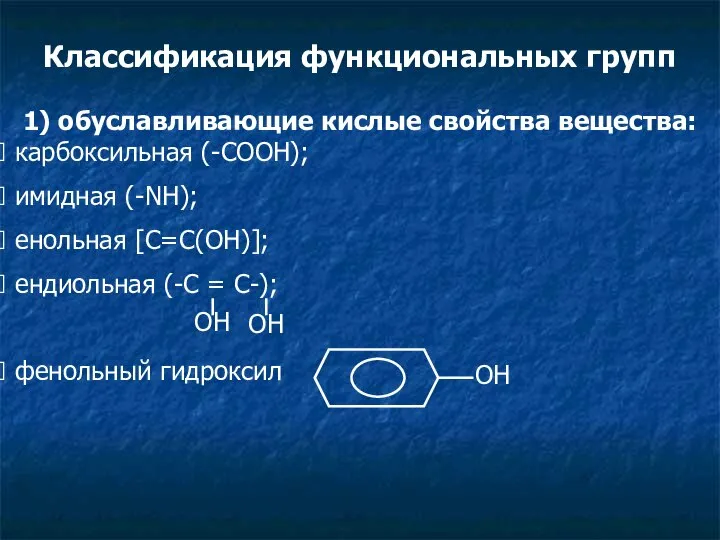
- 3. Классификация функциональных групп 1) обуславливающие кислые свойства вещества: карбоксильная (-СООН); имидная (-NH); енольная [C=C(OH)]; ендиольная (-С
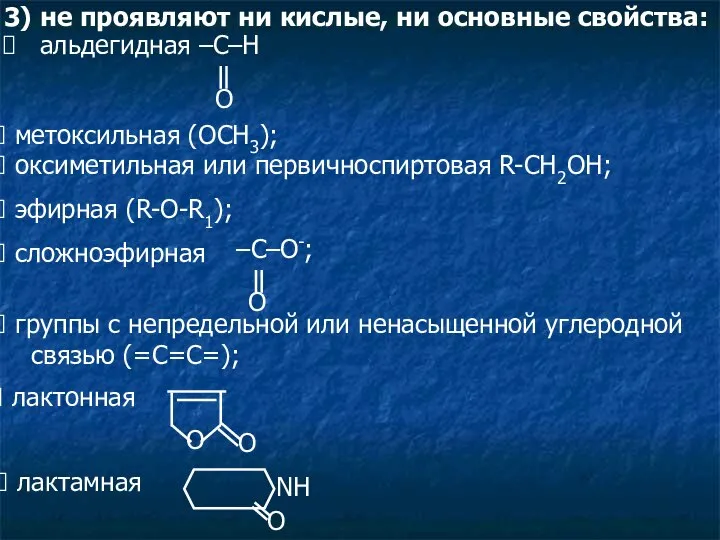
- 5. 3) не проявляют ни кислые, ни основные свойства: метоксильная (ОСН3); оксиметильная или первичноспиртовая R-CH2OH; эфирная (R-O-R1);
- 6. C2H5OH + CH3COOH C2H5О – C – CH3 + H2O КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ФУНКЦИОНАЛЬНЫЕ ГРУППЫ I.
- 7. II. Гидроксильная группа – фенольная. Лекарственные средства, содержащие фено-льную группу: салициловая кислота; ацетилсалициловая кислота; салицилат натрия;
- 8. III. Карбонильная группа – альдегидная. Лекарственные средства: глюкоза; раствор формальдегида. Реакция «серебряного зеркала» AgNO3 + 3NH4OH
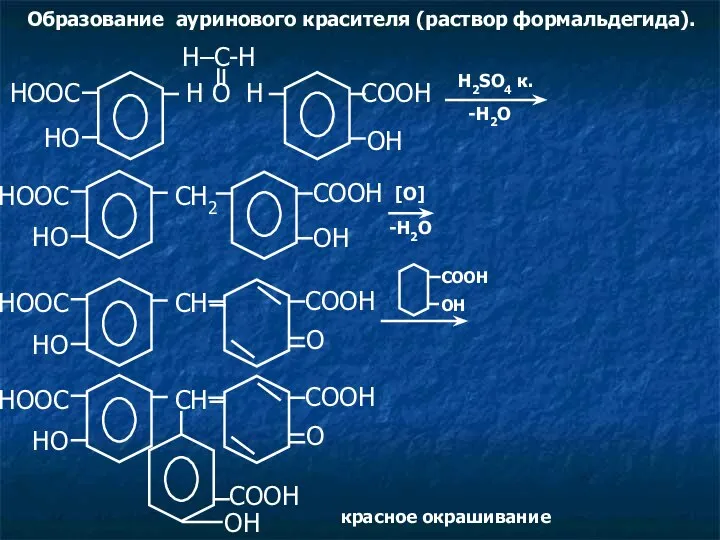
- 9. Образование ауринового красителя (раствор формальдегида). HOOC CH HO O COOH OH COOH красное окрашивание
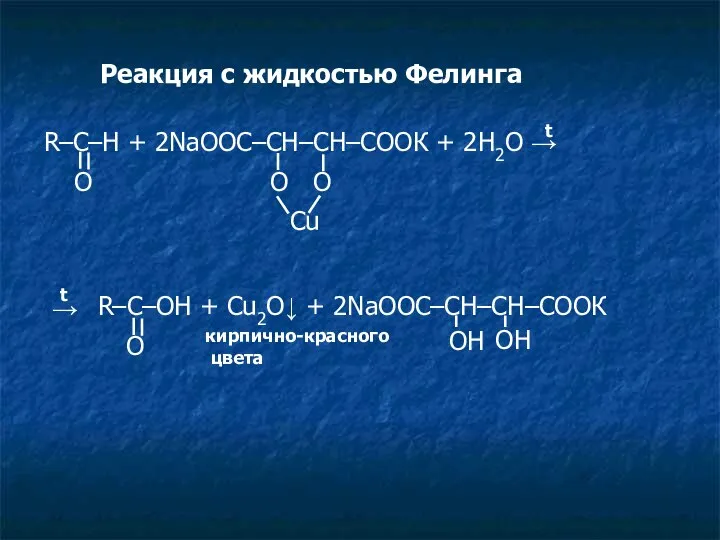
- 10. Реакция с жидкостью Фелинга R–C–H + 2NaOOC–CH–CH–COOК + 2H2O → O O O Cu t O
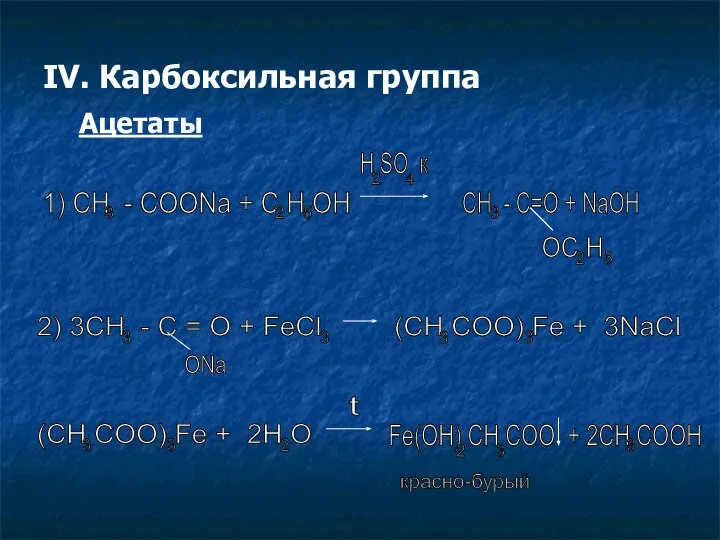
- 11. IV. Карбоксильная группа Ацетаты 1) CH - COONa + C H OH 3 2 5 H
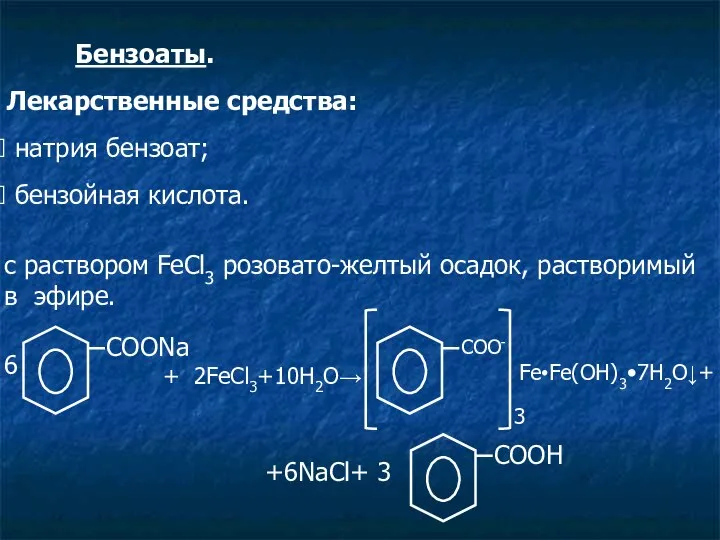
- 12. Бензоаты. Лекарственные средства: натрия бензоат; бензойная кислота. c раствором FeCl3 розовато-желтый осадок, растворимый в эфире. 6
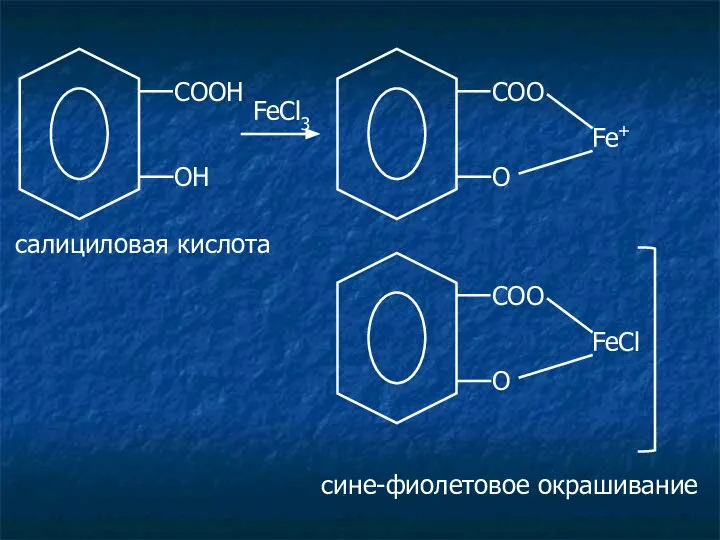
- 13. Салицилаты. Лекарственные средства: салициловая кислота; натрия салицилат. c раствором FeCl3 появляется сине-фиолетовое или красное окрашивание, сохраняется
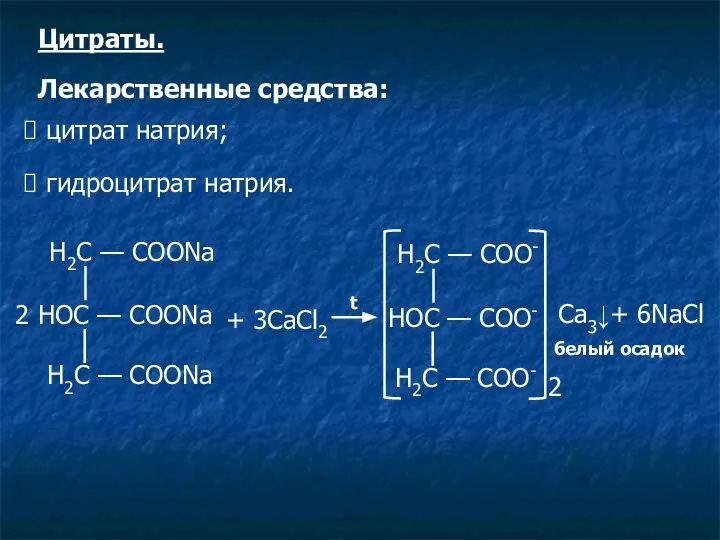
- 15. Н2С — СООNa 2 НOС — СООNa Н2С — СООNa + 3CaCl2 t Н2С — СОО-
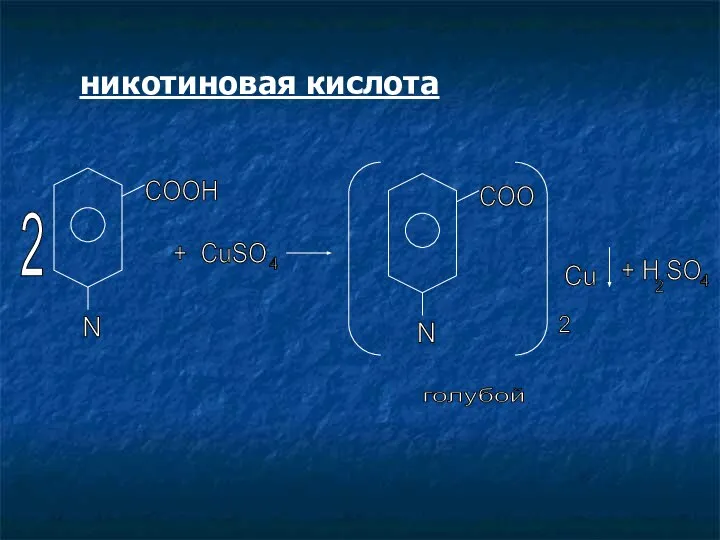
- 16. никотиновая кислота N 2 COOH + CuSO 4 N COO 2 Cu + H SO 2
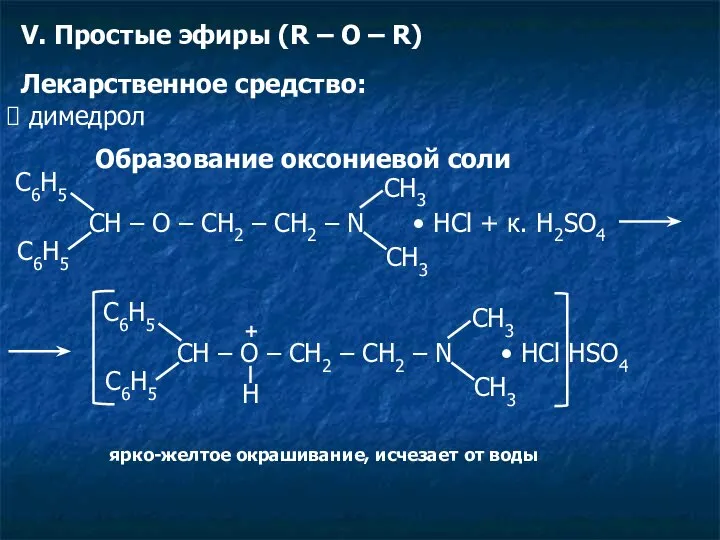
- 17. V. Простые эфиры (R – O – R) Лекарственное средство: димедрол Образование оксониевой соли CH –
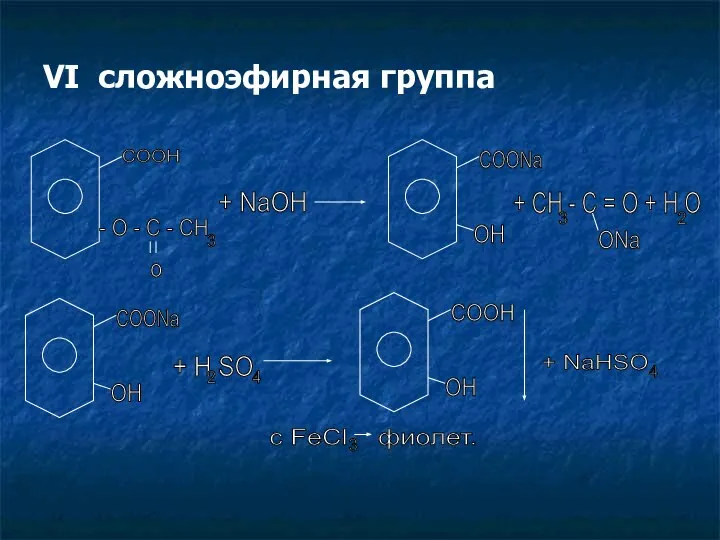
- 18. VI сложноэфирная группа COOH - O - C - CH 3 o + NaOH COONa OH
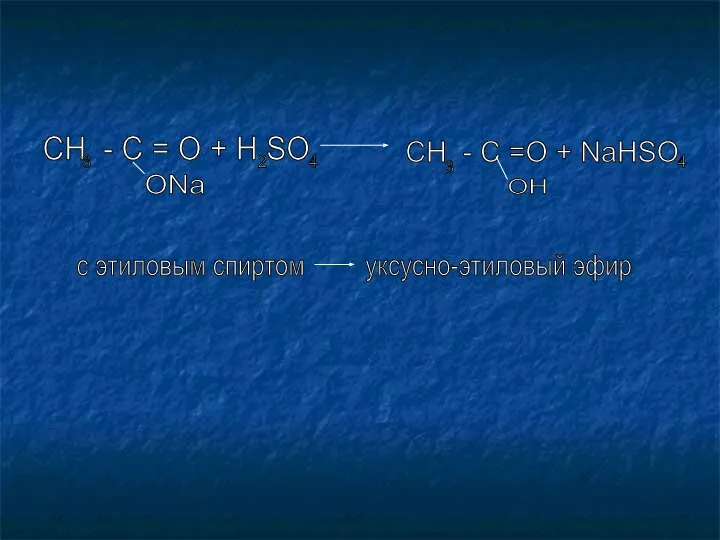
- 19. CH - C = O + H SO 3 ONa 2 4 CH - C =O
- 20. VII. Амины ароматические первичные (R – NH2) Лекарственные средства: анестезин; новокаин; стрептоцид; норсульфазол; сульфацил натрия; натрия
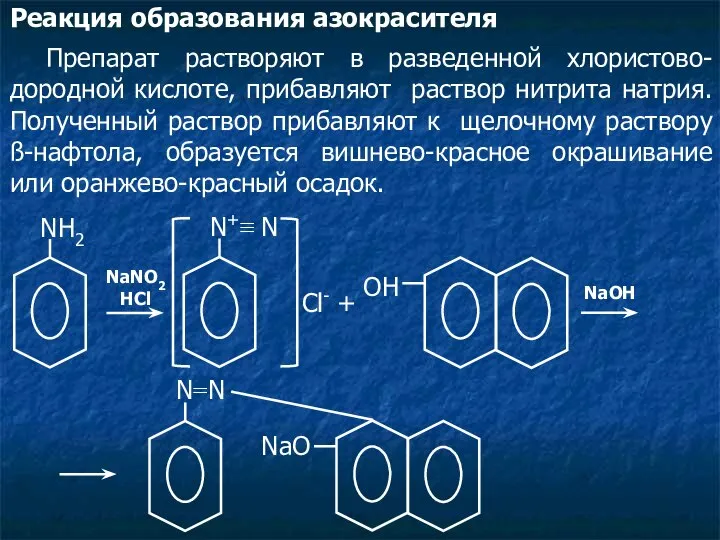
- 21. Реакция образования азокрасителя Препарат растворяют в разведенной хлористово-дородной кислоте, прибавляют раствор нитрита натрия. Полученный раствор прибавляют
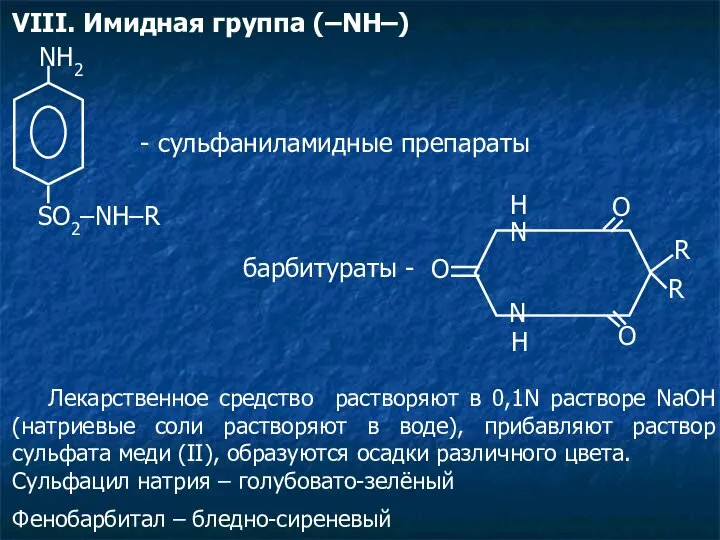
- 22. VIII. Имидная группа (–NH–) NH2 SO2–NH–R - сульфаниламидные препараты O N N O R R O
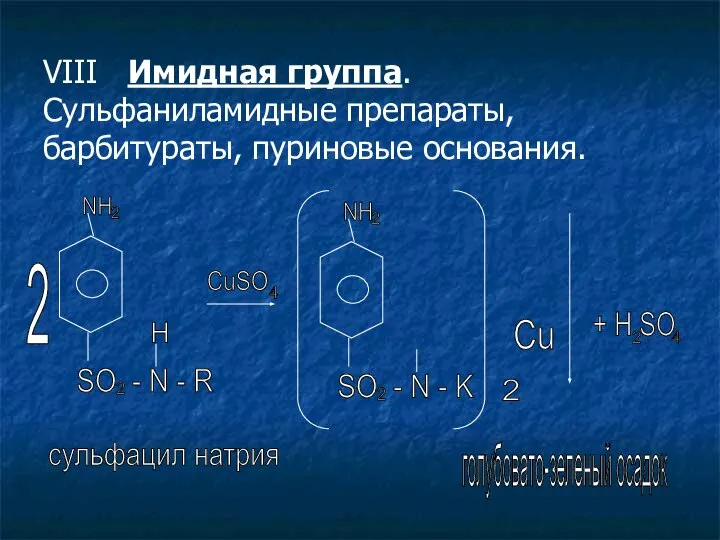
- 23. VIII Имидная группа. Сульфаниламидные препараты, барбитураты, пуриновые основания. 2 NH 2 SO - N - R
- 24. Кислотно-основное титрование в неводных средах Определяют вещества, которые в водной среде невозможно определить методом нейтрализации Из-за
- 25. МЕТОД НЕВОДНОГО ТИТРОВАНИЯ Классификация растворителей Амфитропные или амфотерные: H2O, CH3OH, C2H5OH и другие. Эти растворители играют
- 26. 3) Протофильные или основные: NH3, H2N-NH2, H2N(CH2)2NH2, HCON(CH3)2 и другие вещества основного характера. Молекулы протофильных растворителей
- 27. Преимущество метода кислотно-основного титрования в неводных средах состоит и в том, что он позволяет определять соли
- 28. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ОСНОВАНИЙ И ИХ СОЛЕЙ. HClO4 + CH3COOH → ClO4- + CH3COOH2+ кислота основание ион
- 29. Реакция нейтрализации сопровождается образо-ванием молекул того растворителя, в среде которого протекает данная реакция. 1) HClO4 +
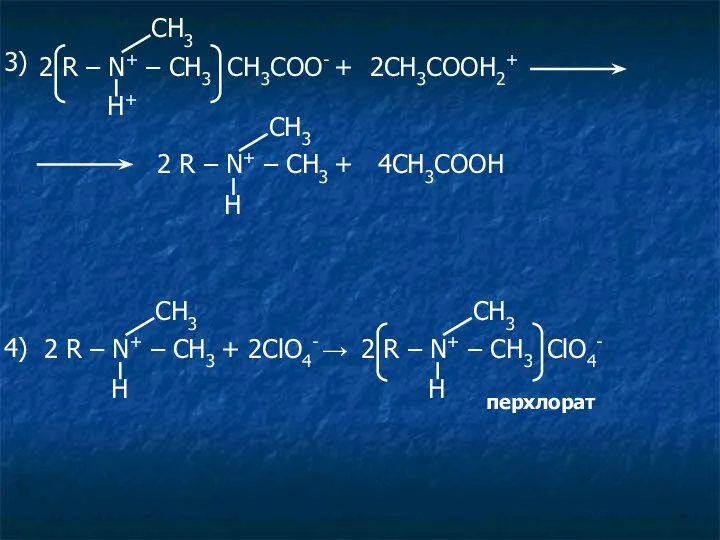
- 30. 2 R – N+ – CH3 CH3COO- + 2CH3COOH2+ Н+ СН3 3) Н СН3 2 R
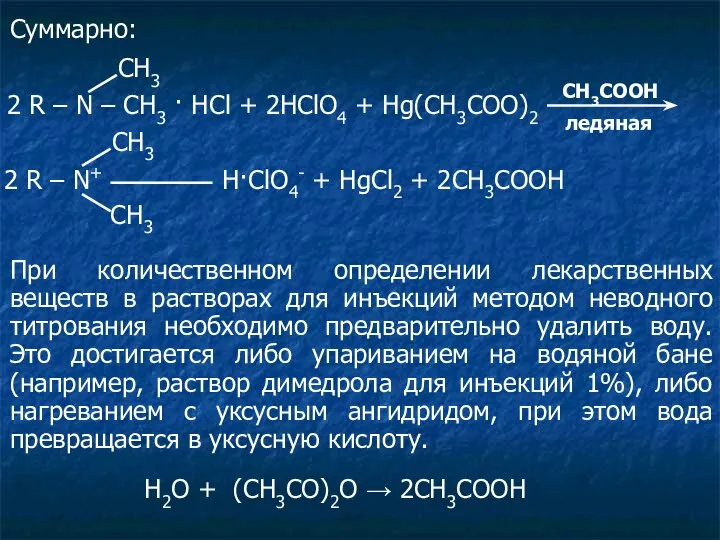
- 31. Суммарно: 2 R – N – CH3 · HCl + 2HClO4 + Hg(CH3COO)2 СН3 CH3COOH ледяная
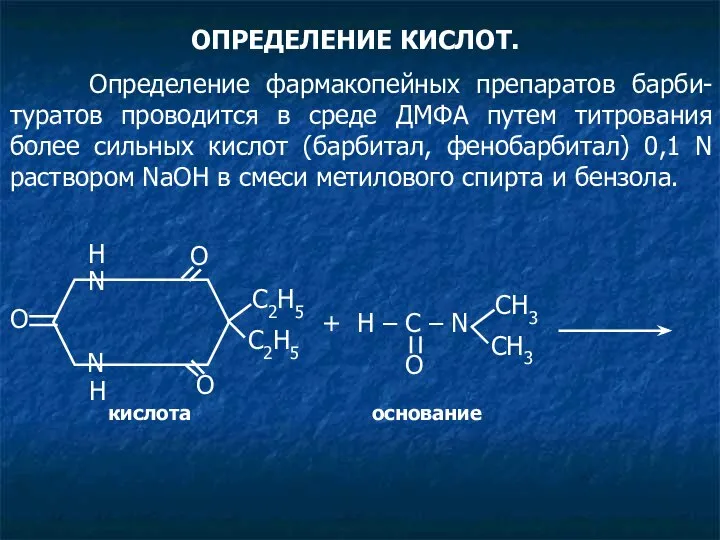
- 32. ОПРЕДЕЛЕНИЕ КИСЛОТ. Определение фармакопейных препаратов барби-туратов проводится в среде ДМФА путем титрования более сильных кислот (барбитал,
- 33. HO N N O С2Н5 O H С2Н5 + H – C – N+ O СН3
- 35. Скачать презентацию














 Каучуки. Природний каучук, гума, синтетичний каучук
Каучуки. Природний каучук, гума, синтетичний каучук Сера и её соединения
Сера и её соединения Оксосоединения: альдегиды и кетоны
Оксосоединения: альдегиды и кетоны Изооктан. Получение. Октановое число и степень сжатия
Изооктан. Получение. Октановое число и степень сжатия Нефть: состав, свойства, месторождения, применение
Нефть: состав, свойства, месторождения, применение Презентация по Химии "Штучні волокна" - скачать смотреть бесплатно
Презентация по Химии "Штучні волокна" - скачать смотреть бесплатно Химия в системе современных естественнонаучных представлений
Химия в системе современных естественнонаучных представлений Алкены. Непредельные углеводороды ряда этилена
Алкены. Непредельные углеводороды ряда этилена Зымыран сұрақтар
Зымыран сұрақтар Свойства солей. Получение солей
Свойства солей. Получение солей «АТОМНАЯ ЭНЕРГЕТИКА»
«АТОМНАЯ ЭНЕРГЕТИКА» Производство серной кислоты H2SO4 « Едва найдется другое, искусственно добываемое вещество, столь часто применяемое в технике, как серная кислота…» (Д. И. Менделеев)
Производство серной кислоты H2SO4 « Едва найдется другое, искусственно добываемое вещество, столь часто применяемое в технике, как серная кислота…» (Д. И. Менделеев) Радиоактивность
Радиоактивность Основания. Простые и сложные ионы
Основания. Простые и сложные ионы Современные области применения изотопной продукции
Современные области применения изотопной продукции Хімічнi елементи
Хімічнi елементи Презентация по Химии "строение спиртов, характерные типы химических реакци" - скачать смотреть
Презентация по Химии "строение спиртов, характерные типы химических реакци" - скачать смотреть  Применение эксклюзионной хроматографии в биологии
Применение эксклюзионной хроматографии в биологии Атомный и ионный радиусы. Принципы шаровых упаковок
Атомный и ионный радиусы. Принципы шаровых упаковок Водородная связь
Водородная связь Подготовила воспитанница 11 «А» класса Кулишова Валерия
Подготовила воспитанница 11 «А» класса Кулишова Валерия Cложные липиды (липоиды)
Cложные липиды (липоиды) Очистка масляных фракций от смолистых веществ
Очистка масляных фракций от смолистых веществ Презентация по Химии "Атоми,молекули, йони, хімічні елементи, їхні назви й символи" - скачать смотреть бесплатно
Презентация по Химии "Атоми,молекули, йони, хімічні елементи, їхні назви й символи" - скачать смотреть бесплатно Подготовка к контрольной работе Химические реакции
Подготовка к контрольной работе Химические реакции Получение радиоактивных изотопов и их применение.
Получение радиоактивных изотопов и их применение. Амины. Азотсодержащие соединения
Амины. Азотсодержащие соединения Кислотность почвы
Кислотность почвы