Содержание
- 2. Инь и Ян химии Кислота Основание
- 3. Теория электролитической диссоциации: недостатки Применимо только к водным растворам, исключая: а) реакции в газовой и твердой
- 4. Протолитическая теория (1923) Кислота – донор протона, основание – акцептор протона. У каждой кислоты есть сопряженное
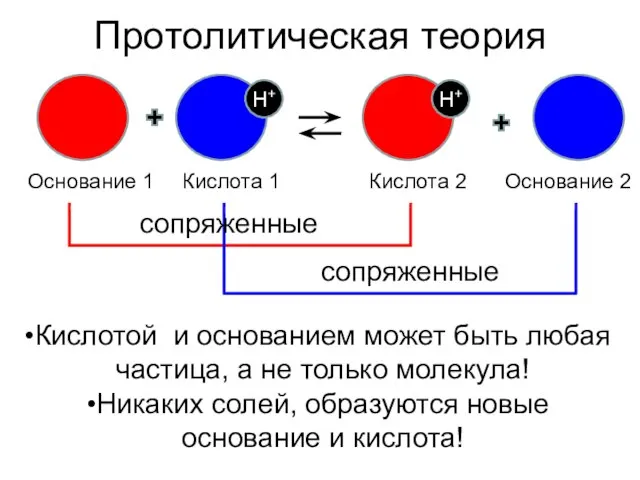
- 5. Протолитическая теория H+ H+ Основание 1 Кислота 1 Кислота 2 Основание 2 сопряженные сопряженные Кислотой и
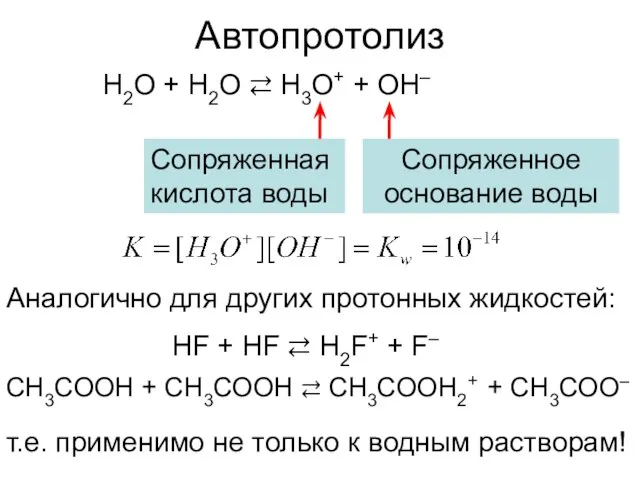
- 6. Автопротолиз H2O + H2O ⇄ H3O+ + OH– Аналогично для других протонных жидкостей: HF + HF
- 7. Константы ионизации для сопряженных кислот и оснований HF + H2O ⇄ H3O+ + F– F– +
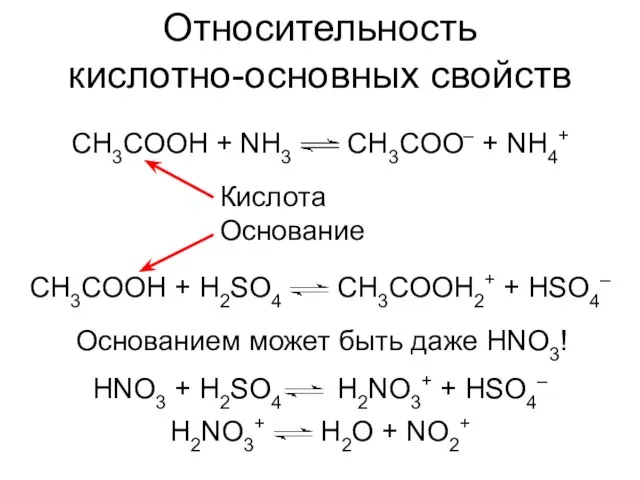
- 8. Относительность кислотно-основных свойств CH3COOH + H2SO4 CH3COOH2+ + HSO4– HNO3 + H2SO4 H2NO3+ + HSO4– Кислота
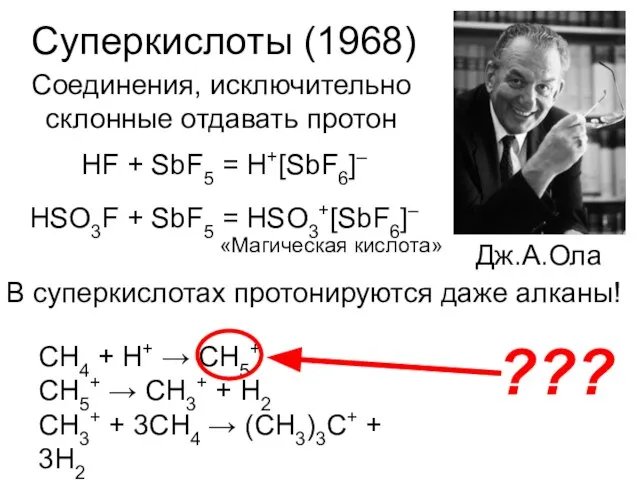
- 9. Суперкислоты (1968) Дж.А.Ола Соединения, исключительно склонные отдавать протон HF + SbF5 = H+[SbF6]– HSO3F + SbF5
- 10. Ограничения протолитической теории Неприменима к реакциям без растворителя; Неприменима к полностью апротонным (не содержащим катионов водорода
- 11. Что за вещество? Тяжелая жидкость с едким, раздражающим запахом; «Дымит» на воздухе; Бурно реагирует со щелочами
- 12. Электронная теория (1923) Кислоты – акцепторы пары электронов (имеют вакантные орбитали) Основания – доноры пары электронов
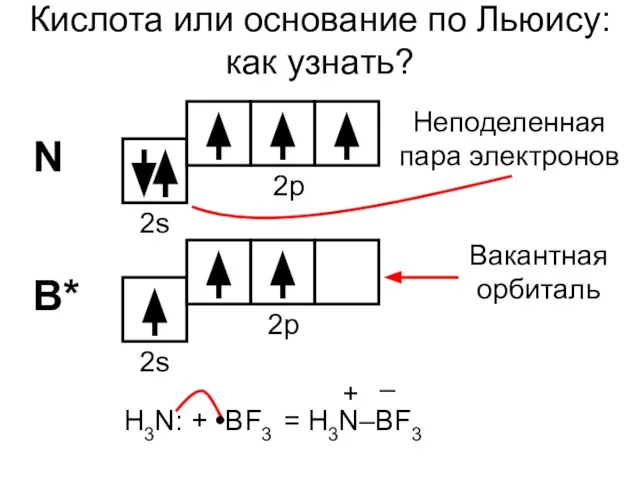
- 13. Кислота или основание по Льюису: как узнать? N B* 2s 2p 2s 2p Неподеленная пара электронов
- 14. Применение теории Льюиса Кислоты Основания AlCl3 + Cl– = [AlCl4]– Zn2+ + 4H2O = [Zn(H2O)4]2+ Химия
- 15. Ограничения теории Льюиса Не работает для некоторых протонных кислот: HF + NH3 = NH4F – но
- 16. Теория реакций в расплаве Лукса – Флуда Применяется для реакций между кислородсодержащими соединениями Хорошо описывает взаимодействия
- 17. Теория «ониевых солей» Ганча Главный признак кислотно-основной реакции – солеобразование; То, что превращается в анион –
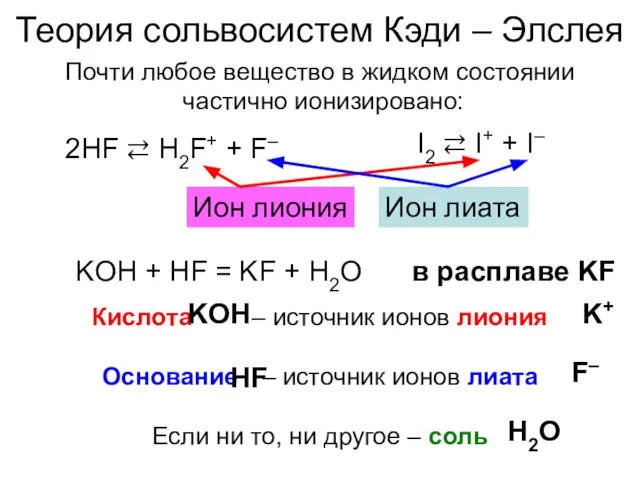
- 18. Теория сольвосистем Кэди – Элслея Почти любое вещество в жидком состоянии частично ионизировано: 2HF ⇄ H2F+
- 19. Обобщенная теория кислот и оснований Усановича (1938 г.) М.И.Усанович (1896–1981) «Кислоты и основания – это не
- 20. Теория ЖМКО: жестких и мягких кислот и оснований Пирсона (1963) Маленький радиус (объем) Высокая степень окисления
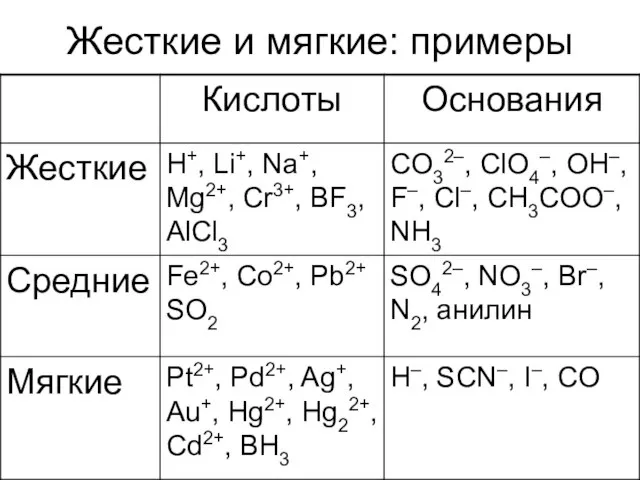
- 21. Жесткие и мягкие: примеры
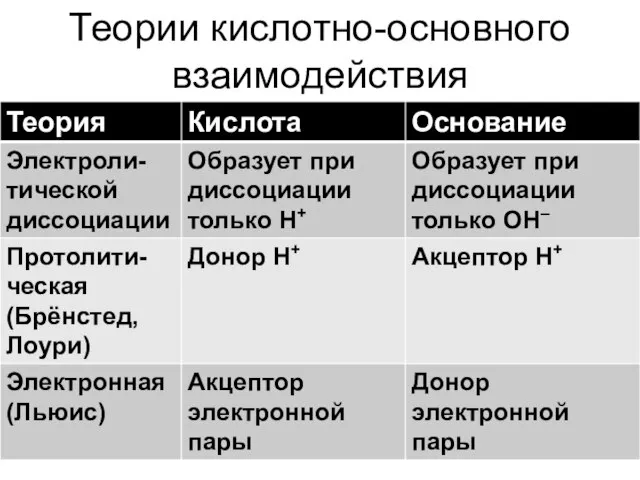
- 22. Теории кислотно-основного взаимодействия
- 24. Скачать презентацию






![Применение теории Льюиса Кислоты Основания AlCl3 + Cl– = [AlCl4]– Zn2+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/516708/slide-13.jpg)





 Фосфор. Философский камень
Фосфор. Философский камень Ақуыздардың құрылысы мен қызыметі
Ақуыздардың құрылысы мен қызыметі Additives for Polymeric Materials
Additives for Polymeric Materials Сплавы, растворы, смеси
Сплавы, растворы, смеси Презентация по Химии "Гормоны" - скачать смотреть
Презентация по Химии "Гормоны" - скачать смотреть  Формальдегід. Будова та шкідливість
Формальдегід. Будова та шкідливість Моя профессия химик-аналитик
Моя профессия химик-аналитик Хімічна промисловість www.themegallery.com
Хімічна промисловість www.themegallery.com  Электрохимические процессы
Электрохимические процессы Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Основные сведения о строении атома
Основные сведения о строении атома Презентация по Химии "Чудеса в решете" - скачать смотреть
Презентация по Химии "Чудеса в решете" - скачать смотреть  Презентация по Химии "Щавелевая кислота" - скачать смотреть
Презентация по Химии "Щавелевая кислота" - скачать смотреть  Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии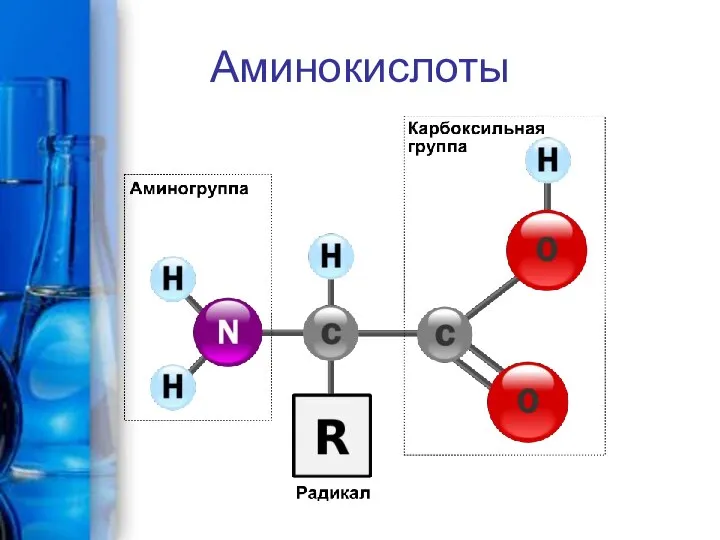 Аминокислоты и белки
Аминокислоты и белки Обмен индивидуальных аминокислот
Обмен индивидуальных аминокислот Термостабилизаторы. Доноры водорода
Термостабилизаторы. Доноры водорода Практическая работа №1. Приготовление растворов с заданной молярной концентрацией
Практическая работа №1. Приготовление растворов с заданной молярной концентрацией Предельные углеводороды
Предельные углеводороды Растворы электролитов
Растворы электролитов Детский стиральный порошок Ушастый нянь
Детский стиральный порошок Ушастый нянь Курсовая работа. Синтез адипиновой кислоты
Курсовая работа. Синтез адипиновой кислоты Реакции ионного обмена
Реакции ионного обмена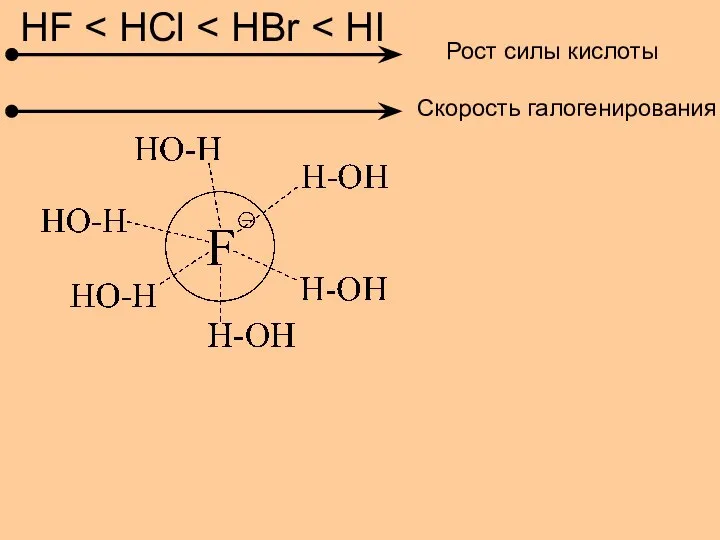 Алкены
Алкены Харчові добавки. Е-числа
Харчові добавки. Е-числа  Экстракция в аналитической химии
Экстракция в аналитической химии Алкены
Алкены Тяжелые р – элементы -полуметаллы
Тяжелые р – элементы -полуметаллы