Содержание
- 2. Н3С СООН Н3С СООН Н3С СООН 3 6 6 Н3С СООН 3 Высшие жирные кислоты ПНЖК
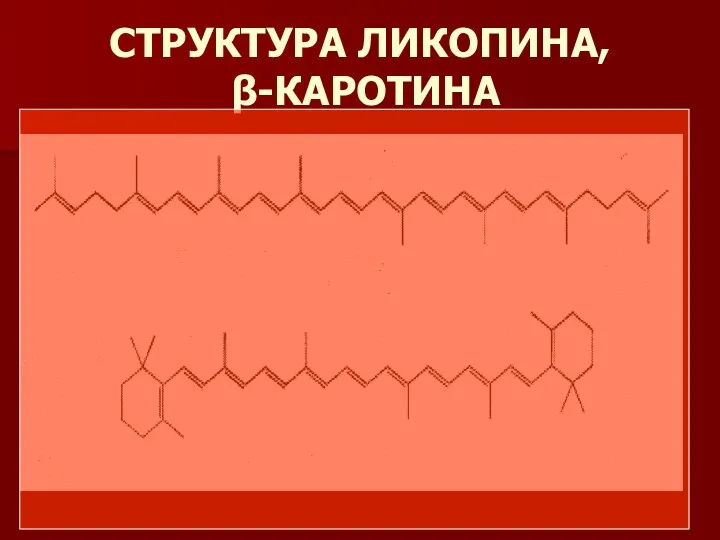
- 3. СТРУКТУРА ЛИКОПИНА, β-КАРОТИНА
- 4. ЛИКОПИН ОПРЕДЕЛЯЕТ ЦВЕТ ТОМАТОВ
- 5. Бета-каротин определяет окраску моркови
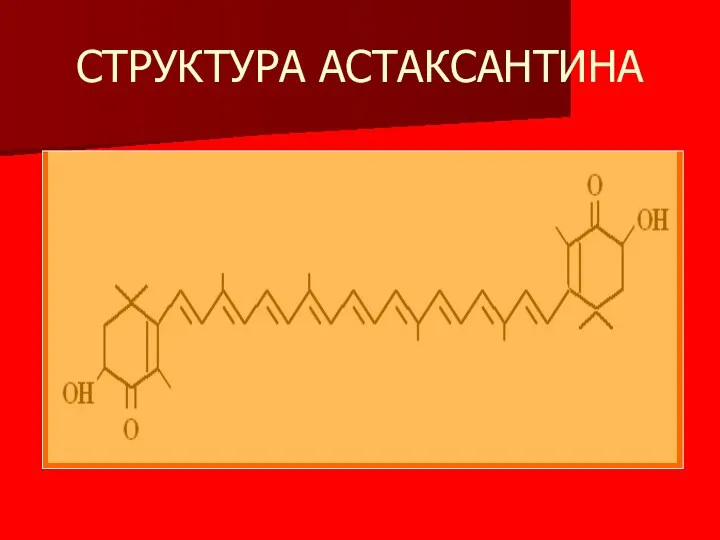
- 6. СТРУКТУРА АСТАКСАНТИНА
- 7. АСТАКСАНТИН ОПРЕДЕЛЯЕТ ОКРАСКУ КРАБОВ, КРЕВЕТОК КРАСНОЙ РЫБЫ
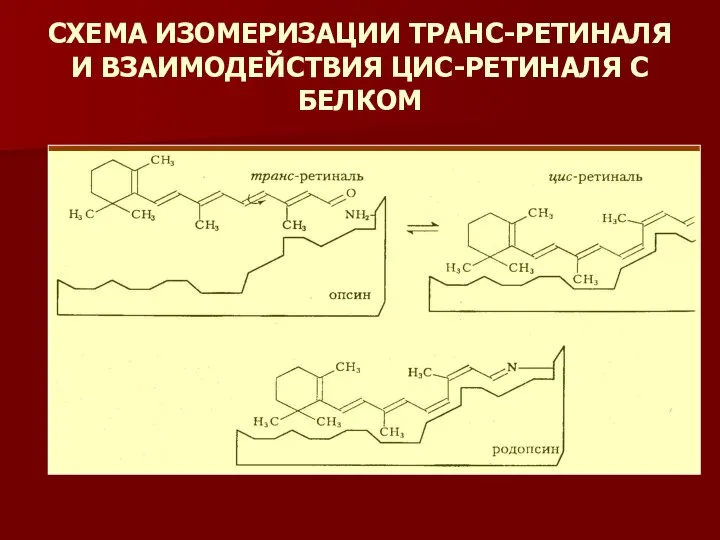
- 8. СХЕМА ИЗОМЕРИЗАЦИИ ТРАНС-РЕТИНАЛЯ И ВЗАИМОДЕЙСТВИЯ ЦИС-РЕТИНАЛЯ С БЕЛКОМ
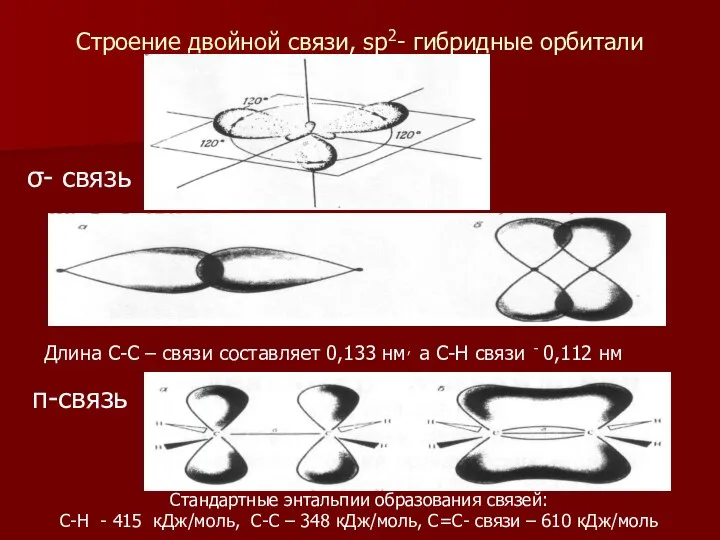
- 9. Строение двойной связи, sp2- гибридные орбитали Длина С-С – связи составляет 0,133 нм, а С-Н связи
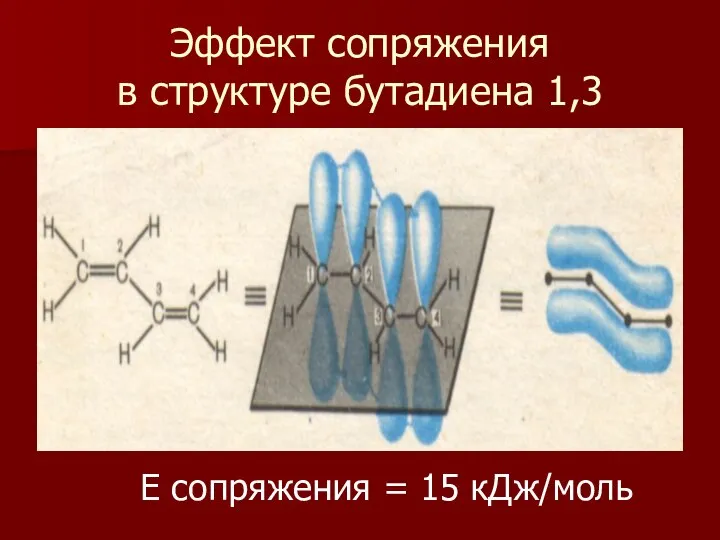
- 10. Эффект сопряжения в структуре бутадиена 1,3 Е сопряжения = 15 кДж/моль
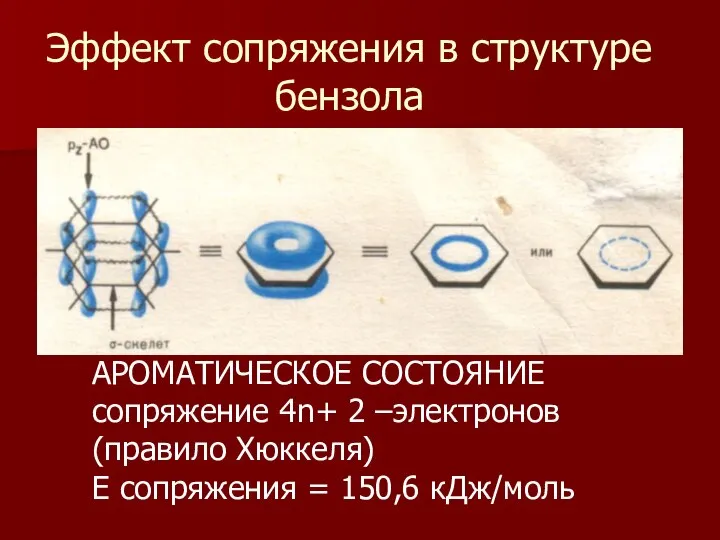
- 11. Эффект сопряжения в структуре бензола АРОМАТИЧЕСКОЕ СОСТОЯНИЕ сопряжение 4n+ 2 –электронов (правило Хюккеля) Е сопряжения =
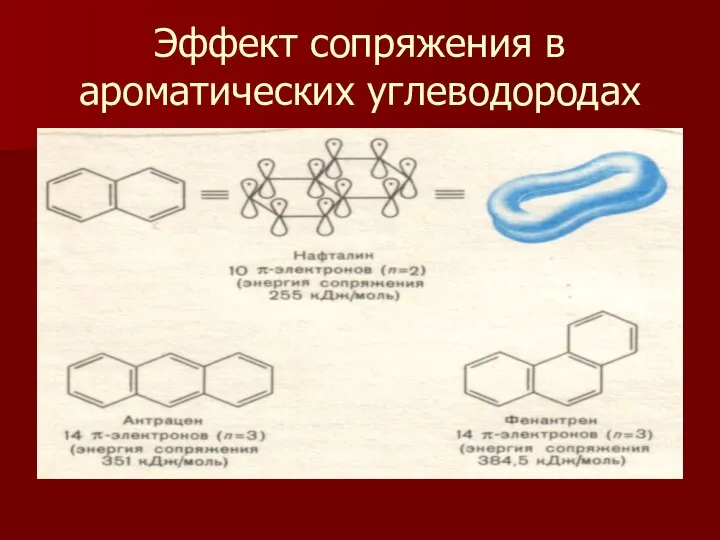
- 12. Эффект сопряжения в ароматических углеводородах
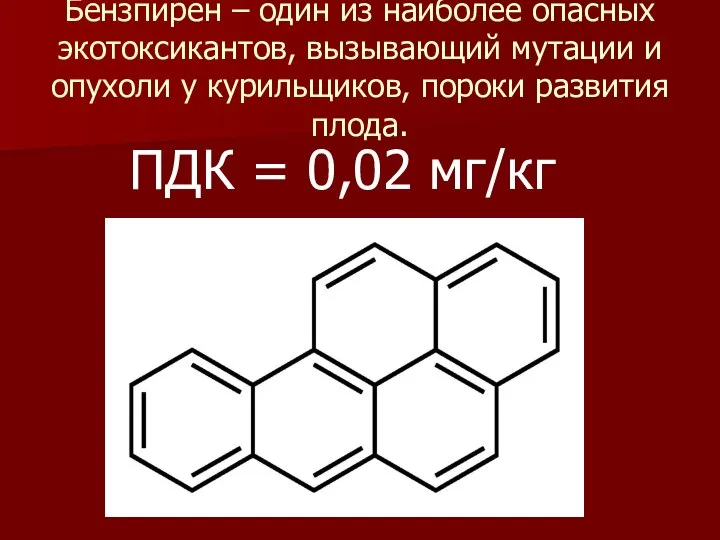
- 13. Бензпирен – один из наиболее опасных экотоксикантов, вызывающий мутации и опухоли у курильщиков, пороки развития плода.
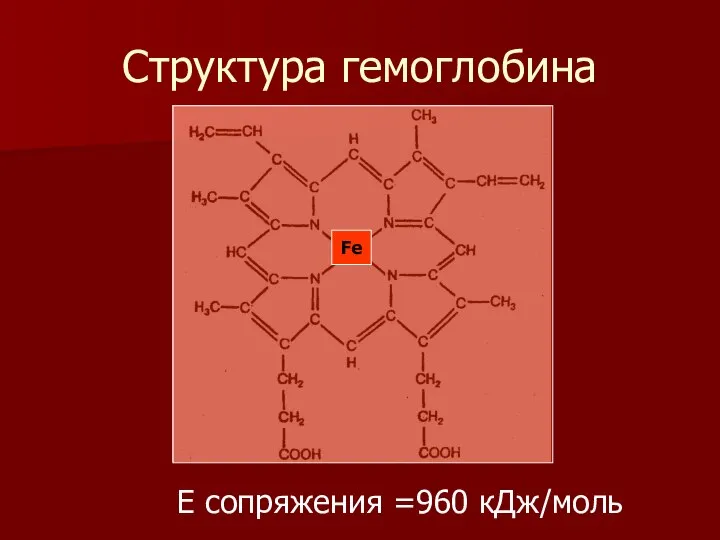
- 14. Структура гемоглобина Fe Е сопряжения =960 кДж/моль
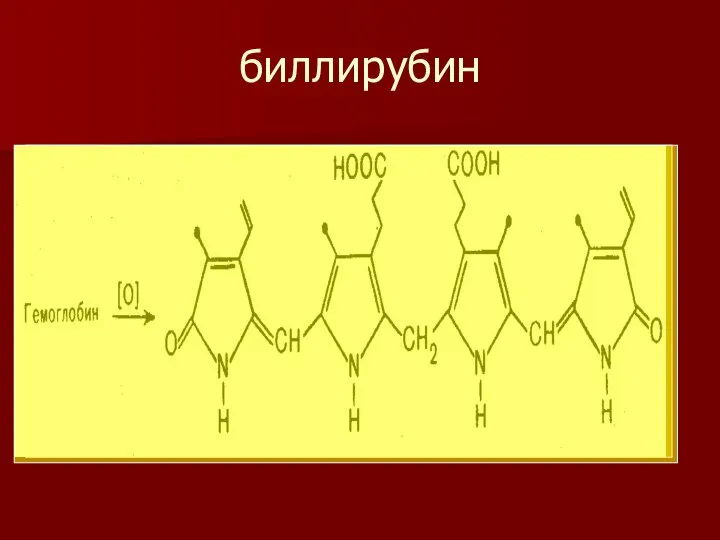
- 15. биллирубин
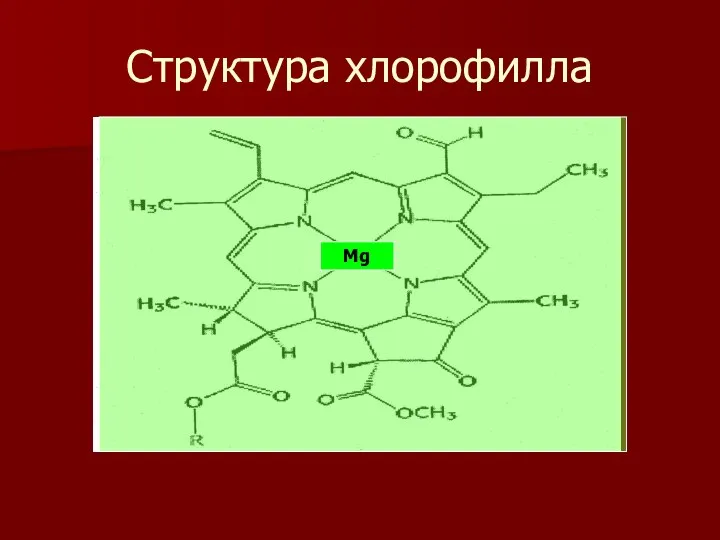
- 16. Структура хлорофилла Mg
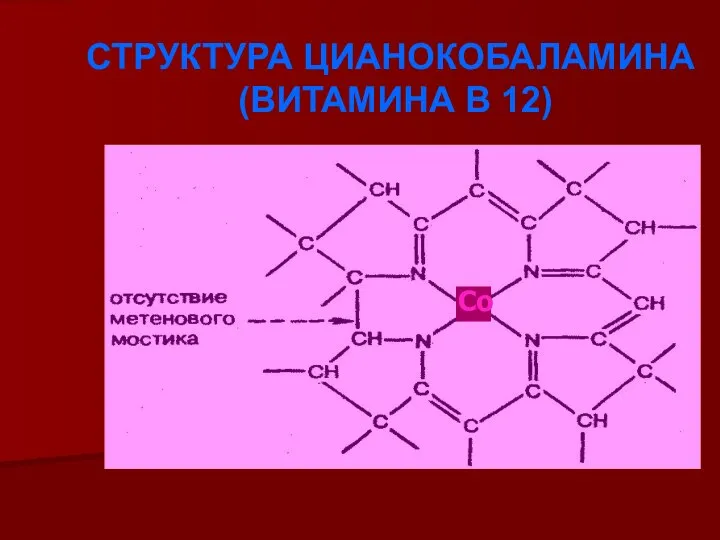
- 17. СТРУКТУРА ЦИАНОКОБАЛАМИНА (ВИТАМИНА В 12) Со
- 18. РАЗНООБРАЗИЕ ОКРАСОК,ОБУСЛОВЛЕННЫХ СОДЕРЖАНИЕМ СОПРЯЖЕННЫХ ПОЛИЕНОВ
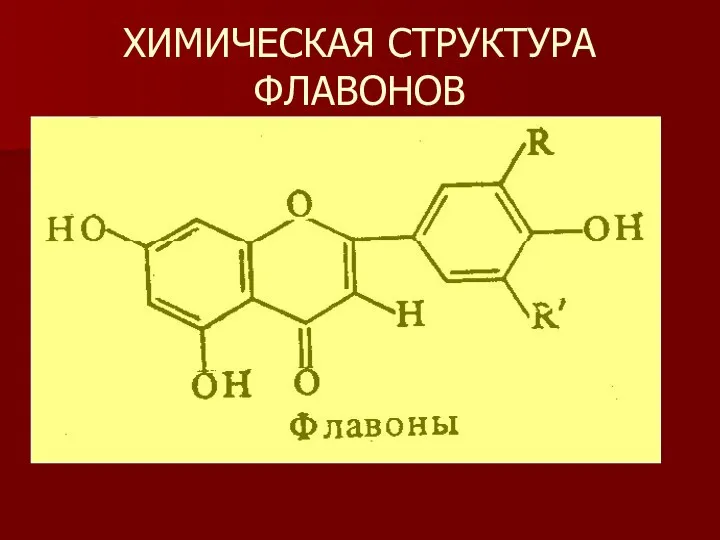
- 19. ХИМИЧЕСКАЯ СТРУКТУРА ФЛАВОНОВ
- 21. Понятие реакционного центра. В ходе биохимических и химических процессов превращению подвергается не вся молекула, а лишь
- 22. Типы разрыва связи Свободнорадикальные частицы образуются при гомолитическом разрыве ковалентной связи Е •|• Y → E•
- 23. Природа активных частиц Свободнорадикальные частицы (имеют неспаренный или валентный электрон) (ОH•, Br •,Cl •, CH3 •,
- 24. Классификация химических реакций 1. По результату химического взаимодействия. Различают реакции замещения, присоединения, элиминирования, окисления, восстановления, кислотно-основные
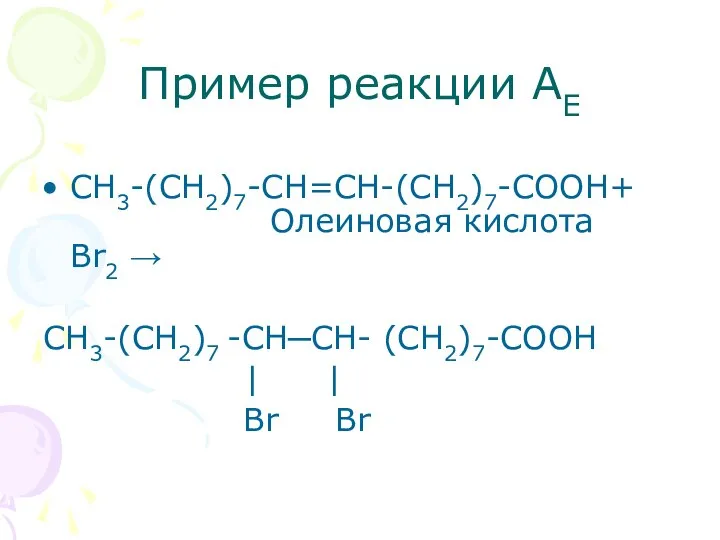
- 25. Пример реакции АЕ СН3-(СН2)7-СН=СН-(СН2)7-СООН+ Олеиновая кислота Br2 → СН3-(СН2)7 -СН─СН- (СН2)7-СООН | | Br Br
- 26. Реакции электрофильного присоединения Субстратом реакций AE являются алкены, алкины, реакции протекают по реакционному центру, представляющему собой
- 27. ВЗАИМНОЕ ВЛИЯНИЕ АТОМОВ В МОЛЕКУЛАХ БИООРГАНИЧЕСКИХ СОЕДИНЕНИЙ ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ (Лайнус Поллинг, 1932 г.) Электроотрицательность – это способность
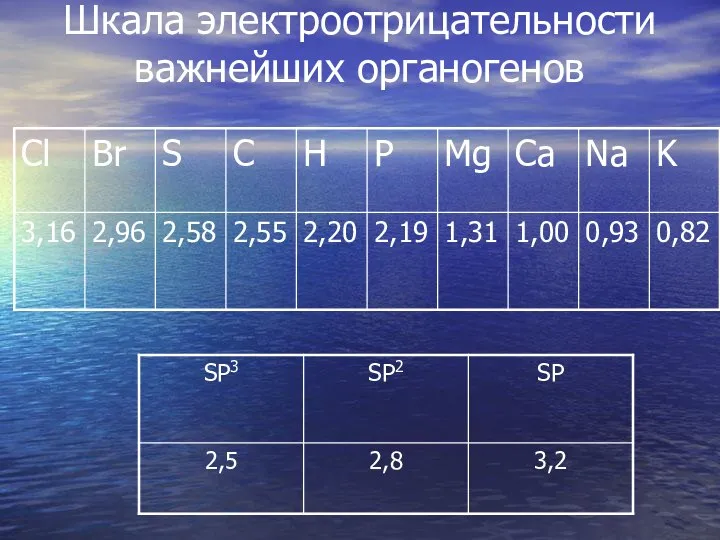
- 28. Шкала электроотрицательности важнейших органогенов
- 29. ИНДУКТИВНЫЙ ЭФФЕКТ Смещение электронной плотности по цепи σ-связей под влиянием заместителя называется индуктивным эффектом ( J
- 30. Электронные индуктивные эффекты заместителей δ+++ δ++ δ+ δ- -J : R-CH2→CH2→CH2→X X= -OH; -NO2; –COOH; -
- 31. МЕЗОМЕРНЫЙ ЭФФЕКТ Мезомерным эффектом называют передачу влияния заместителя в сопряженной системе (смещение электронной плотности в системе
- 32. ПРИРОДА ЗАМЕСТИТЕЛЕЙ Заместители, повышающие электронную плотность в сопряженной системе, проявляют положительный мезомерный эффект, + М, называются
- 33. Природа заместителей Заместители, оттягивающие электронную плотность из сопряженной системы, проявляют отрицательный мезомерный эффект, -М, называются ЭЛЕКТРОНОАКЦЕПТОРАМИ
- 34. Лекция № 2 КИСЛОТНЫЕ И ОСНОВНЫЕ СВОЙСТВА БИООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 35. Кислотность и основность - важные свойства соединений, определяющие их фундаментальные физико-химические и биологические свойства. Ферментативные реакции
- 36. Кислотно-основные взаимодействия А-Н + :В ↔ А- + В-Н кислота основание сопряженное сопряженная основание кислота По
- 37. [НСОО-]×[Н3О+] К= [НСООН]×[Н2О] Ка = К×[Н2О] [НСОО-]×[Н3О+] Ка= [НСООН]
- 38. Чем ниже кислотность, тем выше рКа Ка = 1,75×10-5 рКа = -lg Ка = 4,75
- 39. КИСЛОТНОСТЬ И ОСНОВНОСТЬ СВЯЗАНЫ СО ВЗАИМНЫМ ВЛИЯНИЕМ АТОМОВ В МОЛЕКУЛАХ БИООРГАНИЧЕСКИХ СОЕДИНЕНИЙ, с понятием ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ (Лайнус
- 40. Сила кислоты определяется стабильностью образующихся ионов, которая определяется: 1.Электроотрицательнью элементов
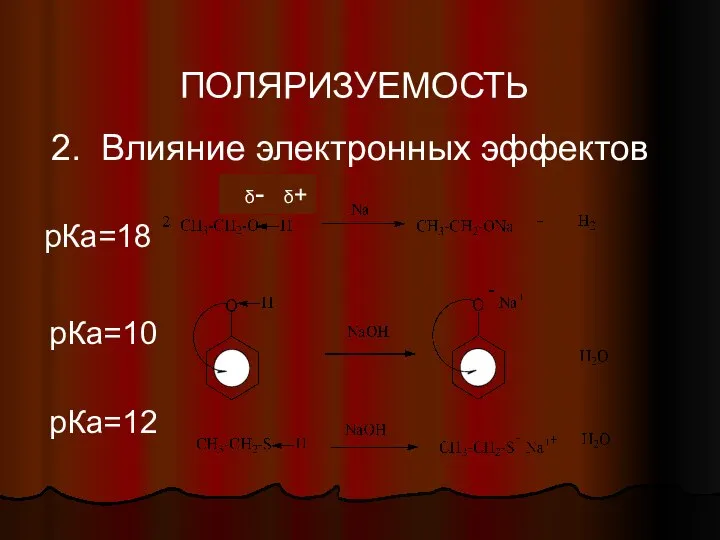
- 41. ПОЛЯРИЗУЕМОСТЬ 2. Влияние электронных эффектов δ- δ+ рКа=18 рКа=10 рКа=12
- 42. Поляризуемость Для S-H кислот преобладающим фактором является поляризуемость. Атомы серы больше по размеру и имеют вакантные
- 43. Кислотность тиолов выше, чем кислотность спиртов R-S-H + NaOH → R-S-Na + H2O R-O-H + NaOH
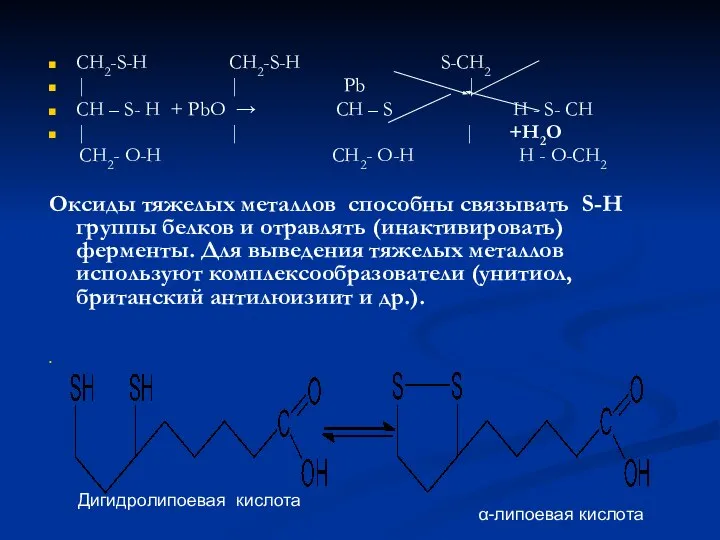
- 44. CH2-S-H CH2-S-H S-CH2 | | Pb | CH – S- H + PbO → CH –
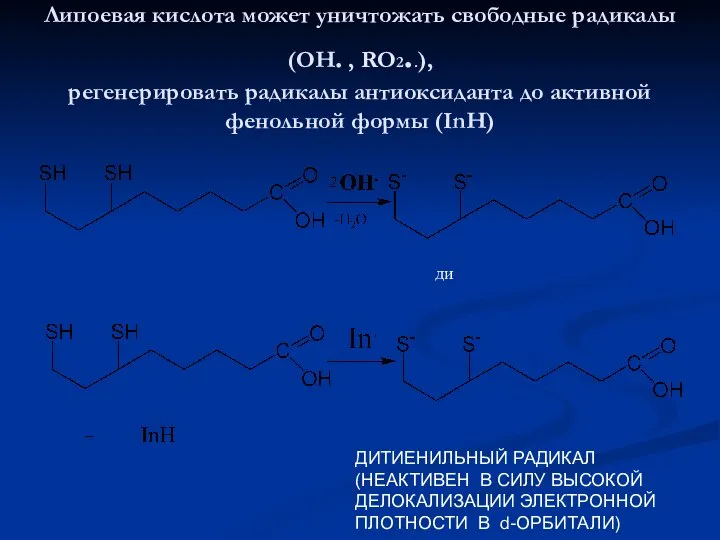
- 45. Липоевая кислота может уничтожать свободные радикалы (ОН. , RO2..), регенерировать радикалы антиоксиданта до активной фенольной формы
- 46. Атомы хлора выполняют роль электроноакцепторов ( - J ) СCl3←СООН > Cl←СH2 ←СООН >СH3→СООН pKa =
- 47. Основность –способность принимать и удерживать протоны Для образования ковалентной связи с протоном Н+ органические основания должны
- 48. Сравнительная оценка основных свойств Величина основности определяется теми же факторами, что и кислотность, но действие этих
- 49. Основания образуют соли с кислотами CH3→ NH2 + HCl → [CH3→ N+H3 ] Cl- хлорид метиламмония
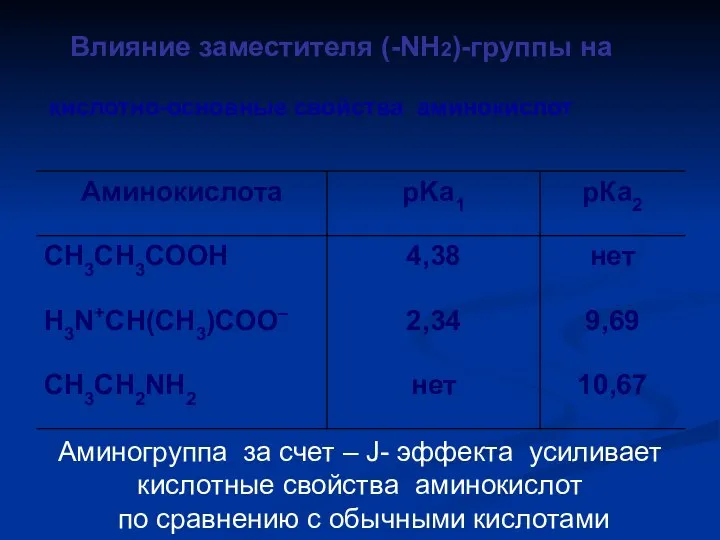
- 50. кислотно-основные свойства аминокислот Влияние заместителя (-NH2)-группы на Аминогруппа за счет – J- эффекта усиливает кислотные свойства
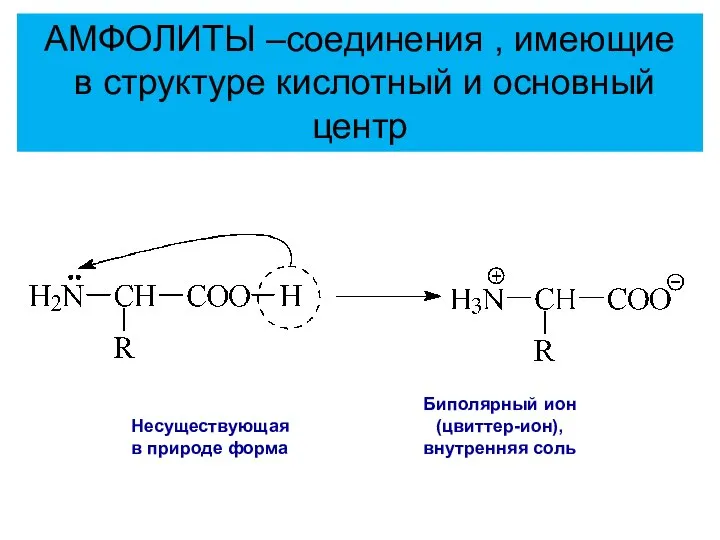
- 51. Несуществующая в природе форма Биполярный ион (цвиттер-ион), внутренняя соль АМФОЛИТЫ –соединения , имеющие в структуре кислотный
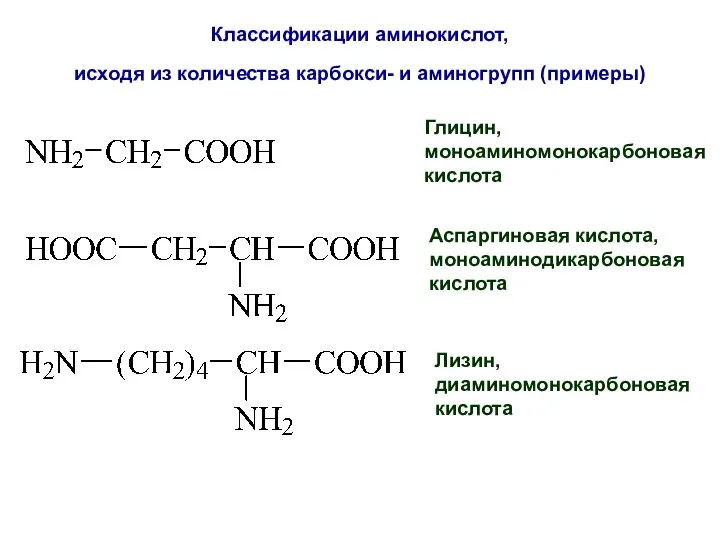
- 52. Классификации аминокислот, исходя из количества карбокси- и аминогрупп (примеры) Глицин, моноаминомонокарбоновая кислота Аспаргиновая кислота, моноаминодикарбоновая кислота
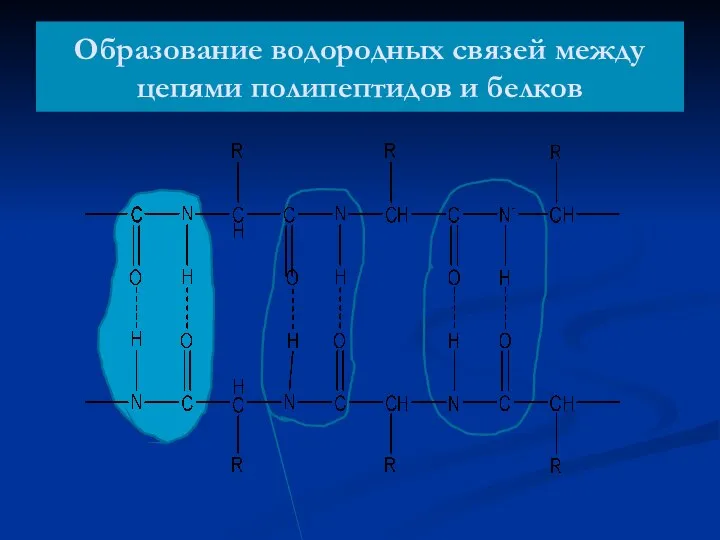
- 53. Образование водородных связей между цепями полипептидов и белков
- 55. Скачать презентацию




















![[НСОО-]×[Н3О+] К= [НСООН]×[Н2О] Ка = К×[Н2О] [НСОО-]×[Н3О+] Ка= [НСООН]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396159/slide-36.jpg)









 Углерод. Химические свойства
Углерод. Химические свойства Применение серной кислоты
Применение серной кислоты СПИРТЫ Урок химии в 9-10 классе
СПИРТЫ Урок химии в 9-10 классе Органические производные пятивалентного фосфора. Способы получения
Органические производные пятивалентного фосфора. Способы получения Многоатомные спирты
Многоатомные спирты Органическая химия. Углеводы. Свойства, получение, применение. Основные представители
Органическая химия. Углеводы. Свойства, получение, применение. Основные представители Вода Презентацию подготовила ученица 8-б класса Гордеева Юлия
Вода Презентацию подготовила ученица 8-б класса Гордеева Юлия Карбонаты и фосфаты
Карбонаты и фосфаты Каталитический крекинг
Каталитический крекинг Алкены
Алкены Теория строения органических соединений
Теория строения органических соединений Биологически важные гетероциклы
Биологически важные гетероциклы Аттестационная работа. Образовательная программа внеурочной деятельности «Химия и физика с детства». (1-4 класс)
Аттестационная работа. Образовательная программа внеурочной деятельности «Химия и физика с детства». (1-4 класс) Растворы Электролитическая диссоциация
Растворы Электролитическая диссоциация  Гомологи аренов
Гомологи аренов Производные индола
Производные индола Облик и габитус кристаллов
Облик и габитус кристаллов Крахмал. Физические свойства
Крахмал. Физические свойства Алкандар. (қаныққан көмірсутектер)
Алкандар. (қаныққан көмірсутектер) Симметрия кристаллических решеток
Симметрия кристаллических решеток Водород. Растворы. 8 класс
Водород. Растворы. 8 класс Твердоконтактные электрохимические платформы для потенциометрических измерений
Твердоконтактные электрохимические платформы для потенциометрических измерений Интерпретация вещественного состава магматических горных пород
Интерпретация вещественного состава магматических горных пород Многоатомные спирты
Многоатомные спирты Акцепторы нейтральных молекул. Клатраты
Акцепторы нейтральных молекул. Клатраты Строение вещества. Химические элементы
Строение вещества. Химические элементы Коллоидное состояние вещества
Коллоидное состояние вещества Основы органической химии
Основы органической химии