Содержание
- 2. Актуальность Элементы, необходимые для построения и жизнедеятельности клеток и организмов, называют биогенными элементами. К жизненно необходимым
- 3. Актуальность Основу всех живых систем составляют шесть элементов: углерод, водород, кислород, азот, фосфор, сера, получивших название
- 4. Цель лекции Показать подход для изучения свойств биогенных элементов, исходя из представления об электронном строении атома
- 5. План лекции Актуальность темы Электронные конфигурации атомов биогенных элементов Гибридизация атомных орбиталей Ковалентные связи σ- и
- 6. Атомная орбиталь (АО) АО - это область пространства в окрестности ядра, где имеется максимальная вероятность (95
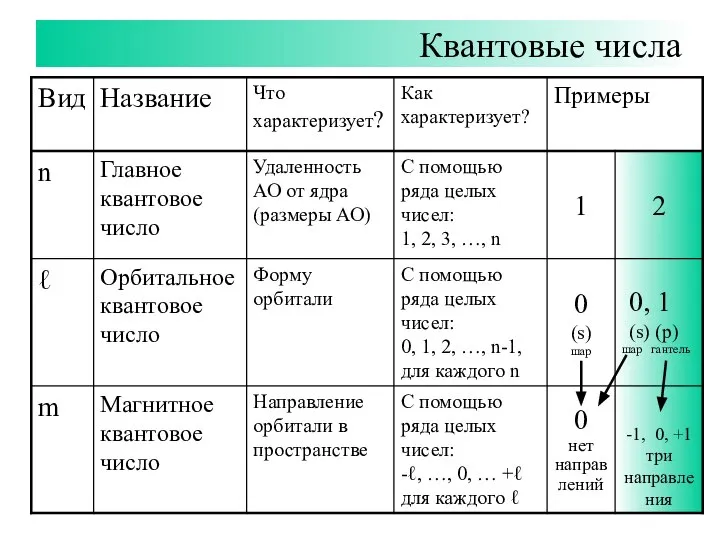
- 7. Квантовые числа
- 8. Энергетическая схема орбиталей
- 9. Заселение орбиталей электронами – в соответствии с тремя принципами Принцип Паули (запрет Паули) Принцип Гунда (запрет
- 10. Принцип наименьшей энергии (правило Клечковского) Электроны заселяют орбитали так, чтобы их общая энергия была минимальной. Общая
- 11. Проскоки (провалы) электронов При заселении d (или f)-орбиталей устойчивым считается состояние, при котором эти d (или
- 12. Примеры проскоков Так, у атома хрома, согласно принципам заселения, электронная конфигурация внешнего валентного уровня должна была
- 13. продолжаем Аналогично, электронная конфигурация внешнего валентного уровня атома меди должна быть Cu – 3d94s2. На самом
- 14. Валентные электроны Валентные электроны – это электроны внешнего уровня и незавершенного предвнешнего подуровня. Именно эти электроны
- 15. Конфигурации валентных электронов атома также определяются положением элемента в таблице Менделеева. При этом используются: - номер
- 16. Примеры: С – 2s22p2 n = 2 p-элемент, 2-я позиция, IV-группа
- 17. N – 2s22p3 P - 3s23p3
- 18. Са – 4s2 Са2+ – (4s0) АО валентного уровня вакантны и могут принимать атомы – доноры
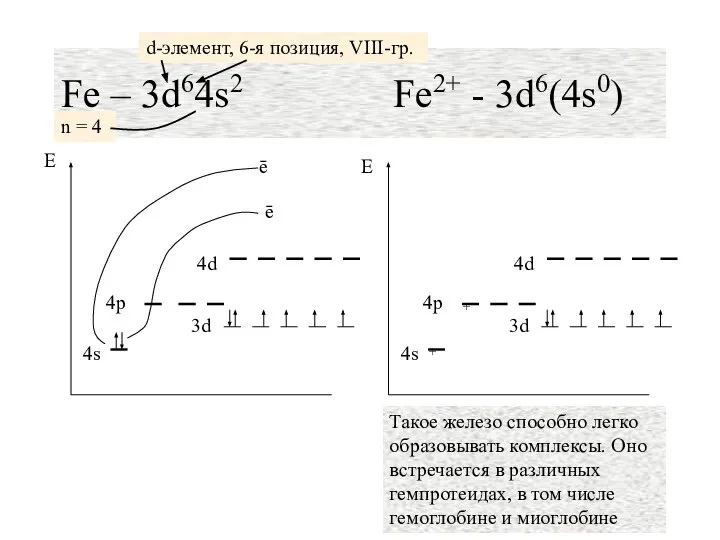
- 19. Fe – 3d64s2 Fe2+ - 3d6(4s0) n = 4 d-элемент, 6-я позиция, VIII-гр.
- 20. Химическая связь Это электростатическое взаимодействие между атомами с участием валентных электронов, сопровождающее выделением энергии от 20
- 21. Ⅰ группа Ⅱ группа Ионная Ковалентная Металлическая Ионная связь возникает между двумя противоположно заряженными частицами –
- 22. Ковалентная связь Это связь с помощью пары электронов, общих для обоих атомов. Причина образования ковалентной связи
- 23. Метод ВС Ковалентная связь образуется путем перекрывания двух валентных АО атомов-партнеров так, что в общее пользование
- 24. продолжаем Если же в перекрывание вступает двухэлектронная АО одного атома и вакантная АО другого атома, то
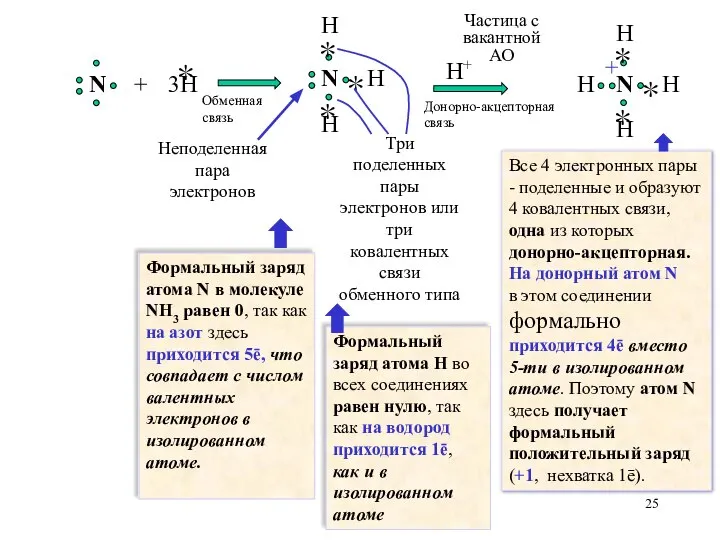
- 25. H Неподеленная пара электронов Три поделенных пары электронов или три ковалентных связи обменного типа Частица с
- 26. Итак, образование донорно-акцепторной связи в катионе аммония, в отличие от образования обменной связи, приводит к изменению
- 27. Можно привести ещё один пример Формальный заряд атома Cl в молекуле AlCl3 равен также 0, так
- 28. Гибридизация АО Гибридизация – это смешивание АО разной формы, а значит и энергии (в пределах валентного
- 29. Наиболее распространенные типы гибридизации АО
- 30. Рис. 3. Энергетическая схема гибридизации АО элементов второго периода (В, С, N, О, F ) Е
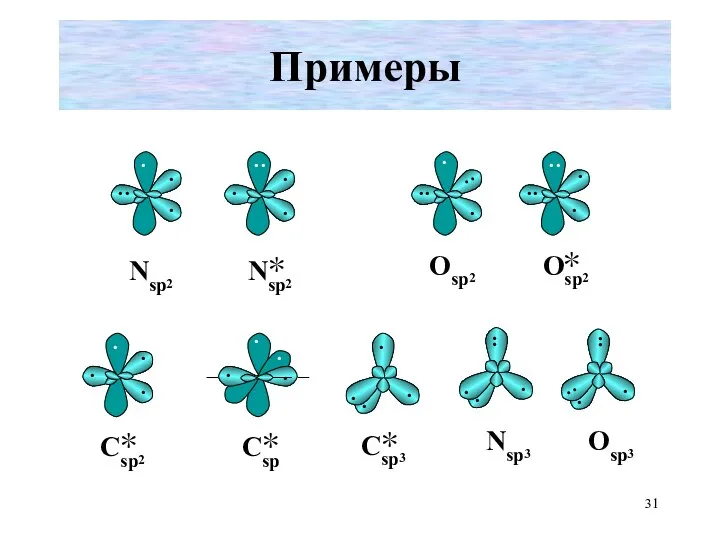
- 31. Примеры
- 32. Где встречаются такие атомы? Для прогнозирования структуры молекул на основе заданной гибридизации атомов можно воспользоваться несколькими
- 33. Однако при определенных условиях несвязывающие АО могут вступить в связь : При наличии в окружающей среде
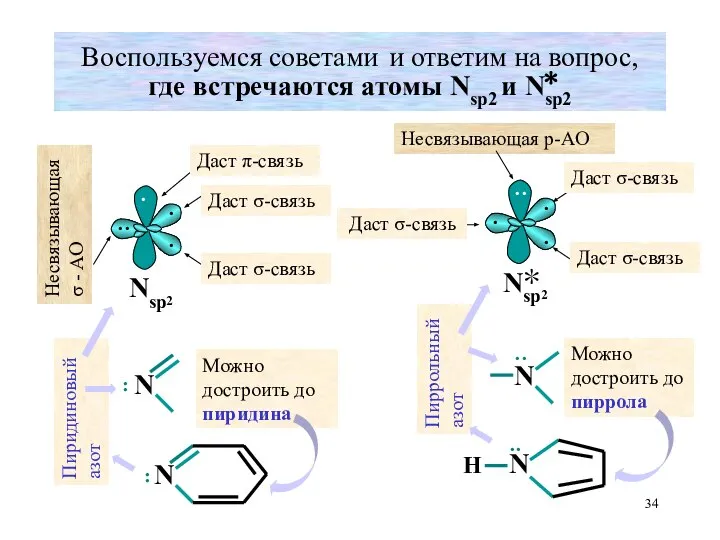
- 34. Воспользуемся советами и ответим на вопрос, где встречаются атомы Nsp2 и Nsp2 · · ·· ·
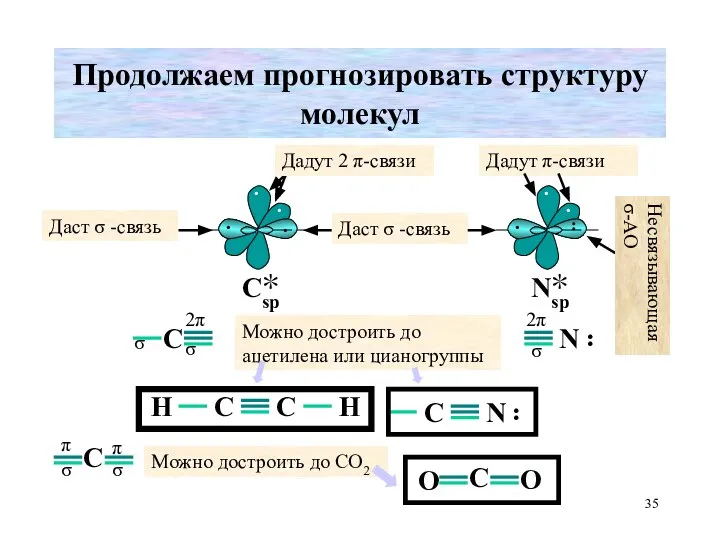
- 35. Продолжаем прогнозировать структуру молекул Дадут 2 π-связи Даст σ -связь Даст σ -связь Можно достроить до
- 36. Определение типа гибридизации Тип гибридизации атома в молекуле определяют с помощью различных спектральных методов. Однако в
- 37. Под объектами понимают Число соседних атомов (партнёров) Число свободных (неподеленных никаким образом) электронных пар Электронная пара
- 38. Примеры атомов со свободными электронными парами Свободные электронные пары атомов азота, кислорода, серы (будут находиться на
- 39. В противном случае, т.е. если ни один из критериев не проходит, имеющаяся у атома электронная пара
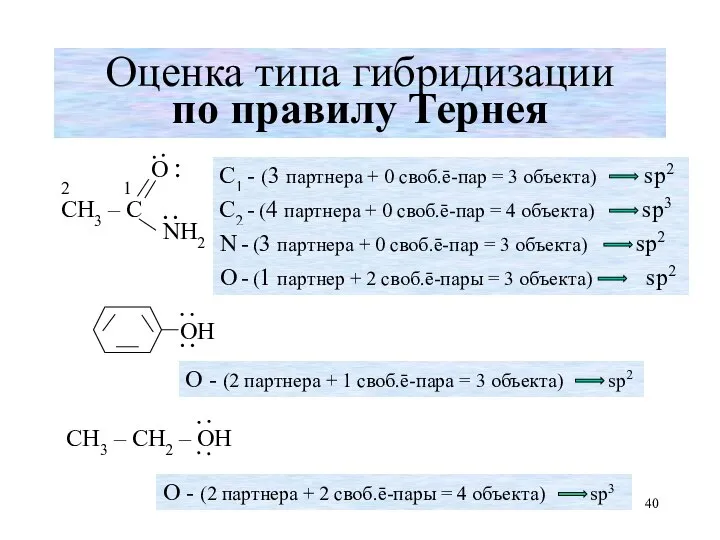
- 40. Оценка типа гибридизации по правилу Тернея ∙ ∙
- 41. Ковалентные связи σ- и π-типа В зависимости от способа и симметрии перекрывания АО ковалентные связи бывают
- 42. продолжаем π-Связь образуется при боковом перекрывании р-АО и имеет плоскость симметрии, проходящую через линию, соединяющую ядра
- 43. # Встречается и другой тип π-связи – c боковым перекрыванием орбиталей p – d ; d
- 44. Общие свойства ковалентной связи В отличие от большинства других типов связей, ковалентная связь характеризуется: Высокой прочностью
- 45. Основные выводы Большинство биогенных элементов сосредоточено в трех первых периодах таблицы Менделеева. По положению их в
- 46. Литература Основная: Слесарев В.И. – Химия: Основы химии живого: Учебник для вузов.– 3-е изд., испр. –
- 47. Литература Дополнительная: Грандберг И.И. – Органическая химия: Учеб. Для студ. вузов, обучающихся по агроном. спец. –
- 48. Внимание! Приготовиться к вопросу Пиррол Пирролидин Пиридин Пиперидин
- 50. Скачать презентацию








































 Серная кислота. (9 класс)
Серная кислота. (9 класс) Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Atomic number, Mass number and Isotopes
Atomic number, Mass number and Isotopes Ароматические углеводороды
Ароматические углеводороды Каталитикалық крекинг
Каталитикалық крекинг Аттестационная работа. Проектно-исследовательская деятельность учащихся на уроках химии и во внеурочной работе
Аттестационная работа. Проектно-исследовательская деятельность учащихся на уроках химии и во внеурочной работе Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Характеристика элементов VI-В группы. Хром
Характеристика элементов VI-В группы. Хром Строение атома. Периодичность свойств элементов и их соединений
Строение атома. Периодичность свойств элементов и их соединений Вольфрам және молибден
Вольфрам және молибден КРАХМАЛ и ЦЕЛЛЮЛОЗА (С6Н10О5)n
КРАХМАЛ и ЦЕЛЛЮЛОЗА (С6Н10О5)n  Ш. Мәрҗани исемендәге Комыргуҗа урта мәктәбе Физика укытучысы Шәрәфетдинова Р.З. 2012 ел
Ш. Мәрҗани исемендәге Комыргуҗа урта мәктәбе Физика укытучысы Шәрәфетдинова Р.З. 2012 ел Познаваемость мира. Сведения о клетке. Подготовила ученица 11 класса Шапаренко Екатерина
Познаваемость мира. Сведения о клетке. Подготовила ученица 11 класса Шапаренко Екатерина Химия элементов IVA группы
Химия элементов IVA группы Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия
Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия Органическое топливо. Теплота сгорания топлива
Органическое топливо. Теплота сгорания топлива Химические свойства и получение алканов
Химические свойства и получение алканов Кислород и его применение
Кислород и его применение Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Алюминий және оның қосылыстары
Алюминий және оның қосылыстары Кремний и его соединения
Кремний и его соединения Характеристика металу Ферум
Характеристика металу Ферум Виды присадок к моторному топливу. Керосин
Виды присадок к моторному топливу. Керосин Предмет химии. Вещества и их физические свойства. (8 класс)
Предмет химии. Вещества и их физические свойства. (8 класс)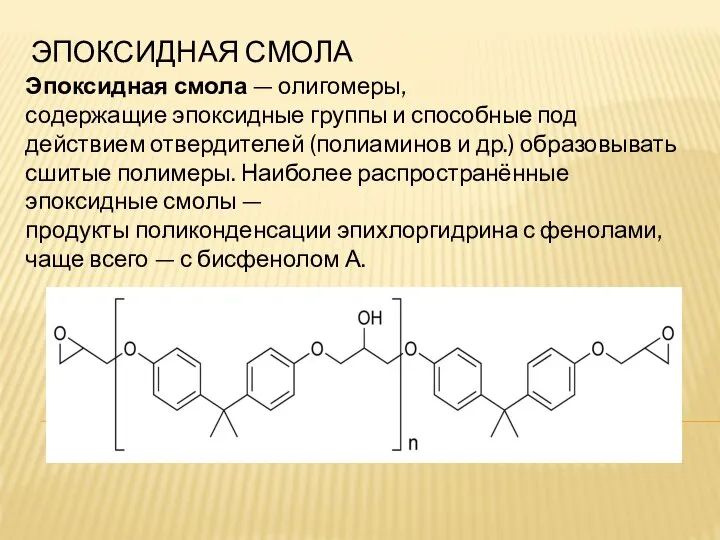 Эпоксидная смола
Эпоксидная смола Материя и цвет. Свет
Материя и цвет. Свет Способы выражения состава раствора. Решение задач
Способы выражения состава раствора. Решение задач Метаболизм источников энергии
Метаболизм источников энергии