Содержание
- 2. Качественные реакции в биохимии Реакции на углеводы
- 3. Качественная реакция на углеводы (и все прочие гликоли) Образование хелатных комплексов с медью-II в щелочной среде
- 4. Выявление восстанавливающих сахаров Альдозы при смешении с щелочным раствором гидроксида меди-II дают желтый, а затем оранжевый
- 5. Гидролиз олиго- и полисахараидов Сахароза и крахмал в кислой среде расщепляются при нагревании до мономеров. (C6H10O5)n
- 6. Качественные реакции в биохимии Реакции на белки
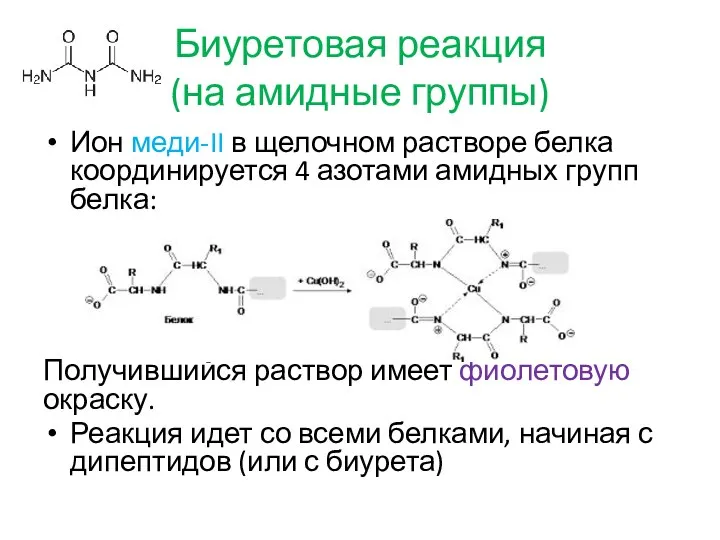
- 7. Биуретовая реакция (на амидные группы) Ион меди-II в щелочном растворе белка координируется 4 азотами амидных групп
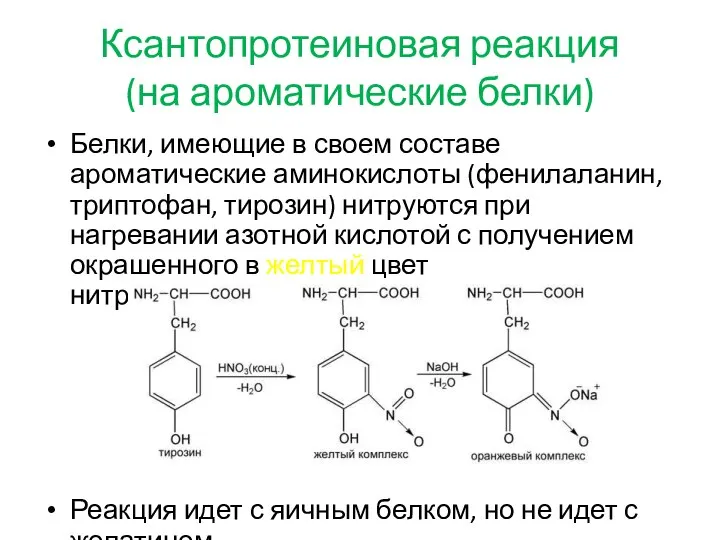
- 8. Ксантопротеиновая реакция (на ароматические белки) Белки, имеющие в своем составе ароматические аминокислоты (фенилаланин, триптофан, тирозин) нитруются
- 9. Выявление серосодержащих белков Белки, в состав которых входят серосодержащие аминокислоты (цистеин, метионин), при взаимодействии с щелочным
- 10. Осаждение белка Белки осаждаются без денатурации в разных условиях: При нагревании белка вблизи изоэлектрической точки; При
- 11. Качественные реакции в органической химии Различение органических кислот
- 12. Различение органических кислот, дающих нерастворимые осадки Некоторые анионы органических кислоты способны давать нерастворимые осадки с ионами
- 13. Окисление органических кислот гидроксидом меди-II Муравьиная кислота является не только кислотой, но и альдегидом. Потому ей
- 14. Качественные реакции в органической химии Проба на фенолы
- 15. Бромирование фенолов Растворы фенолов реагируют с бромной водой с образованием малорастворимых производных. В случае с фенолом
- 17. Скачать презентацию












 Electrochemistry. (Chapter 6)
Electrochemistry. (Chapter 6) Биологическое окисление
Биологическое окисление Химические реакции. Физические и химические явления
Химические реакции. Физические и химические явления Химическая связь. Метод молекулярных орбиталей
Химическая связь. Метод молекулярных орбиталей Химия и здоровье человека
Химия и здоровье человека Электролитическая диссоциация
Электролитическая диссоциация Металлы и сплавы -материал для древних и современных олимпийских наград.
Металлы и сплавы -материал для древних и современных олимпийских наград. Презентация к уроку химии по теме «Спирты» 10 класс. УМК Габриеляна О.С. Базовый уровень
Презентация к уроку химии по теме «Спирты» 10 класс. УМК Габриеляна О.С. Базовый уровень Семейства химических элементов. Периодический закон Д.И. Менделеева
Семейства химических элементов. Периодический закон Д.И. Менделеева Производные 8-замещенных хинолина
Производные 8-замещенных хинолина Лабораторное оборудование, посуда и средства защиты Разработка для проведения практических работ по химии подготовила Нерев
Лабораторное оборудование, посуда и средства защиты Разработка для проведения практических работ по химии подготовила Нерев Органическая химия
Органическая химия Гормоны и адаптация. (Лекция 15)
Гормоны и адаптация. (Лекция 15) Физико-химические основы разделения горючих ископаемых и продуктов их переработки. Хроматография
Физико-химические основы разделения горючих ископаемых и продуктов их переработки. Хроматография Элементы титан и хром
Элементы титан и хром Синтетические моющие средства
Синтетические моющие средства Базовое нефтехимическое сырье. Углеводородные газы
Базовое нефтехимическое сырье. Углеводородные газы Окислительно-восстановительные потенциалы (электродные потенциалы)
Окислительно-восстановительные потенциалы (электродные потенциалы) Виды изомерии у моносахаридов
Виды изомерии у моносахаридов Тесты по неорганической химии
Тесты по неорганической химии Определение прочности куриного яйца (с разным цветом скорлупы: белые и коричневые)
Определение прочности куриного яйца (с разным цветом скорлупы: белые и коричневые) Физико-химические основы получения лекарственных препаратов. Лекция 2
Физико-химические основы получения лекарственных препаратов. Лекция 2 Organic molecules
Organic molecules Руды металлов Виртуальная коллекция
Руды металлов Виртуальная коллекция  Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура
Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть
Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть  Изменение агрегатного состояния вещества. Двигатели внутреннего сгорания
Изменение агрегатного состояния вещества. Двигатели внутреннего сгорания Презентация по Химии "Металлическая связь" - скачать смотреть
Презентация по Химии "Металлическая связь" - скачать смотреть