Содержание
- 2. Метод молекулярных орбиталей (МО) наиболее нагляден в его графической модели линейной комбинации атомных орбиталей (ЛКАО). Метод
- 3. Перекрываются атомные орбитали, близкие по энергии. В результате перекрывания двух атомных орбиталей образуются две молекулярные. Одна
- 4. Молекулярная орбиталь, не участвующая в образовании химической связи, носит название несвязывающей. Ее энергия равна энергии исходной
- 5. Применим метод МО ЛКАО и разберем строение молекулы водорода. Изобразим на двух параллельных диаграммах энергетические уровни
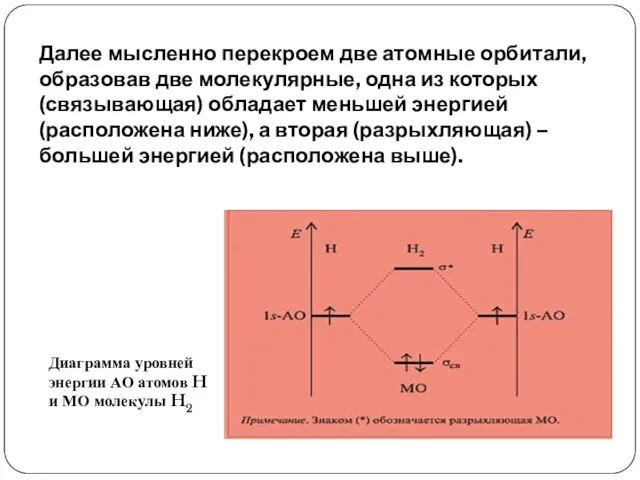
- 6. Далее мысленно перекроем две атомные орбитали, образовав две молекулярные, одна из которых (связывающая) обладает меньшей энергией
- 7. Видно, что имеется выигрыш в энергии по сравнению с несвязанными атомами. Свою энергию понизили оба электрона,
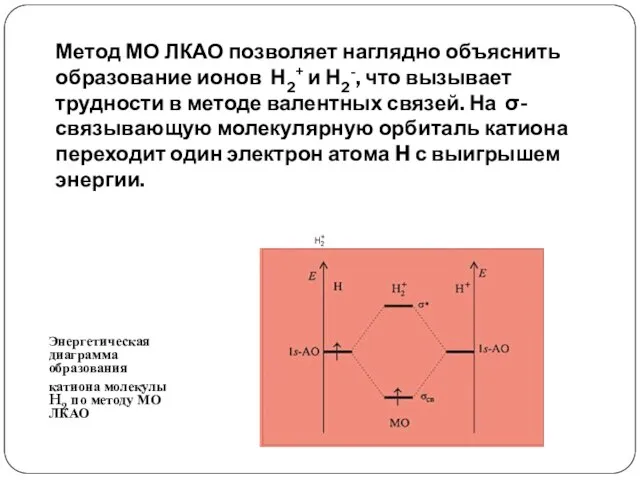
- 8. Метод МО ЛКАО позволяет наглядно объяснить образование ионов Н2+ и Н2-, что вызывает трудности в методе
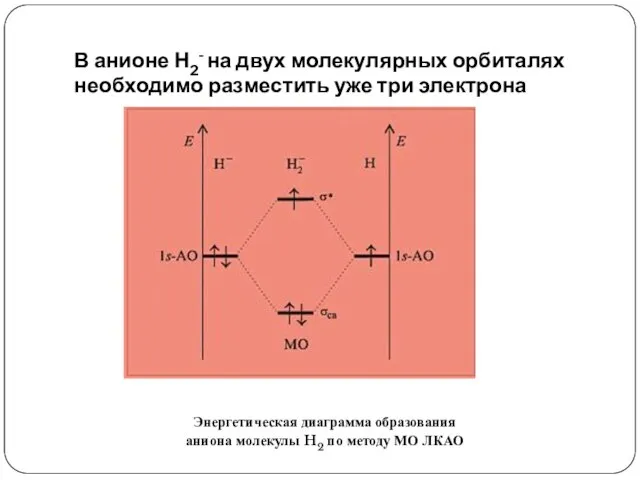
- 9. В анионе Н2- на двух молекулярных орбиталях необходимо разместить уже три электрона Энергетическая диаграмма образования аниона
- 10. Если два электрона, опустившись на связывающую орбиталь, дают выигрыш в энергии, то третьему электрону приходится повысить
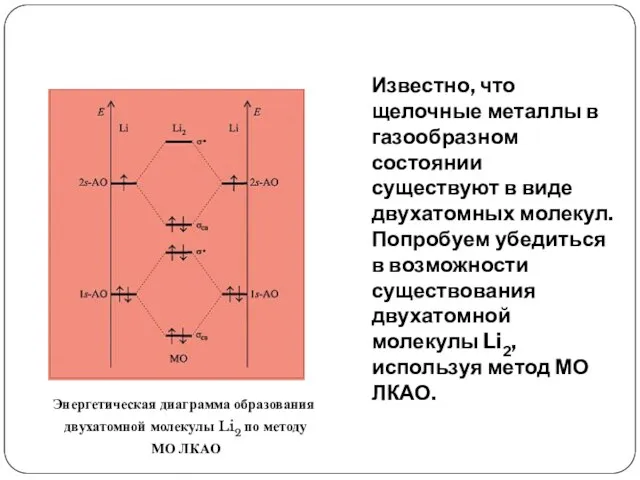
- 11. Известно, что щелочные металлы в газообразном состоянии существуют в виде двухатомных молекул. Попробуем убедиться в возможности
- 12. Перекрывание валентных 2s-орбиталей атомов лития приведет также к образованию одной σ-связывающей и одной разрыхляющей молекулярных орбиталей.
- 13. Перекрывание одинаковых 1s-орбиталей атомов лития даст две молекулярные орбитали (связывающую и разрыхляющую), которые согласно принципу минимума
- 14. Используя метод МО ЛКАО, рассмотрим возможность образования молекулы He2 . Энергетическая диаграмма, иллюстрирующая с помощью метода
- 15. В этом случае два электрона займут связывающую молекулярную орбиталь, а два других – разрыхляющую. Выигрыша в
- 16. Методом МО ЛКАО легко продемонстрировать парамагнитные свойства молекулы кислорода. С тем чтобы не загромождать рисунок, не
- 17. Перекрывание p-АО, направленных вдоль оси x -связи Перекрывание p-АО, направленных вдоль оси y (z), с образованием
- 18. Энергетическая диаграмма, иллюстрирующая с помощью метода МО ЛКАО парамагнитные свойства молекулы O2
- 19. Среди молекулярных орбиталей молекулы кислорода, образовавшихся в результате перекрывания p-АО, две π-связывающие вырожденные (с одинаковой энергией)
- 20. Среди двухатомных молекул одной из наиболее прочных является молекула CO. Метод МО ЛКАО легко позволяет объяснить
- 21. Результатом перекрывания p-орбиталей атомов O и C является образование двух вырожденных π-связывающих и одной – σ
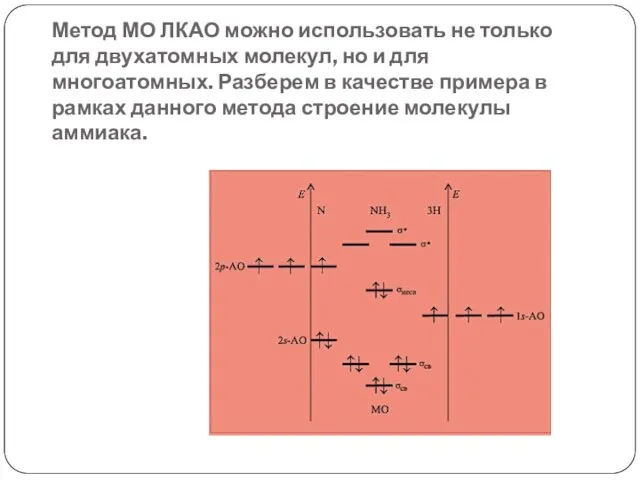
- 22. Метод МО ЛКАО можно использовать не только для двухатомных молекул, но и для многоатомных. Разберем в
- 23. Поскольку три атома водорода имеют только три 1s-орбитали, то суммарное число образованных молекулярных орбиталей будет равно
- 24. Вопросы и задания
- 25. 1. Какие виды связей можно отнести к химическим? 2. Какие два основных подхода к рассмотрению химической
- 26. 5. Что такое электроотрицательность? Из каких данных электроотрицательность рассчитывается? О чем электроотрицательности атомов, образующих химическую связь,
- 28. Скачать презентацию



















 Генетика. Лекция 5 Генотип. Геном. Кариотип. Геномные мутации. Генный баланс. Компенсация доз генов. Эволюция генома.
Генетика. Лекция 5 Генотип. Геном. Кариотип. Геномные мутации. Генный баланс. Компенсация доз генов. Эволюция генома.  Мыс. Мыс көзі
Мыс. Мыс көзі Какое свойство кожуры апельсина помогает держать его на поверхности воды
Какое свойство кожуры апельсина помогает держать его на поверхности воды Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Порфирины. Производные порфина. (Лекция 14)
Порфирины. Производные порфина. (Лекция 14) Жиры и масла Выполнила ученица 10 «А» класса Кобылкина Яна
Жиры и масла Выполнила ученица 10 «А» класса Кобылкина Яна  Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура
Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура Презентация по Химии "Химическая связь" - скачать смотреть бесплатно
Презентация по Химии "Химическая связь" - скачать смотреть бесплатно Хімічні методи підвищення продуктивності свердловини
Хімічні методи підвищення продуктивності свердловини Введение. Теория строения органических соединений А.М.Бутлерова. Лекция 1-2
Введение. Теория строения органических соединений А.М.Бутлерова. Лекция 1-2 Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Простые вещества - металлы
Простые вещества - металлы Дисперсная система
Дисперсная система Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Анодные реакции коррозионного процесса
Анодные реакции коррозионного процесса Химия и биохимия игристых вин
Химия и биохимия игристых вин Истрия развития химии
Истрия развития химии Группа нефелиновых сиенитов-фонолитов
Группа нефелиновых сиенитов-фонолитов Производные пиррозилидина. (Лекция 6)
Производные пиррозилидина. (Лекция 6) Введение в экологическую токсикологию
Введение в экологическую токсикологию Физическая и коллоидная химия
Физическая и коллоидная химия Геология полезных ископаемых
Геология полезных ископаемых Среднее (полное) общее образование. Химия. Изучение химии на профильном уровне
Среднее (полное) общее образование. Химия. Изучение химии на профильном уровне Предельные углеводороды
Предельные углеводороды Гліцерин. Загальні відомості про гліцерин
Гліцерин. Загальні відомості про гліцерин Определение валентности элементов
Определение валентности элементов Лужноземельні елементи. Фізичні та хімічні властивості простих речовин та сполук, що вони утворюють
Лужноземельні елементи. Фізичні та хімічні властивості простих речовин та сполук, що вони утворюють Подготовила воспитанница 11 «А» класса Кулишова Валерия
Подготовила воспитанница 11 «А» класса Кулишова Валерия