Презентация по химии «СОЛИ» Выполнил: ученик 8 А класса МОУ - лицея № 4 имени Героя России Горшкова Д. Е. г. Тулы Чуваев Сергей Юр
Содержание
- 2. Соли – вещества, состоящие из атомов металла, соединённых c кислотным остатком. Общая формула класса: MenAm
- 3. Классификация солей В зависимости от состава соли бывают: 1. Средние – продукт полного замещения водорода в
- 4. Классификация солей 3. Основные – продукт неполного замещения групп OH- основания на кислотный остаток. Mg(OH)2 +
- 5. Классификация солей 5. Смешанные – состоящие из общего металла и различных кислотных остатков. CuOHNO3 + CH3COOH
- 6. Получение солей Соли получают при химическом взаимодействии соединений различных классов и простых веществ. Отметим важнейшие способы
- 7. Получение солей 1. Реакция нейтрализации: Ca(OH)2 + H2CO3 = = CaCO3 + 2H2O карбонат кальция
- 8. Получение солей 2. Взаимодействие металлов с неметаллами: 2Al + 3S = Al2S3 сульфид алюминия
- 9. Получение солей 3. Взаимодействие металлов с кислотами: Zn + 2HCl = ZnCl2 + H2 хлорид цинка
- 10. Получение солей 4. Взаимодействие основных оксидов с кислотными оксидами. CaO + SiO2 = CaSiO3 силикат кальция
- 11. Физические свойства солей Соли, за небольшим исключением, являются твёрдыми кристал-лическими веществами различного цвета. По растворимости в
- 12. Химические свойства солей Соли взаимодействуют: C простыми веществами – металлами и неметаллами. со сложными – кислотами,
- 13. Химические свойства солей 1. С металлами: CuSO4 + Fe = FeSO4 + Cu сульфат меди (II)
- 14. Химические свойства солей 3. С кислотами: 2NaCl + H2SO4 = хлорид натрия = Na2SO4 + 2HCl
- 15. Химические свойства солей 4. С щелочами: FeCl2 + 2NaOH = хлорид железа (II) =Fe(OH)2 + 2NaCl
- 16. Химические свойства солей 5. С солями: AgNO3 + KCl = нитрат серебра =AgCl + KNO3 хлорид
- 18. Скачать презентацию















 Связующие ЭКС
Связующие ЭКС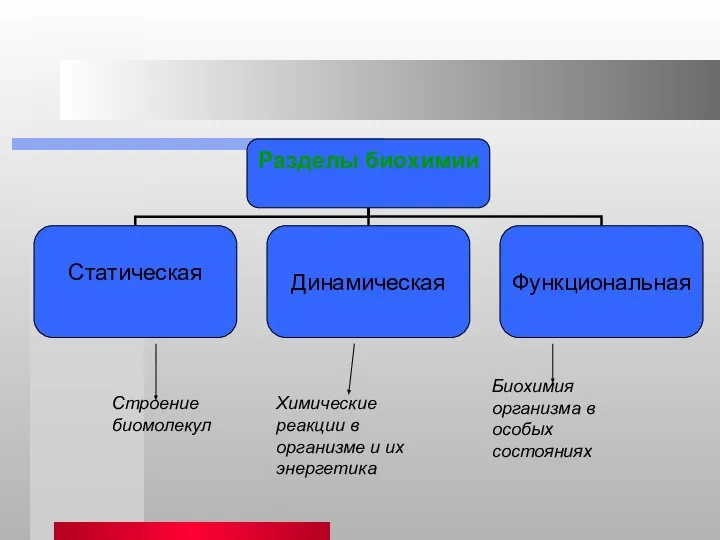 Разделы и основные понятия биохимии
Разделы и основные понятия биохимии Химия и пища. Маркировка, упаковка пищевых и гигиенических продуктов
Химия и пища. Маркировка, упаковка пищевых и гигиенических продуктов Презентация по Химии "Форфор" - скачать смотреть
Презентация по Химии "Форфор" - скачать смотреть  Ցեմենտի արտադրություն
Ցեմենտի արտադրություն Вопросительное местоимение КТО
Вопросительное местоимение КТО Особенности строения ионных кристаллов. Постоянная Моделунга. Энергия кристаллической решётки. Цикл Борна-Габера
Особенности строения ионных кристаллов. Постоянная Моделунга. Энергия кристаллической решётки. Цикл Борна-Габера Ниобий. Физиологическое действие
Ниобий. Физиологическое действие Origin of petroleum dilemma
Origin of petroleum dilemma Фармацевтическая разработка липосомального крема с экстрактами лопуха войлочного и крапивы двудомной для укрепления волос
Фармацевтическая разработка липосомального крема с экстрактами лопуха войлочного и крапивы двудомной для укрепления волос Характеристика ПМ общетехнического, инженерного и констркуционного назначения
Характеристика ПМ общетехнического, инженерного и констркуционного назначения Нанотехнологии и науки о материалах
Нанотехнологии и науки о материалах Анализ смеси веществ. (Лекция 6)
Анализ смеси веществ. (Лекция 6) Растворы
Растворы Неорганические соединения серы
Неорганические соединения серы Фенолы. Номенклатура фенолов
Фенолы. Номенклатура фенолов Презентация по Химии "Кислород" - скачать смотреть
Презентация по Химии "Кислород" - скачать смотреть  Деятельность лабораторий контроля химических факторов. Внедрение политики импортозамещения
Деятельность лабораторий контроля химических факторов. Внедрение политики импортозамещения Химический состав клетки. Неорганические соединения
Химический состав клетки. Неорганические соединения Алкалоиды
Алкалоиды Суды залалсыздандыру әдістері
Суды залалсыздандыру әдістері Презентация по Химии "Древняя и античная химия" - скачать смотреть
Презентация по Химии "Древняя и античная химия" - скачать смотреть  Очистка поверхности медного сплава
Очистка поверхности медного сплава Загальна характеристика рослинних кормiв. (Тема 1)
Загальна характеристика рослинних кормiв. (Тема 1) Дюралюминий. Дюраль
Дюралюминий. Дюраль Производство серной кислоты H2SO4
Производство серной кислоты H2SO4 Пластические массы
Пластические массы Непредельные углеводороды. Алкены. 9 класс
Непредельные углеводороды. Алкены. 9 класс