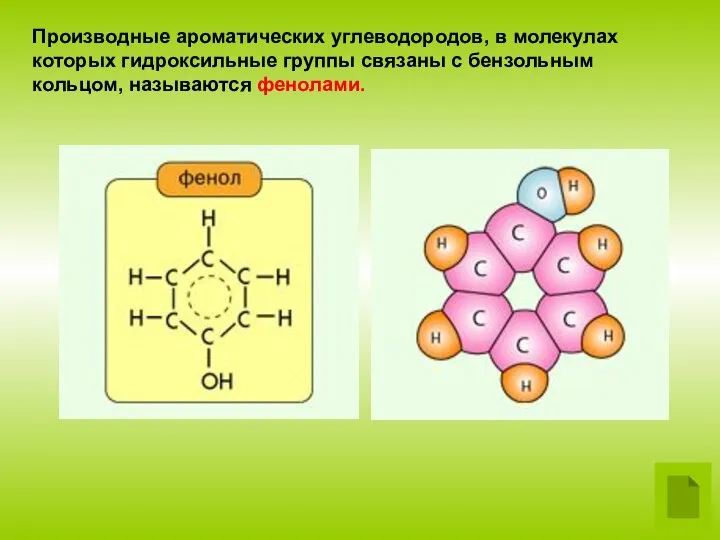
Реакции фенола по бензольному кольцу
Гидроксильная группа фенола повышает электронную плотность
в
бензольном кольце, особенно, в орто- и пара-положениях
(+М-эффект ОН-группы).
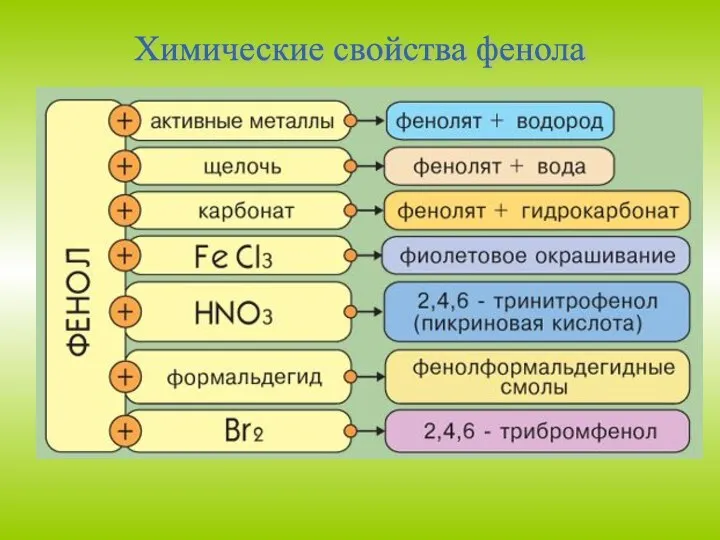
Поэтому фенол значительно активнее бензола вступает в реакции
электрофильного замещения (SE) в ароматическом кольце.
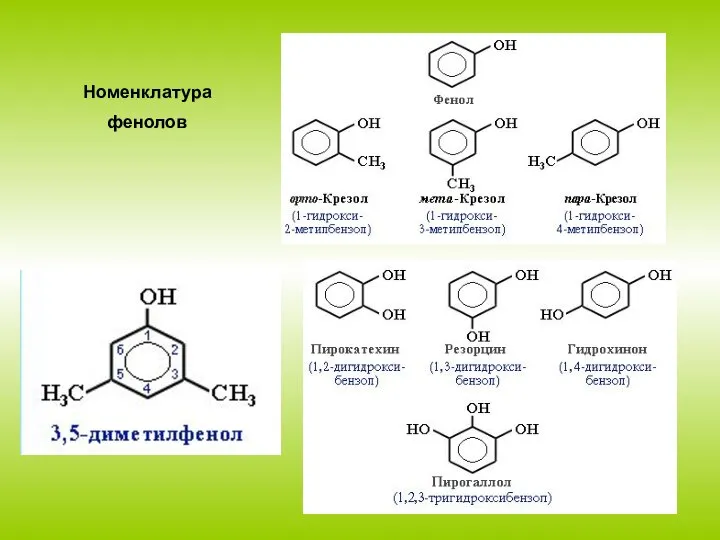
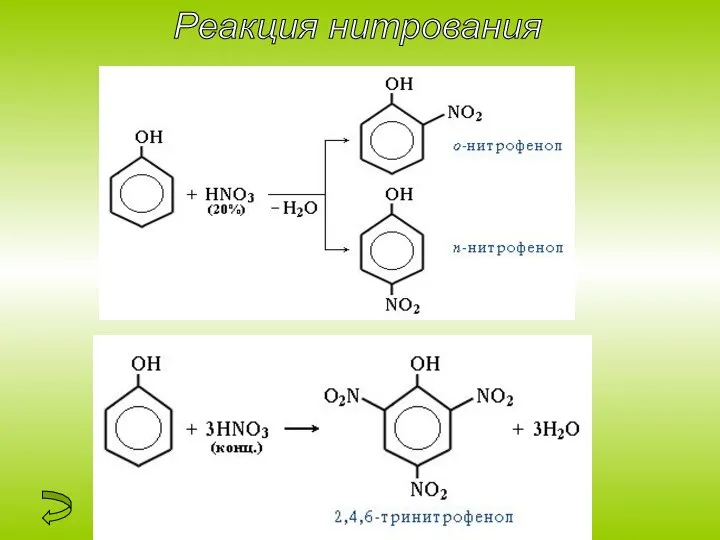
1. Нитрование. Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов .
При использовании концентрированной HNO3 образуется 2,4,6-
тринитрофенол (пикриновая кислота)
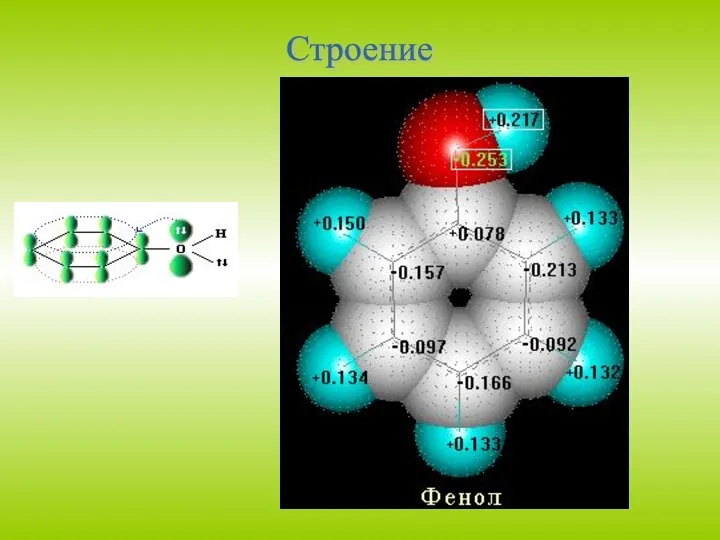
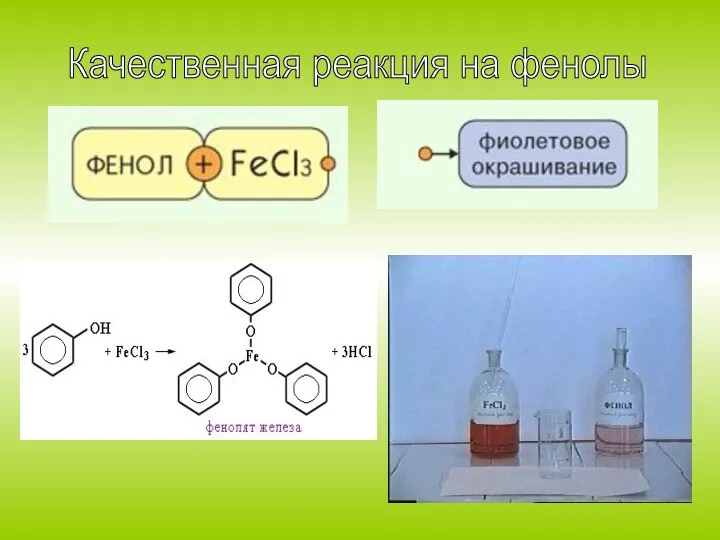
2. Галогенирование. Фенол легко при комнатной температуре
взаимодействует с бромной водой с образованием белого осадка
2,4,6-трибромфенола (качественная реакция на фенол)
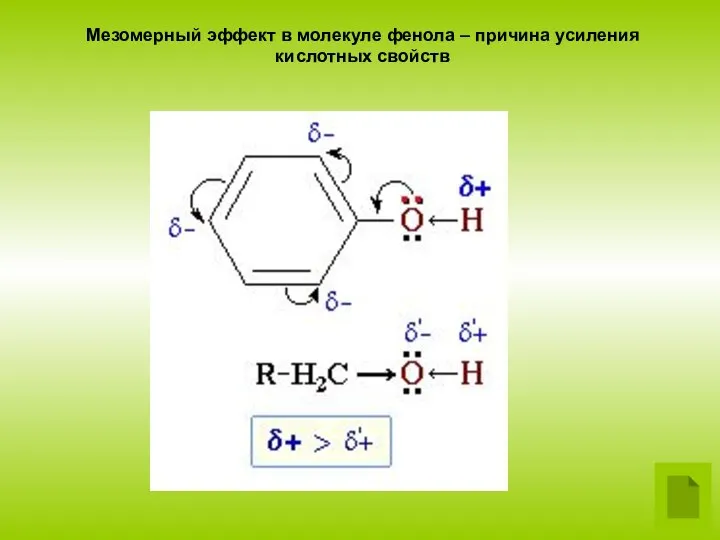
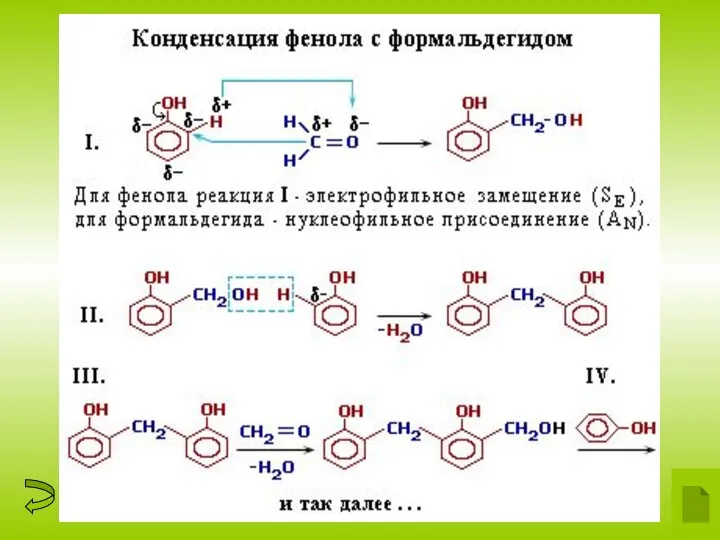
3. Конденсация с альдегидами . Данная реакция имеет
большое практическое значение и используется при получении
фенолформальдегидных смол.
Получение





 Электролиз
Электролиз Тотығу стрестің өсімдіктерге әсері
Тотығу стрестің өсімдіктерге әсері Цветные сплавы
Цветные сплавы Химические элементы. Знаки химических элементов
Химические элементы. Знаки химических элементов Биологическая роль и строение углеводов
Биологическая роль и строение углеводов Определение содержания солей в нефти
Определение содержания солей в нефти Аммиак NH3
Аммиак NH3 Строение электронных оболочек атомов
Строение электронных оболочек атомов Обменные реакции в растворах электролитов
Обменные реакции в растворах электролитов Заседание временного творческого коллектива ОМО УГПС Технологии материалов, УГПС Химические технологии
Заседание временного творческого коллектива ОМО УГПС Технологии материалов, УГПС Химические технологии Особенности сплавов цветных металлов
Особенности сплавов цветных металлов Органічні та біологічні молекули
Органічні та біологічні молекули Металлы
Металлы  Моторные масла. Свойства, состав, классификация
Моторные масла. Свойства, состав, классификация Презентация по Химии "Природные источники углеводородов" - скачать смотреть бесплатно
Презентация по Химии "Природные источники углеводородов" - скачать смотреть бесплатно Химическая связь
Химическая связь Основания
Основания Презентация по Химии "Родословная Д. И. Менделеева." - скачать смотреть бесплатно
Презентация по Химии "Родословная Д. И. Менделеева." - скачать смотреть бесплатно Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение
Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение Алканы (Предельные углеводороды. Парафины. Насыщенные углеводороды)
Алканы (Предельные углеводороды. Парафины. Насыщенные углеводороды) Химическая связь. Лекция 2
Химическая связь. Лекция 2 Химическая технология природных энергоносителей и углеродных материалов
Химическая технология природных энергоносителей и углеродных материалов Утилизация отходов
Утилизация отходов Состав, строение и свойства белков
Состав, строение и свойства белков Хлор. Химический элемент
Хлор. Химический элемент Презентация АТОМНАЯ ЭНЕРГЕТИКА
Презентация АТОМНАЯ ЭНЕРГЕТИКА КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко Лекция 2. Физико-химические основы строения пластов
Лекция 2. Физико-химические основы строения пластов