Содержание
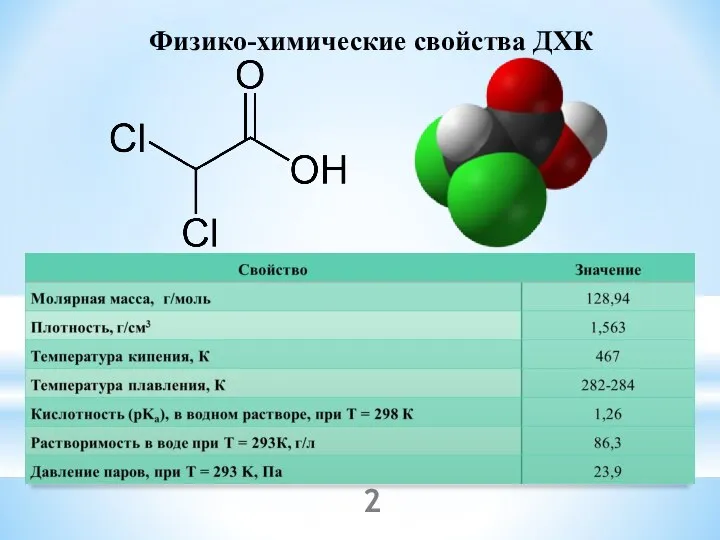
- 2. Физико-химические свойства ДХК
- 3. Получение ДХК Наиболее распространенный метод производства для дихлоруксусной кислоты является гидролиз хлорангидрида, который получают окислением трихлорэтилена:
- 4. Применение ДХК
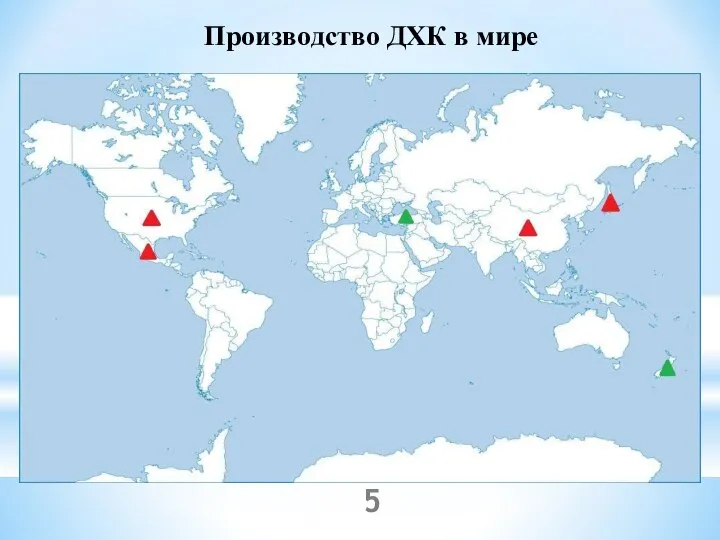
- 5. Производство ДХК в мире
- 6. Токсикологическое действие ДХК Гигиенические нормативы ДХК В 2002 г. Международное агентство по изучению рака (МАИР) отнесло
- 7. Проблема хлорирования воды Концентрация ДХК в хлорированной воде бассейнов Концентрация ДХК в питьевой воде
- 8. Концентрация радикалов OH в атмосфере приблизительно составляет 106 молекул в см3. OH● + CHCl2COOH → C●Cl2COOH
- 9. Метод конкурирующих реакций F + CHCl2COOH → продукты (C*Cl2COOH; CHCl2COO*; HF) F + c-C6H12 → продукты
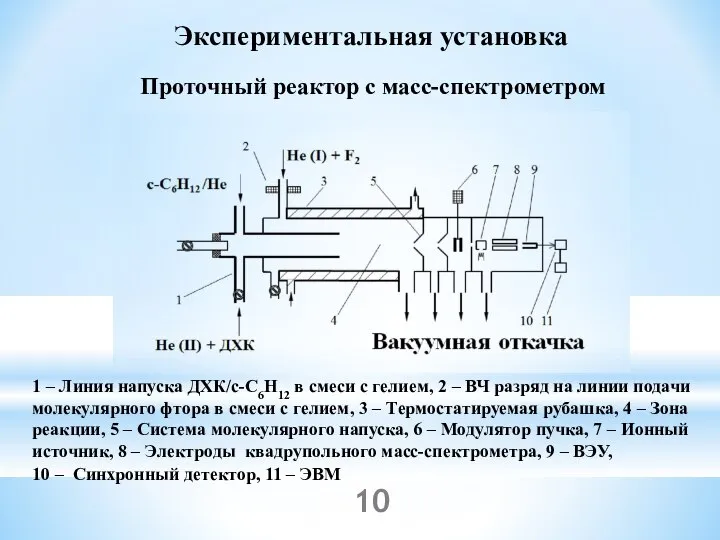
- 10. Экспериментальная установка 1 – Линия напуска ДХК/c-C6H12 в смеси с гелием, 2 – ВЧ разряд на
- 11. Экспериментальная установка
- 12. Экспериментальная установка Разряд Система вакуумной откачки (паромасляный насос)
- 13. Экспериментальная установка Реактор
- 14. Результаты эксперимента Сравнительный масс-спектр ДХК
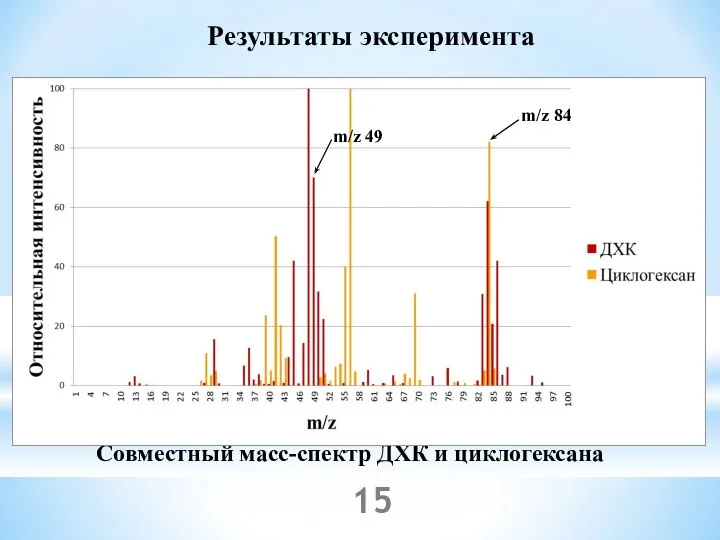
- 15. Результаты эксперимента Совместный масс-спектр ДХК и циклогексана m/z 84 m/z 49
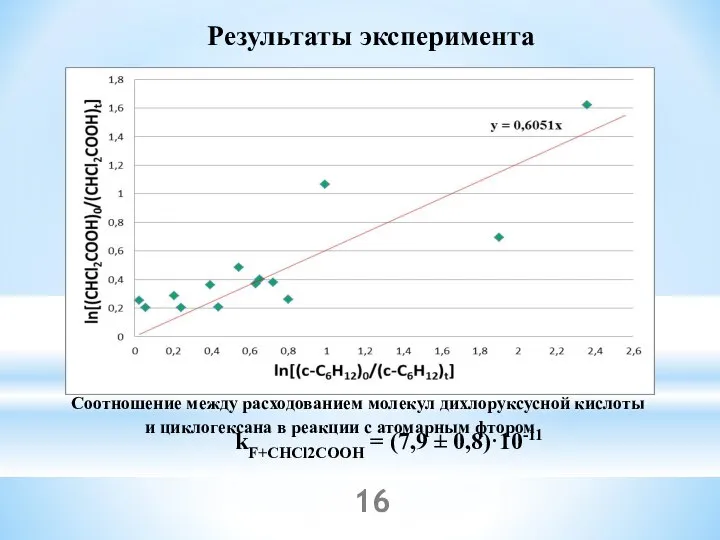
- 16. Результаты эксперимента kF+CHCl2COOH = (7,9 ± 0,8)·10-11 Соотношение между расходованием молекул дихлоруксусной кислоты и циклогексана в
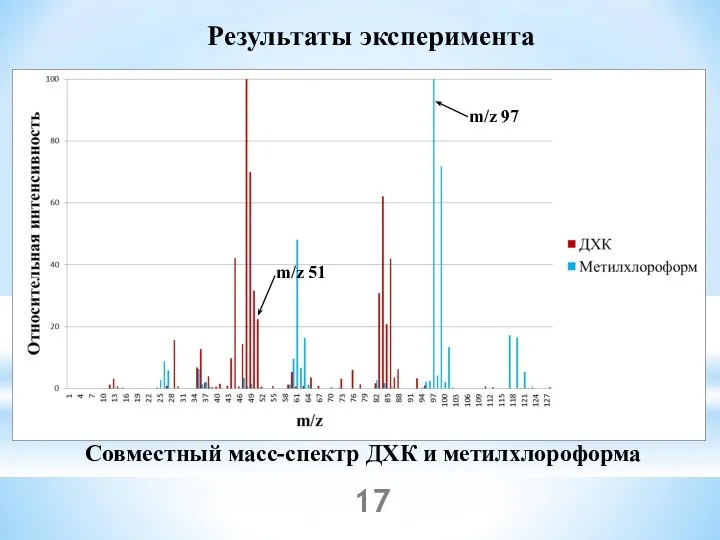
- 17. Результаты эксперимента Совместный масс-спектр ДХК и метилхлороформа m/z 97 m/z 51
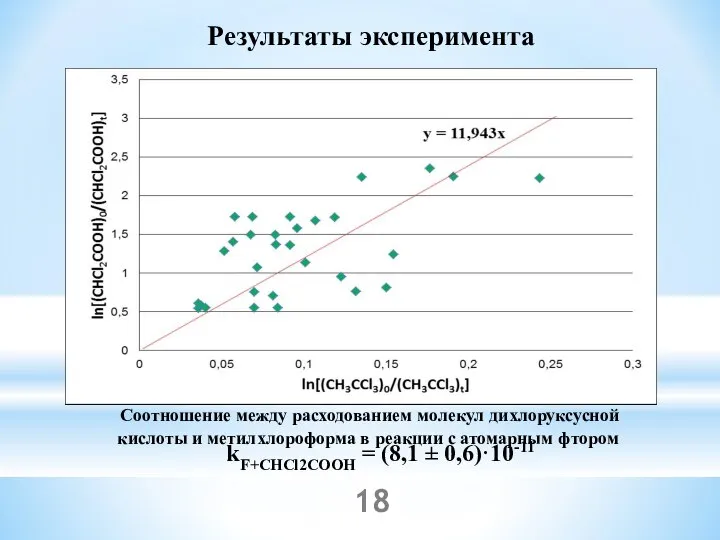
- 18. Результаты эксперимента Соотношение между расходованием молекул дихлоруксусной кислоты и метилхлороформа в реакции с атомарным фтором kF+CHCl2COOH
- 19. Выводы Среднее значение константы скорости реакции составляет: kF+CHCl2COOH = (8,0 ± 0,9)·10-11 cm3 molecule-1 s-1
- 21. Скачать презентацию











 Тема: Химическая связь и ее типы Урок химии в 11 классе
Тема: Химическая связь и ее типы Урок химии в 11 классе Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений
Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть
Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть  Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Alkanes. A “family” of hydrocarbons
Alkanes. A “family” of hydrocarbons Фенол Подготовил Ежов Сергей
Фенол Подготовил Ежов Сергей Орагническая химия. Теория А.М. Бутлерова
Орагническая химия. Теория А.М. Бутлерова Продолжение лекции «Химическая связь»
Продолжение лекции «Химическая связь»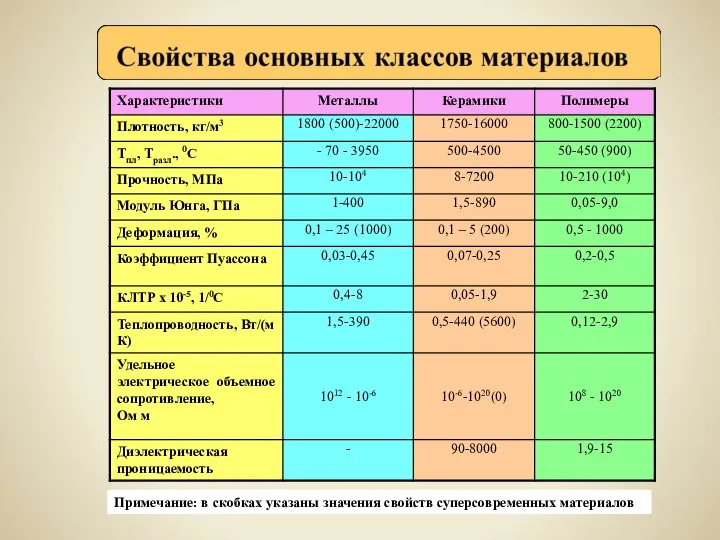 Свойства основных классов материалов
Свойства основных классов материалов Алканы и алкены
Алканы и алкены Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение Логическая структура модуля по дисциплине Аналитическая химия
Логическая структура модуля по дисциплине Аналитическая химия Аммофос өндірісі. Алыну әдісі
Аммофос өндірісі. Алыну әдісі Лабораторные занятия по теме: Методы защиты электрооборудования от коррозии
Лабораторные занятия по теме: Методы защиты электрооборудования от коррозии Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Гидролиз солей. Составила: Рудчинкова Л.Ю., учитель химии и биологии МОУ «СОШ им. М.М. Рудченко с. Перелюб Перелюбского района Сарато
Гидролиз солей. Составила: Рудчинкова Л.Ю., учитель химии и биологии МОУ «СОШ им. М.М. Рудченко с. Перелюб Перелюбского района Сарато Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Межкристаллитная коррозия МКК
Межкристаллитная коррозия МКК Механизмы двухсубстатных реакций
Механизмы двухсубстатных реакций Начала физической химии
Начала физической химии Альдегиды и кетоны: свойства, получение, применение
Альдегиды и кетоны: свойства, получение, применение Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом
Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом Липиды. Классификация липидов
Липиды. Классификация липидов Орбитали и связи
Орбитали и связи Общая и медицинская химия
Общая и медицинская химия Циклоалканы. Строение, изомерия, получение и свойства
Циклоалканы. Строение, изомерия, получение и свойства Белки. Структуры белков
Белки. Структуры белков