Содержание
- 2. РАСТВОРЫ
- 3. 1. По агрегатному состоянию – жидкие, твердые и газообразные КЛАССИФИКАЦИЯ 2. По размеру частиц – истинные,
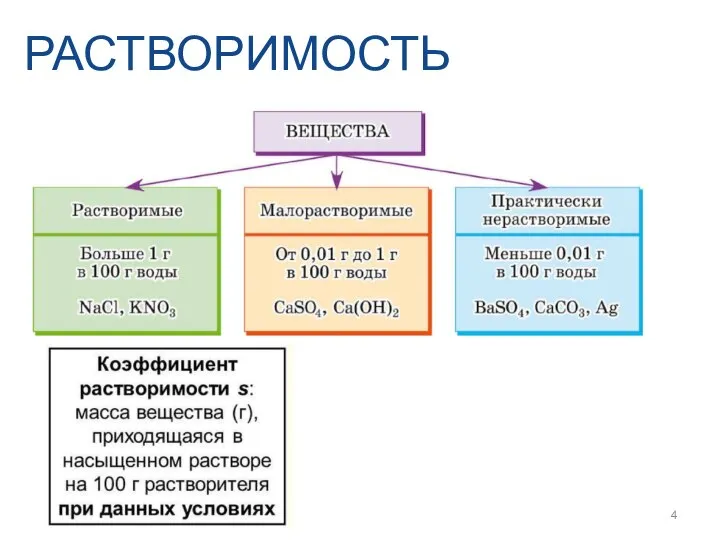
- 4. РАСТВОРИМОСТЬ
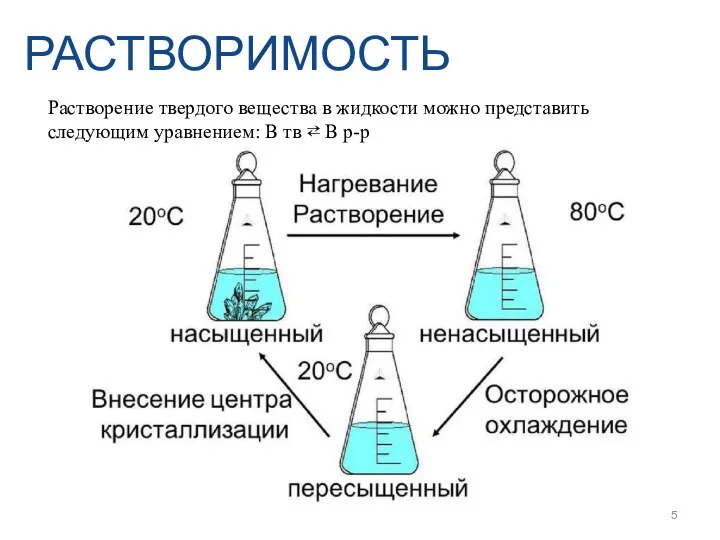
- 5. РАСТВОРИМОСТЬ Растворение твердого вещества в жидкости можно представить следующим уравнением: В тв ⇄ В р-р
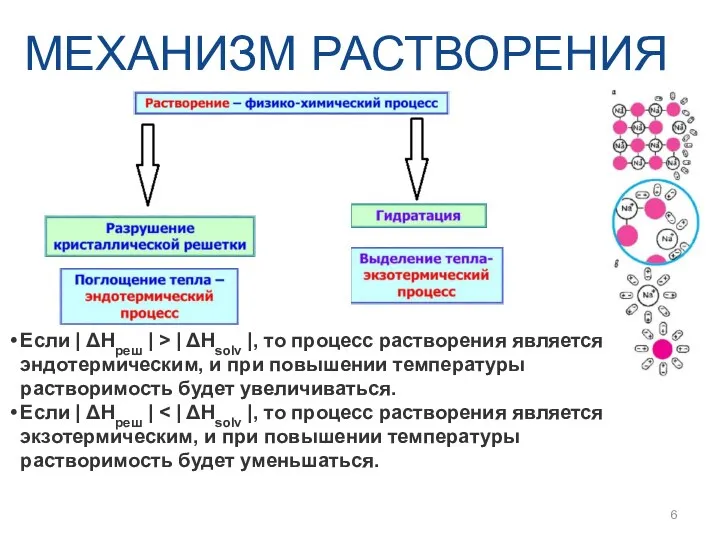
- 6. МЕХАНИЗМ РАСТВОРЕНИЯ Если | ΔHреш | > | ΔHsolv |, то процесс растворения является эндотермическим, и
- 7. КОНЦЕНТРАЦИЯ РАСТВОРОВ - порядок реакции
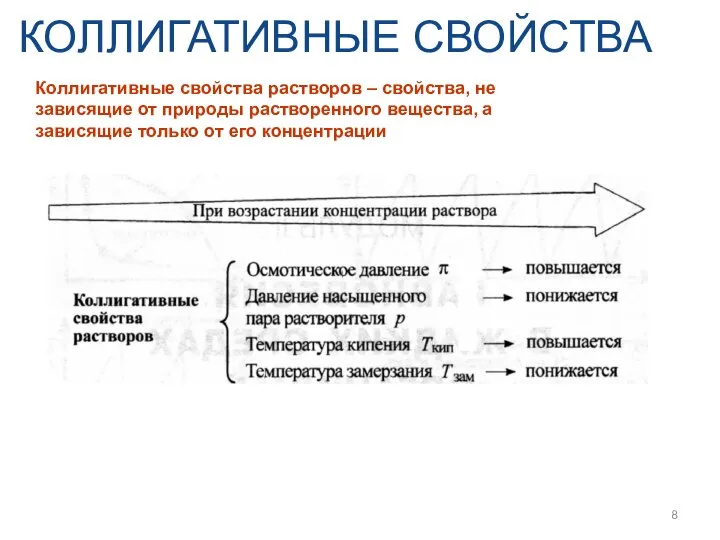
- 8. КОЛЛИГАТИВНЫЕ СВОЙСТВА Коллигативные свойства растворов – свойства, не зависящие от природы растворенного вещества, а зависящие только
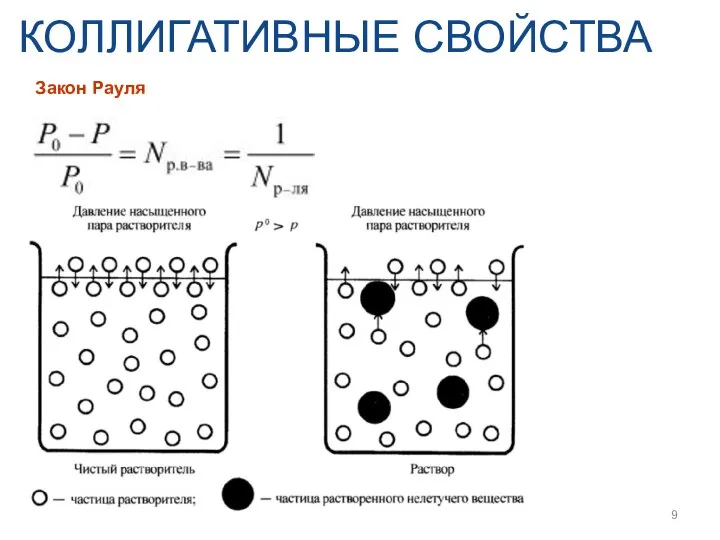
- 9. КОЛЛИГАТИВНЫЕ СВОЙСТВА Закон Рауля
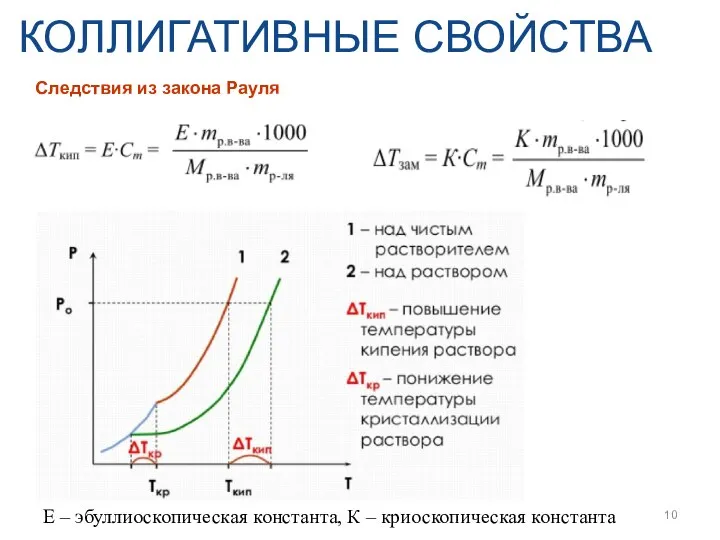
- 10. КОЛЛИГАТИВНЫЕ СВОЙСТВА Следствия из закона Рауля E – эбуллиоскопическая константа, К – криоскопическая константа
- 11. КОЛЛИГАТИВНЫЕ СВОЙСТВА
- 12. КОЛЛИГАТИВНЫЕ СВОЙСТВА Уравнения применимы только к растворам неэлектролитов. Для растворов электролитов в уравнение вводят поправочный коэффициент
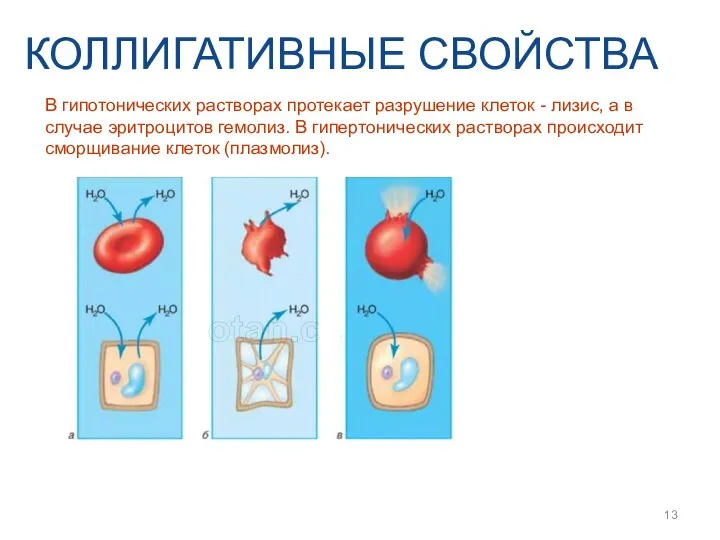
- 13. КОЛЛИГАТИВНЫЕ СВОЙСТВА В гипотонических растворах протекает разрушение клеток - лизис, а в случае эритроцитов гемолиз. В
- 14. Распад электролита на ионы под влиянием полярных молекул растворителя (например, воды) называется электролитической диссоциацией. АВ +
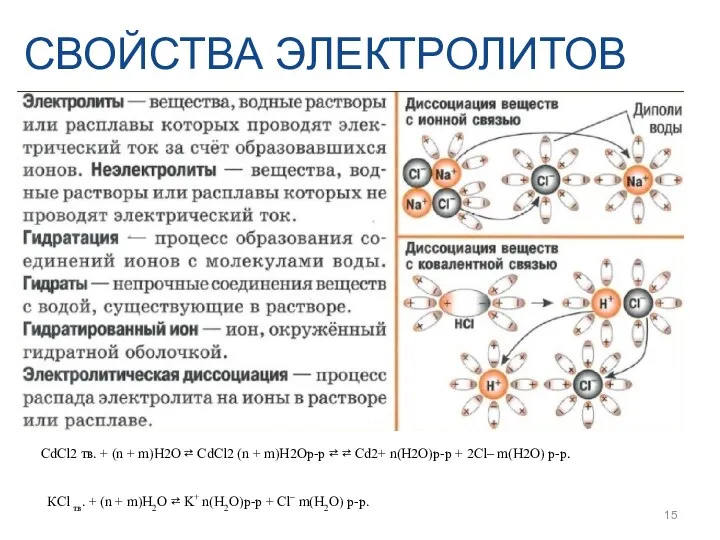
- 15. СВОЙСТВА ЭЛЕКТРОЛИТОВ CdCl2 тв. + (n + m)H2O ⇄ CdCl2 (n + m)H2Oр-р ⇄ ⇄ Cd2+
- 16. СВОЙСТВА ЭЛЕКТРОЛИТОВ Т.к. диссоциация- процесс обратимый, то для него справедлив закон действующих масс. Для бинарного электролита
- 17. СВОЙСТВА ЭЛЕКТРОЛИТОВ Пусть раствор содержал С моль/л электролита, степень диссоциации которого α, тогда в равновесии концентрация
- 18. СВОЙСТВА ЭЛЕКТРОЛИТОВ
- 19. СВОЙСТВА ЭЛЕКТРОЛИТОВ Согласно теории Дебая-Гюккеля для описания реальных свойств растворов сильных электролитов вводится понятие эффективной (кажущейся)
- 20. СВОЙСТВА ЭЛЕКТРОЛИТОВ Z=1 (NaNO3 = Na+ + NO3-) I= ½ (C1·12 + C2·12) = C I=C
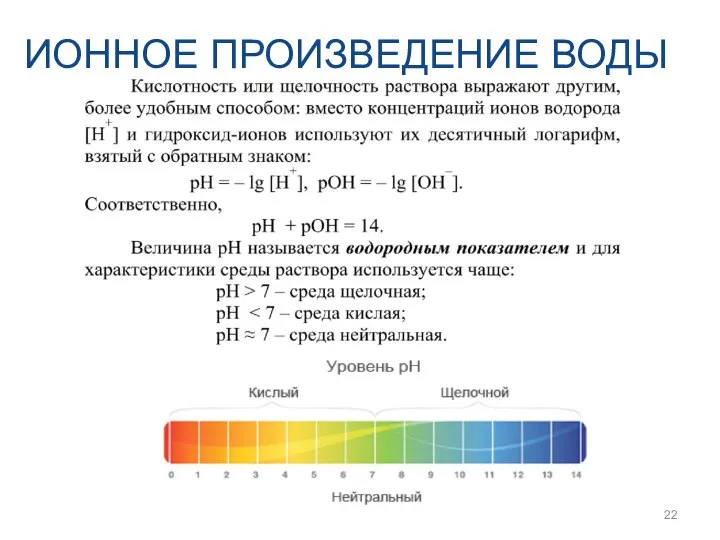
- 21. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ
- 22. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ
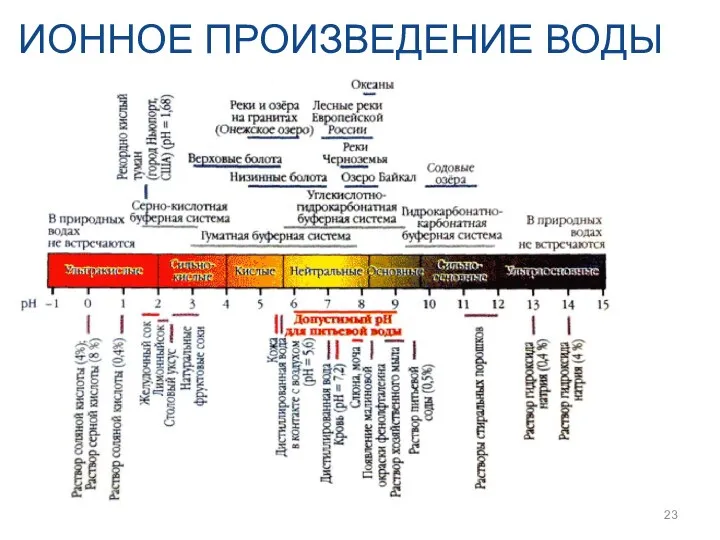
- 23. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ
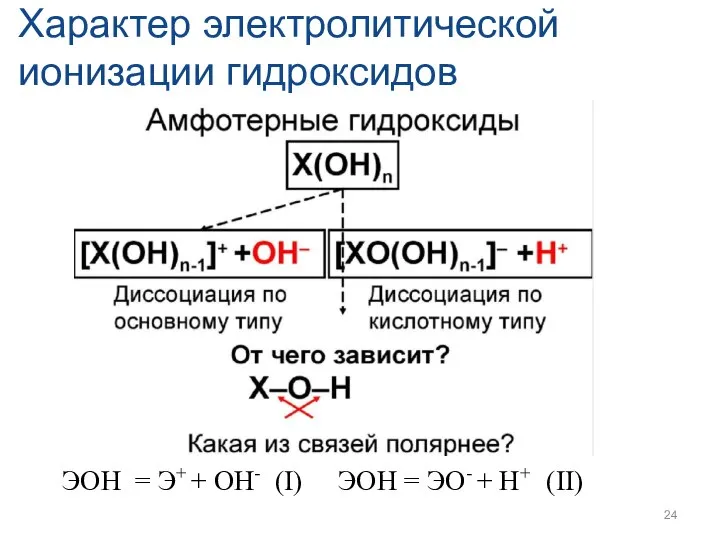
- 24. Характер электролитической ионизации гидроксидов ЭОН = Э+ + ОН- (I) ЭОН = ЭО- + Н+ (II)
- 25. Диссоциация многоосновных кислот
- 26. Диссоциация многокислотных оснований
- 27. Реакции в растворах. Гидролиз Нейтрализация доходит до конца только тогда, когда единственным малодиссоциированным веществом в системе
- 28. Реакции в растворах. Гидролиз
- 29. Реакции в растворах. Гидролиз
- 30. Реакции в растворах. Гидролиз
- 31. Реакции в растворах. Гидролиз
- 32. Реакции в растворах. Гидролиз В случае соли NH4CH3COO, константы диссоциации КNH4OH = КСН3СООН практически одинаковы и
- 33. Гидролиз. Количественные характеристики
- 34. Гетерогенные равновесия в растворе
- 35. Гетерогенные равновесия в растворе Условие образования осадка: ПИ > ПР ПИ – произведение концентраций (ионов)
- 36. Гетерогенные равновесия в растворе
- 37. Гетерогенные равновесия в растворе Малорастворимые соли слабых кислот потому и растворяются в сильных кислотах, что при
- 38. Гетерогенные равновесия в растворе Иногда осадки солей растворяются с образованием прочных комплексных ионов. Так, хлорид серебра
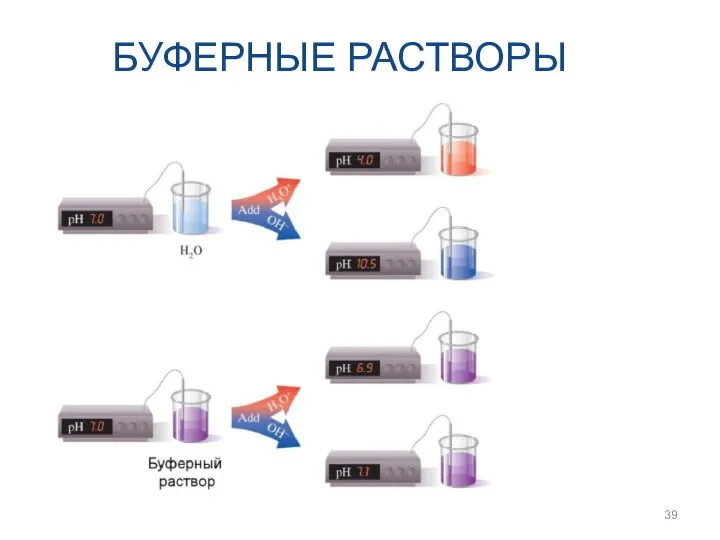
- 39. БУФЕРНЫЕ РАСТВОРЫ
- 40. БУФЕРНЫЕ РАСТВОРЫ
- 41. БУФЕРНЫЕ РАСТВОРЫ
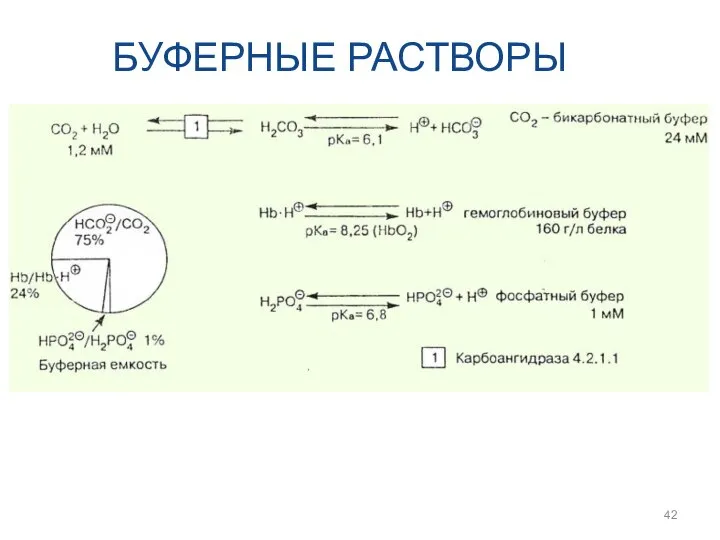
- 42. БУФЕРНЫЕ РАСТВОРЫ
- 43. БУФЕРНЫЕ РАСТВОРЫ
- 44. БУФЕРНЫЕ РАСТВОРЫ
- 45. БУФЕРНЫЕ РАСТВОРЫ
- 46. БУФЕРНЫЕ РАСТВОРЫ
- 47. БУФЕРНЫЕ РАСТВОРЫ
- 49. Скачать презентацию

































 Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Шкала рН
Шкала рН Тотығутотықсыздану титрлеу әдістері. Дәріс № 7
Тотығутотықсыздану титрлеу әдістері. Дәріс № 7 Мас-спектр кластерів вуглецю
Мас-спектр кластерів вуглецю Предельные углеводороды
Предельные углеводороды Обобщающий урок по теме: «Основные классы неорганических соединений. Генетическая связь между классами неорганических соединени
Обобщающий урок по теме: «Основные классы неорганических соединений. Генетическая связь между классами неорганических соединени Металлы и сплавы -материал для древних и современных олимпийских наград.
Металлы и сплавы -материал для древних и современных олимпийских наград. Морфология тел полезных ископаемых
Морфология тел полезных ископаемых Алюминий в природе
Алюминий в природе Моделирование (7 класс)
Моделирование (7 класс) Топливо и топливосжигающие устройства. Искусственные виды топлив. Газификация твердого топлива
Топливо и топливосжигающие устройства. Искусственные виды топлив. Газификация твердого топлива Региональная металлогения
Региональная металлогения Термический анализ
Термический анализ Расчет ректификационной колонны
Расчет ректификационной колонны Дисперсные
Дисперсные  Дисперсные системы
Дисперсные системы Органічні розчинники. Їх застосування
Органічні розчинники. Їх застосування Химическая энергия
Химическая энергия Управління якістю лікарських засобів у фармацевтичній галузі
Управління якістю лікарських засобів у фармацевтичній галузі Биохимия почек и мочи. (Лекция 10)
Биохимия почек и мочи. (Лекция 10) Промышленные типы месторождений железа
Промышленные типы месторождений железа Дисперсные системы
Дисперсные системы Соли. Названия и классификация солей
Соли. Названия и классификация солей Разработка методики расчета фазового равновесия при длительном хранении СПГ
Разработка методики расчета фазового равновесия при длительном хранении СПГ galogeny
galogeny Cоляная кислота и ее соли
Cоляная кислота и ее соли Производство азотной кислоты
Производство азотной кислоты МОУ Квитокская средняя общеобразовательная школа. УРОК ХИМИИ. 11 КЛАСС. Химия и производство. Учитель: Левицкая Лариса Виктор
МОУ Квитокская средняя общеобразовательная школа. УРОК ХИМИИ. 11 КЛАСС. Химия и производство. Учитель: Левицкая Лариса Виктор