Содержание
- 2. Якість лікарського засобу – це сукупність властивостей, які надають лікарському засобу (ЛЗ) здатність задовольняти потреби споживачів
- 3. КРИТЕРІЇ ЯКОСТІ ефективність; безпечність застосування; значна перевага перед відомими, близькими за дією лікарськими засобами, які вже
- 4. Забезпечення якості ліків – це широко розповсюджена концепція, що включає комплекс заходів, які впливають на якість
- 5. Контроль якості – це та частина системи управління якістю, яка пов'язана з відбором проб, специфікаціями та
- 6. ОСНОВНІ ВИМОГИ ДО КОНТРОЛЮ ЯКОСТІ: Наявність належних засобів для здійснення контролю. Кваліфікований персонал, на який покладена
- 7. Мають бути складені протоколи, які документально підтверджують, що всі необхідні заходи щодо відбору проб, контролю та
- 8. Перевірка готової продукції на відповідність реєстраційному досьє (активні інгредієнти, допоміжні речовини, необхідна чистота, контейнери (упаковка), маркування).
- 9. Необхідно зберігати достатню кількість контрольних зразків вихідної сировини і препаратів, що дозволяє проводити випробування продукції в
- 10. Якість ЛЗ досягається шляхом суворого дотримання принципів забезпечення якості від розробки до виробництва і потім підтримується
- 11. Якість - сукупність особливостей та характеристик продуктів або послуг, які роблять можливим задовольняти існуючі або передбачені
- 12. Якість лікарського засобу - придатність до призначеного використання та відповідність усім вимогам національної реєстрації, а також
- 13. ОСНОВНИМИ ВЛАСТИВОСТЯМИ (ХАРАКТЕРИСТИКАМИ) ЛІКАРСЬКОГО ЗАСОБУ Є: ефективність лікарського засобу - полягає у високих профілактичних і терапевтичних
- 14. новий лікарський засіб має бути ефективніший, ніж відомий аналог, при задовільному сприйнятті; при однаковій ефективності з
- 15. тотожність і кількісний вміст інгредієнтів, відсутність домішок, активність і стабільність хімічного складу лікарського засобу, стійкість при
- 16. активність стосовно: кількості нозологій (одна, дві і більше); перебігу хвороби (гострий, підгострий, хронічний); ступеня важкості хвороби
- 17. Якість виробу медичного призначення - сукупність властивостей медичного виробу, які відображають безпеку, довговічність, надійність медичного виробу
- 18. ВЛАСТИВОСТЯМИ ВИРОБУ МЕДИЧНОГО ПРИЗНАЧЕННЯ Є: ефективність; надійність; функціональність; довговічність; ремонтопридатність; економічність; дизайн; легкість у користуванні тощо.
- 19. Ефективність виробу медичного призначення - сукупність характеристик медичного виробу, що забезпечують досягнення профілактичного, діагностичного, лікувального та/або
- 20. Оцінка якості лікарського засобу - це діяльність державних органів, які мають право оцінювати шляхом інспектування, нагляду,
- 21. Гарантування якості лікарського засобу - це діяльність підприємств, організацій, установ і закладів, що виробляють або розподіляють
- 22. GМР (за визначенням ВООЗ) — частина [концепції] забезпечення якості, що гарантує послідовне виробництво і контроль виробів
- 23. ОСНОВНІ ВИМОГИ ДО НАЛЕЖНОЇ ВИРОБНИЧОЇ ПРАКТИКИ ЛІКАРСЬКИХ ЗАСОБІВ Власник ліцензії на виробництво зобов'язаний виробляти лікарські засоби
- 24. ЗАБЕЗПЕЧЕННЯ ЯКОСТІ Забезпечення якості – всеохоплююче поняття, що включає всі питання, які окремо або в цілому
- 25. СИСТЕМА ЗАБЕЗПЕЧЕННЯ ЯКОСТІ, ПОВИННА ГАРАНТУВАТИ, ЩО: лікарські засоби розроблені й досліджені з урахуванням вимог належної виробничої
- 26. лікарські засоби не будуть продані й поставлені до того, як Уповноважена особа не засвідчить, що кожна
- 27. НАЛЕЖНА ВИРОБНИЧА ПРАКТИКА ЛІКАРСЬКИХ ЗАСОБІВ (GMP) Належна виробнича практика є частиною забезпечення якості, яка гарантує, що
- 28. ОСНОВНІ ВИМОГИ GMP: усі виробничі процеси повинні бути чітко визначені; їх слід систематично переглядати з урахуванням
- 29. мають бути в наявності всі засоби для GMP, включаючи: навчений персонал, що має необхідну кваліфікацію; відповідні
- 30. оператори повинні бути навчені правильному виконанню процедур; під час виробництва слід складати протоколи рукописним способом і/або
- 31. при дистрибуції (оптовому продажу) продукції зведений до мінімуму ризик зниження її якості; має бути в наявності
- 32. КОНТРОЛЬ ЯКОСТІ Контроль якості – це та частина належної виробничої практики, яка пов'язана із відбором проб,
- 33. ДО КОНТРОЛЮ ЯКОСТІ ВИСУВАЮТЬ ТАКІ ОСНОВНІ ВИМОГИ: наявність належних засобів, навчений персонал і затверджені методики для
- 34. методи випробування мають пройти валідацію; мають бути складені протоколи (рукописним способом і/або з використанням приладу, що
- 35. протоколи, складені за результатами контролю й випробувань матеріалів, проміжної, нерозфасованої та готової продукції, повинні бути офіційно
- 36. ОГЛЯД ЯКОСТІ ПРОДУКЦІЇ Огляди, як правило, слід здійснювати та документувати щорічно, беручи до уваги попередні огляди;
- 37. огляд критичних точок контролю у процесі виробництва та контролю готової продукції; огляд всіх серій, що не
- 38. огляд всіх змін, внесених до процесів або аналітичних методик; огляд поданих/затверджених/відхилених змін до реєстраційних досьє, у
- 39. огляд правильності попередніх коригувальних заходів щодо процессу виробництва або обладнання; огляд післяреєстраційних зобов’язань у разі отримання
- 40. УПРАВЛІННЯ РИЗИКОМ ДЛЯ ЯКОСТІ Управління ризиком для якості є систематичним процесом для загальної оцінки, контролю, передачі
- 41. СИСТЕМА УПРАВЛІННЯ РИЗИКОМ ДЛЯ ЯКОСТІ МАЄ ГАРАНТУВАТИ, ЩО оцінювання ризику для якості базується на наукових знаннях,
- 43. Скачать презентацию




















![GМР (за визначенням ВООЗ) — частина [концепції] забезпечення якості, що гарантує](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404141/slide-21.jpg)



















 Компания «Родник здоровья»
Компания «Родник здоровья» Электродный потенциал. Критерий протекания окислительно-восстановительных реакций
Электродный потенциал. Критерий протекания окислительно-восстановительных реакций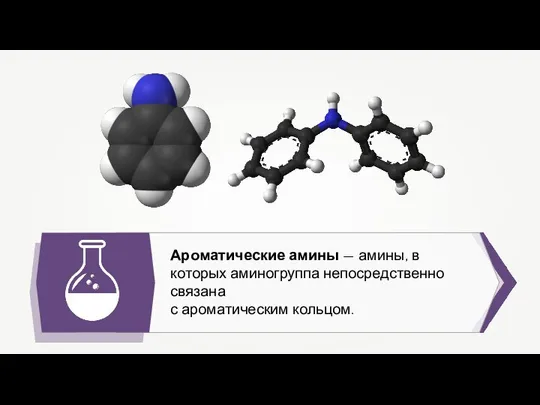 Ароматические амины
Ароматические амины Электропроводность растворов электролитов. Числа переноса
Электропроводность растворов электролитов. Числа переноса Полимерные растворы – условия образования
Полимерные растворы – условия образования Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией
Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией Семинар на тему Природные источники углеводородов и их переработка
Семинар на тему Природные источники углеводородов и их переработка Вода и растворы. Лекция 3
Вода и растворы. Лекция 3 Энергия алмасудың бірінші сатысы: күрделі заттардың арнайы жолдармен ыдырап, универсалды аралық өнімдерге айналуы
Энергия алмасудың бірінші сатысы: күрделі заттардың арнайы жолдармен ыдырап, универсалды аралық өнімдерге айналуы Митохондрии и пластиды
Митохондрии и пластиды Склеивание древесины. Клеи
Склеивание древесины. Клеи Минералы и горные породы Крыма
Минералы и горные породы Крыма Краун-эфиры
Краун-эфиры Углеводы. Дисахариды и полисахариды
Углеводы. Дисахариды и полисахариды Химический источник электрического тока
Химический источник электрического тока Презентация по Химии "Адсорбционная хроматография. Жидкостная хроматография" - скачать смотреть
Презентация по Химии "Адсорбционная хроматография. Жидкостная хроматография" - скачать смотреть  Застосування нових сучасних матеріалів з оригінльними властивостями
Застосування нових сучасних матеріалів з оригінльними властивостями  Внеклассное мероприятие по химии. Своя игра
Внеклассное мероприятие по химии. Своя игра Основы химической термодинамики
Основы химической термодинамики Роль химии в жизни человека
Роль химии в жизни человека Амфотерные неорганические и органические соединения МОУ «Гатчинская СОШ №2» Учитель химии: Г.Г.Павлова Учитель инфор
Амфотерные неорганические и органические соединения МОУ «Гатчинская СОШ №2» Учитель химии: Г.Г.Павлова Учитель инфор К 180-летию со дня рождения Д.И. Менделеева
К 180-летию со дня рождения Д.И. Менделеева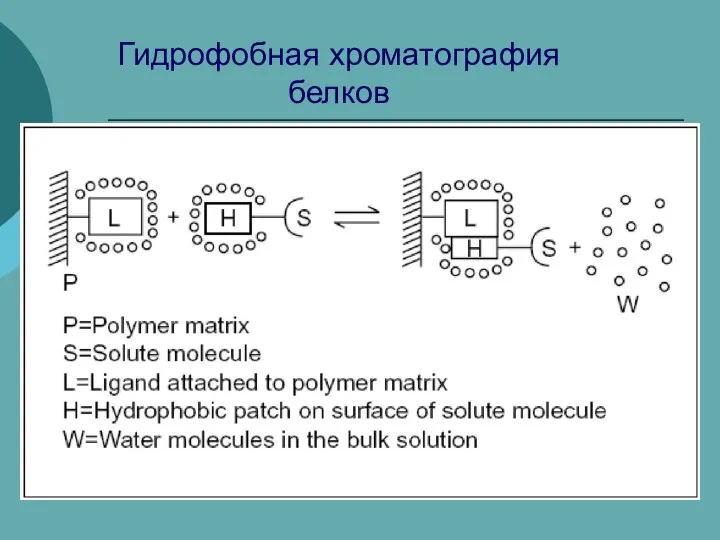 Гидрофобная хроматография белков
Гидрофобная хроматография белков Алюминий и его сплавы. Назначение
Алюминий и его сплавы. Назначение Классификация и номенклатура органических соединений. (Лекция 1)
Классификация и номенклатура органических соединений. (Лекция 1) Научные основы процессов разделения
Научные основы процессов разделения Chemical bonds
Chemical bonds Материаловедение
Материаловедение