Содержание
- 2. Кислород в атмосфере Земли появился около 600 млн. лет назад, что потребовало перестройки механизмов функционирования живых
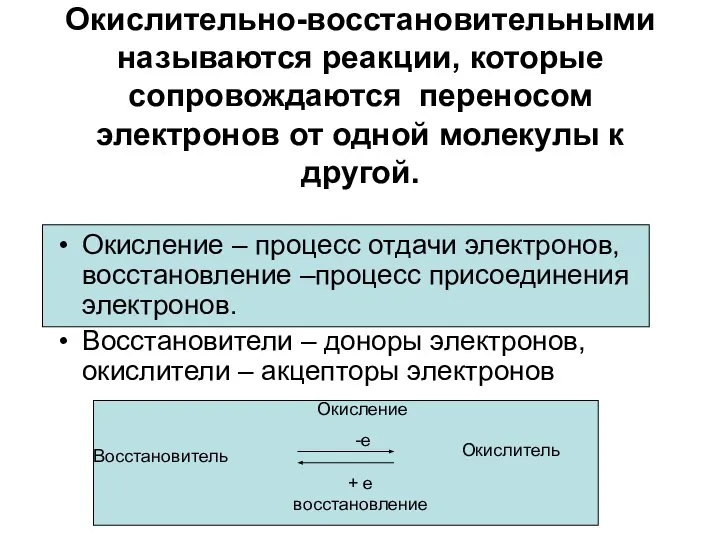
- 3. Окислительно-восстановительными называются реакции, которые сопровождаются переносом электронов от одной молекулы к другой. Окисление – процесс отдачи
- 4. Значение реакций окисления-восстановления в организме 1. Окисление питательных веществ (процессы катаболизма), при которых выделяется энергия, запасаемая
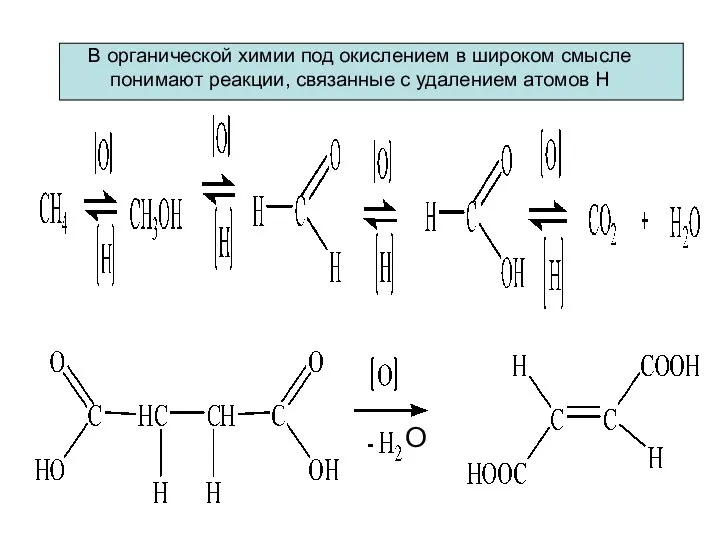
- 5. В органической химии под окислением в широком смысле понимают реакции, связанные с удалением атомов Н О
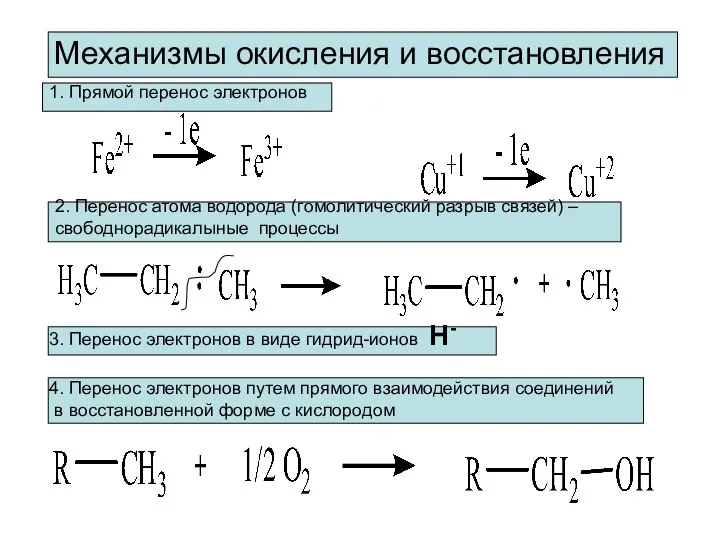
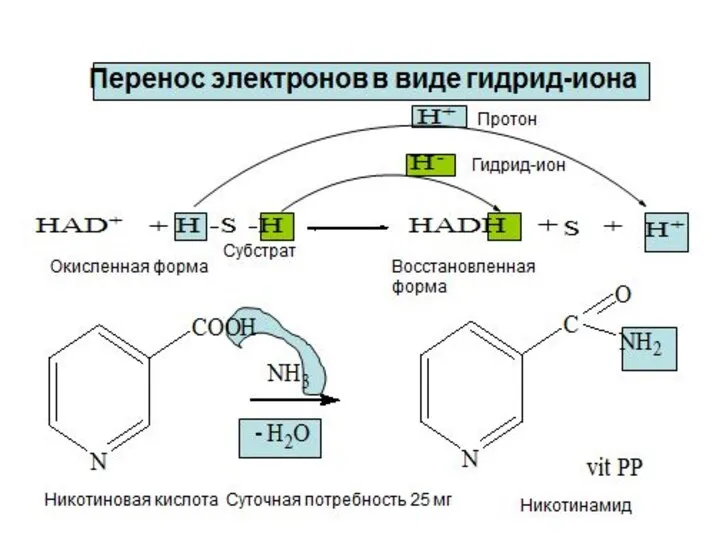
- 6. Механизмы окисления и восстановления 1. Прямой перенос электронов 2. Перенос атома водорода (гомолитический разрыв связей) –
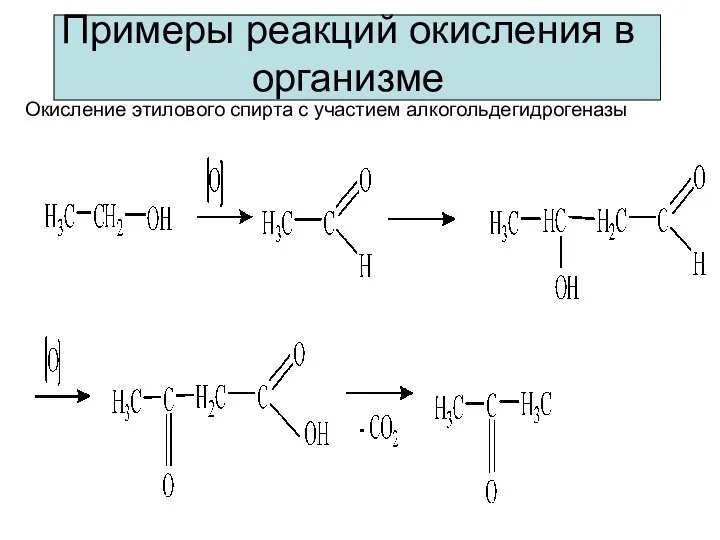
- 7. Примеры реакций окисления в организме Окисление этилового спирта с участием алкогольдегидрогеназы
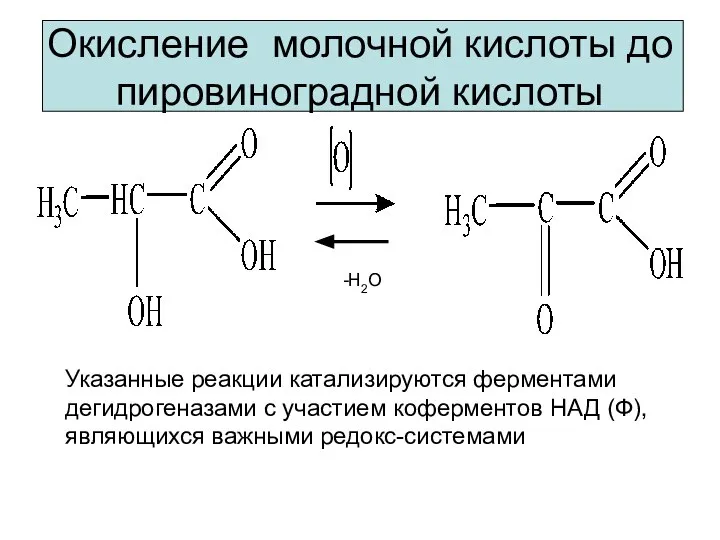
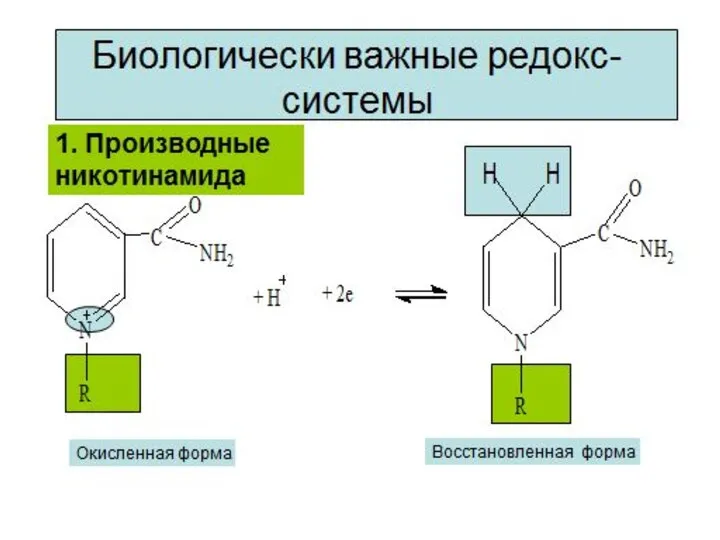
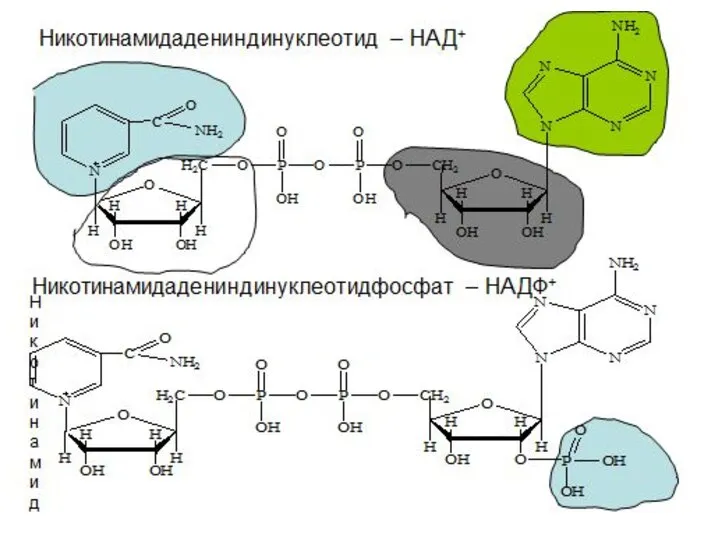
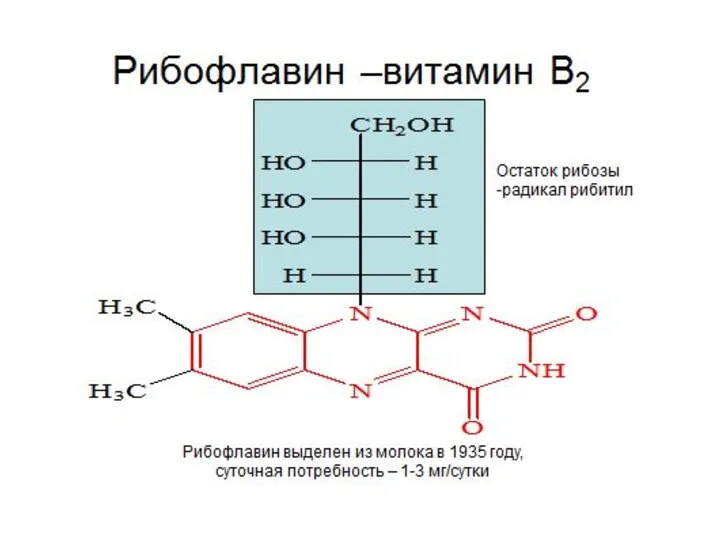
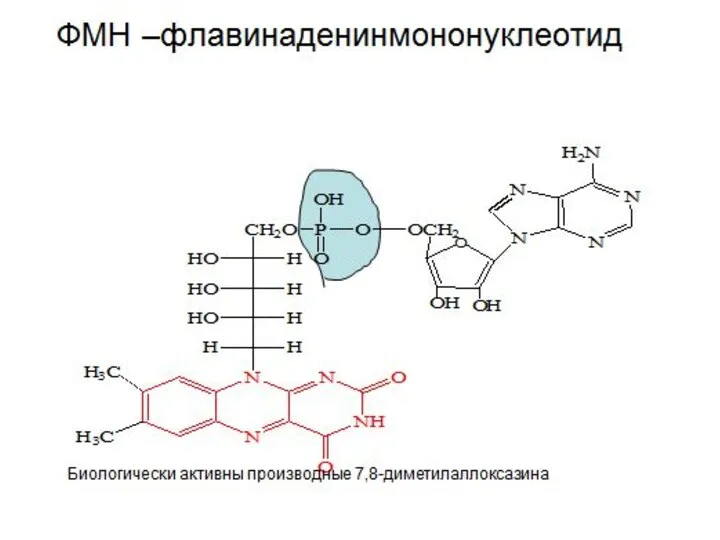
- 8. Окисление молочной кислоты до пировиноградной кислоты Указанные реакции катализируются ферментами дегидрогеназами с участием коферментов НАД (Ф),
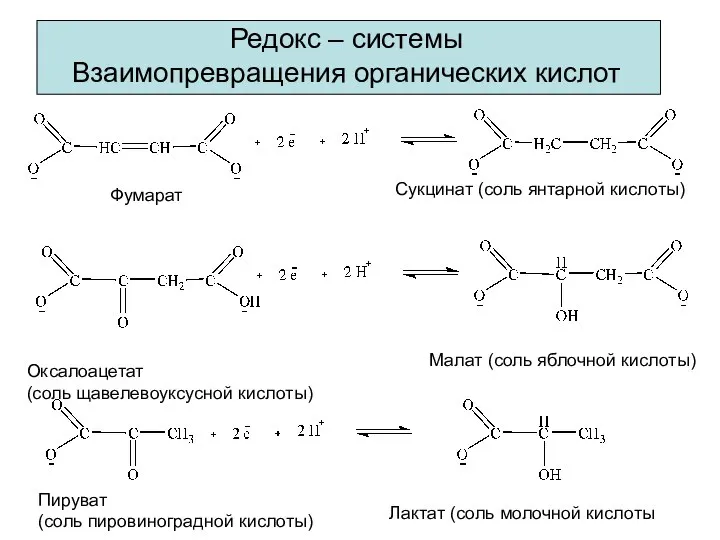
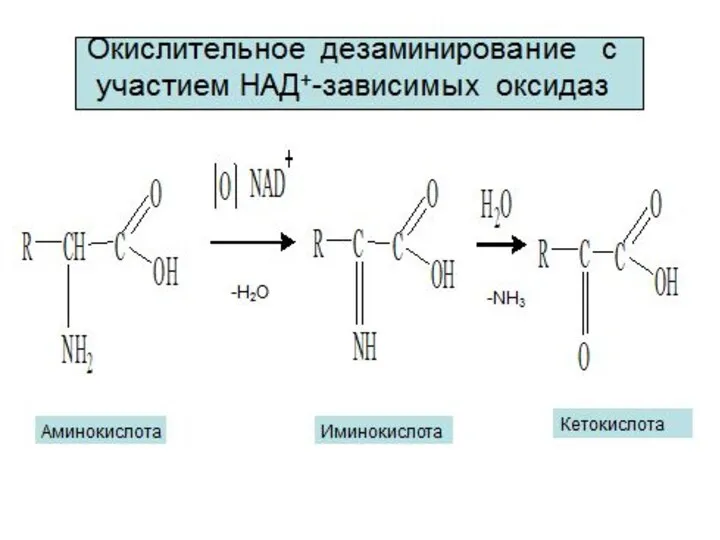
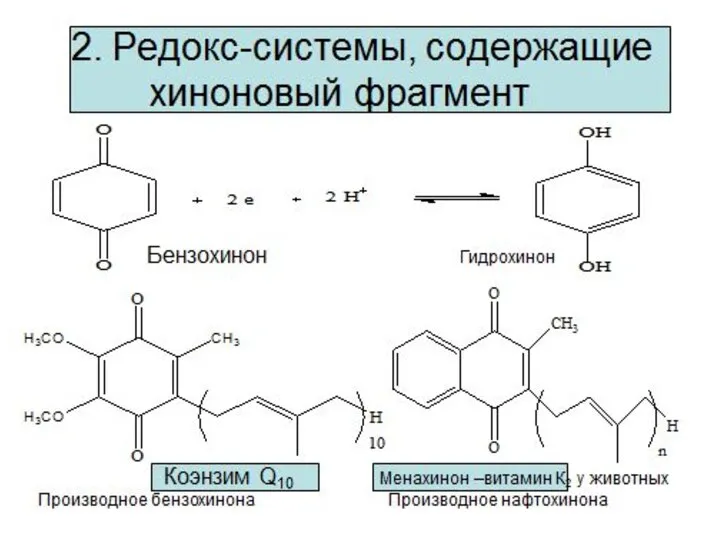
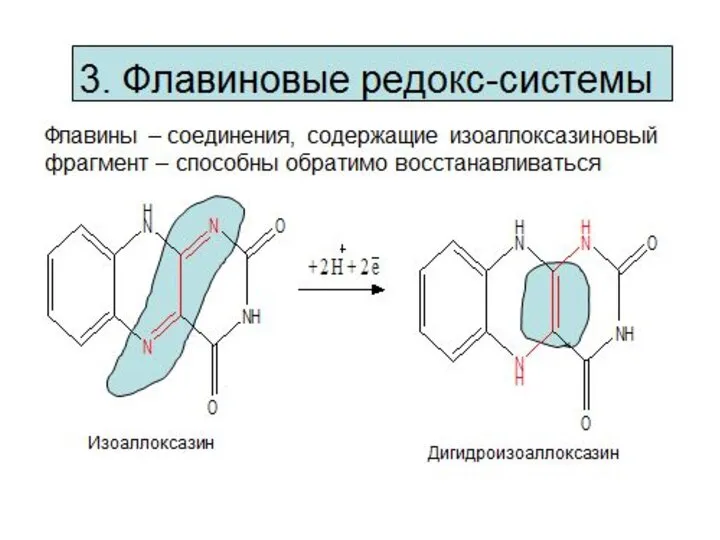
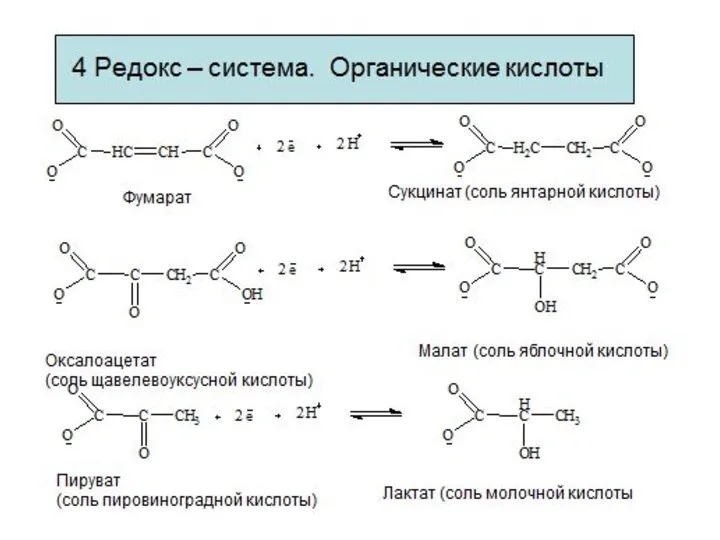
- 9. Редокс – системы Взаимопревращения органических кислот Фумарат Сукцинат (соль янтарной кислоты) Оксалоацетат (соль щавелевоуксусной кислоты) Малат
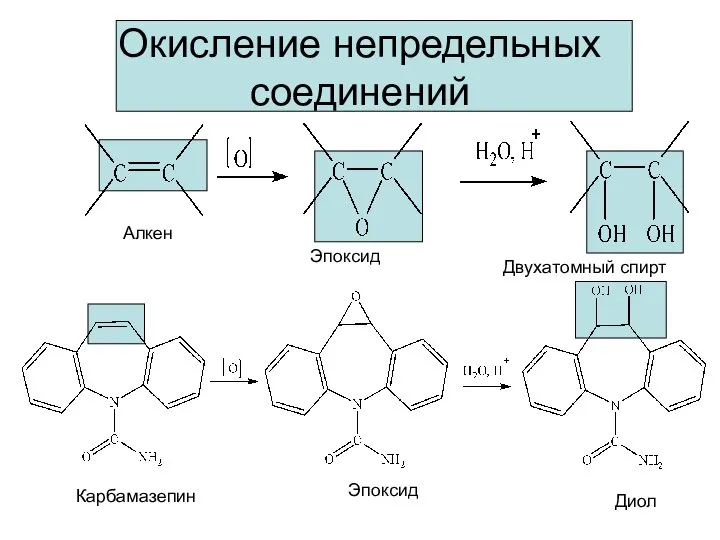
- 11. Окисление непредельных соединений Алкен Эпоксид Двухатомный спирт Карбамазепин Эпоксид Диол
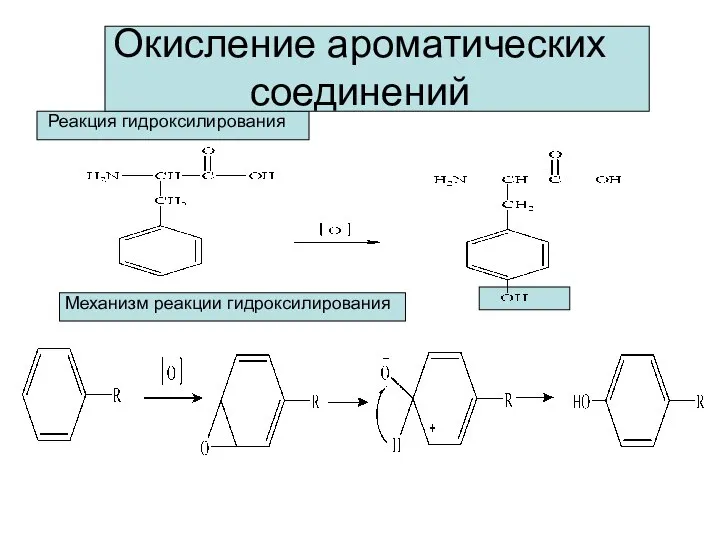
- 12. Окисление ароматических соединений Реакция гидроксилирования Механизм реакции гидроксилирования
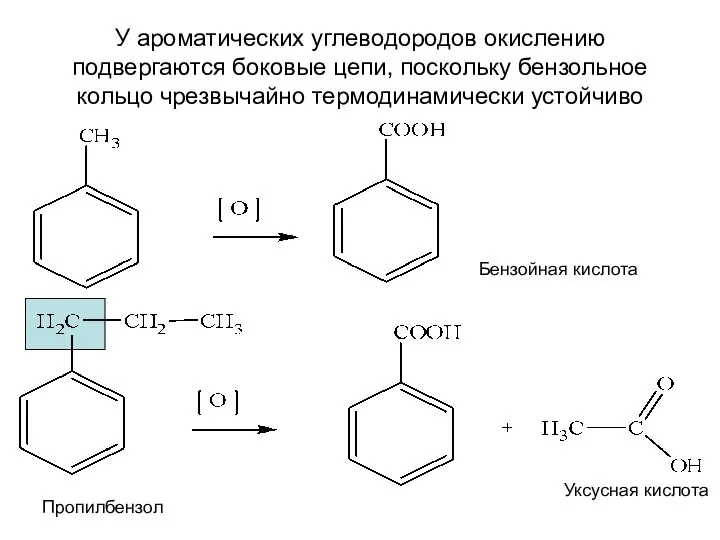
- 13. У ароматических углеводородов окислению подвергаются боковые цепи, поскольку бензольное кольцо чрезвычайно термодинамически устойчиво Бензойная кислота Пропилбензол
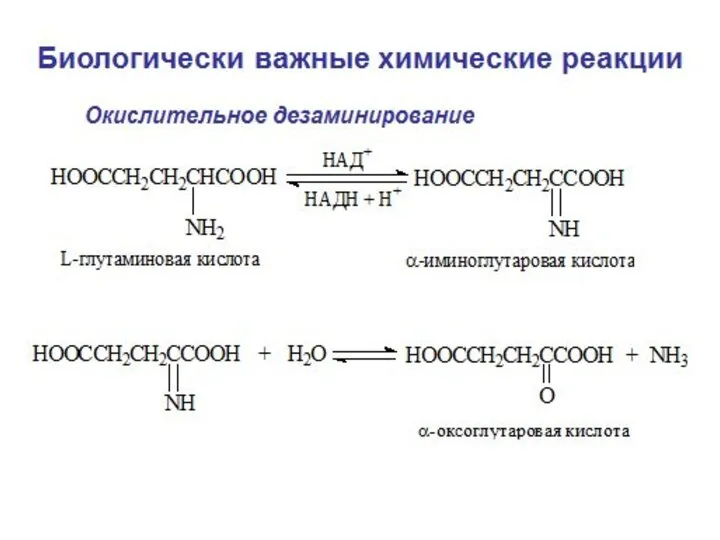
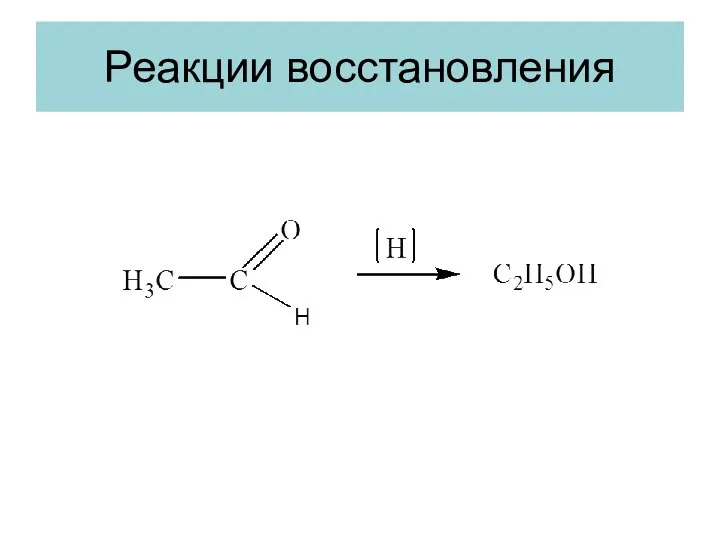
- 14. Реакции восстановления
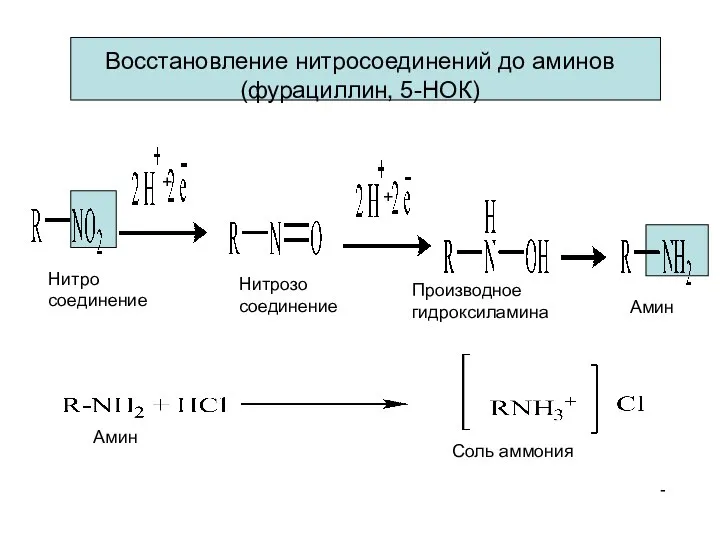
- 15. Нитро соединение Нитрозо соединение Производное гидроксиламина Амин Восстановление нитросоединений до аминов (фурациллин, 5-НОК) - Амин Соль
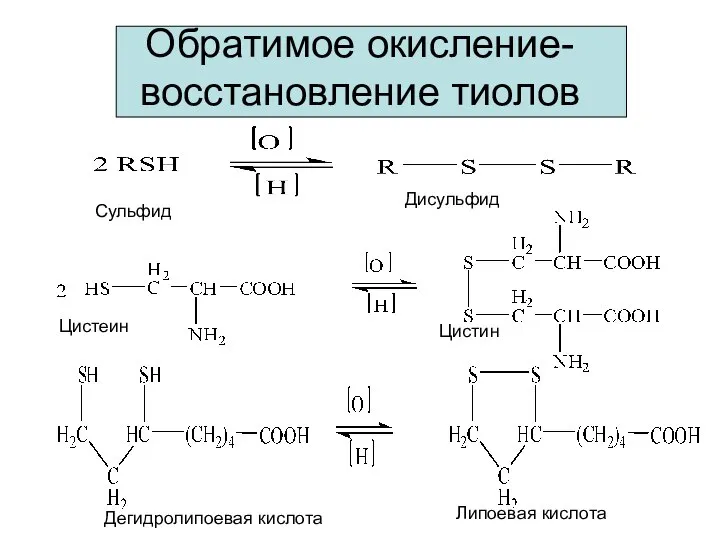
- 16. Обратимое окисление-восстановление тиолов Сульфид Дисульфид Цистеин Цистин Дегидролипоевая кислота Липоевая кислота
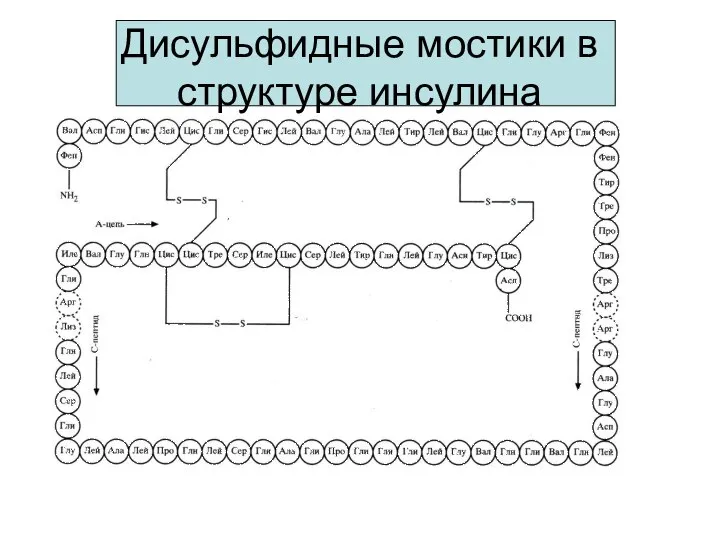
- 17. Дисульфидные мостики в структуре инсулина
- 29. Скачать презентацию



 Структурная организация и функции клеточных мембран. (Лекция 2.1)
Структурная организация и функции клеточных мембран. (Лекция 2.1) Презентация по Химии "Амфотерные оксиды и гидроксиды" 9 класс
Презентация по Химии "Амфотерные оксиды и гидроксиды" 9 класс Химическая термодинамика
Химическая термодинамика Неорганические вещества клетки
Неорганические вещества клетки Спазган: применение, форма, свойства, состав
Спазган: применение, форма, свойства, состав Окислительно-восстановительные потенциалы (электродные потенциалы)
Окислительно-восстановительные потенциалы (электродные потенциалы) Теоретические и экспериментальные методы исследования в химии
Теоретические и экспериментальные методы исследования в химии Азотсодержащие соединения
Азотсодержащие соединения Презентация по Химии "Высшие природные полимеры - Белки и Нуклеиновые кислоты" - скачать смотреть
Презентация по Химии "Высшие природные полимеры - Белки и Нуклеиновые кислоты" - скачать смотреть  Неметаллы. Аллотропия. Куцапкина Людмила Васильевна учитель химии ГБОУ гимназии № 343 Невского района Санкт- Петербурга
Неметаллы. Аллотропия. Куцапкина Людмила Васильевна учитель химии ГБОУ гимназии № 343 Невского района Санкт- Петербурга Неоадъювантная химиотерапия в лечении рака шейки матки. Опыт РКОД
Неоадъювантная химиотерапия в лечении рака шейки матки. Опыт РКОД Проблемно-исследовательские технологии обучения химии
Проблемно-исследовательские технологии обучения химии Стали: свойства и классификации (для 7-х классов)
Стали: свойства и классификации (для 7-х классов) Продовольча проблема і хімія Сочнєвої Ірини 11-А
Продовольча проблема і хімія Сочнєвої Ірини 11-А  Выполнил: учащийся группы 3/4 Драгун Кирилл Руководитель: преподаватель химии Карасева Е.А.
Выполнил: учащийся группы 3/4 Драгун Кирилл Руководитель: преподаватель химии Карасева Е.А. Химический состав яблока
Химический состав яблока Титан. Структура, применение, свойства (11 класс)
Титан. Структура, применение, свойства (11 класс) Становление органической химии как отдельной науки. (Модуль 1)
Становление органической химии как отдельной науки. (Модуль 1) Полимерные реагенты в бурении
Полимерные реагенты в бурении Типы кристаллических решёток
Типы кристаллических решёток Презентация по Химии "Химическая эволюция. Эволюция биополимерных молекул. 10-й класс" - скачать смотреть
Презентация по Химии "Химическая эволюция. Эволюция биополимерных молекул. 10-й класс" - скачать смотреть  Physics and chemistry of surface phenomena
Physics and chemistry of surface phenomena Обмен белков
Обмен белков Сырьевая база парфюмерно-косметической промышленности
Сырьевая база парфюмерно-косметической промышленности Именные реакции в органической химии
Именные реакции в органической химии Цемент Цеме́нт — загальна назва мінеральних в'яжучих порошкоподібних матеріалів, які після затворення їх водою, з рідкого або тістоподібного стану переходять у твердий каменеподібний стан при звичайній температурі і використовується для
Цемент Цеме́нт — загальна назва мінеральних в'яжучих порошкоподібних матеріалів, які після затворення їх водою, з рідкого або тістоподібного стану переходять у твердий каменеподібний стан при звичайній температурі і використовується для  Пластические массы
Пластические массы Производство серной кислоты контактным способом
Производство серной кислоты контактным способом