Содержание
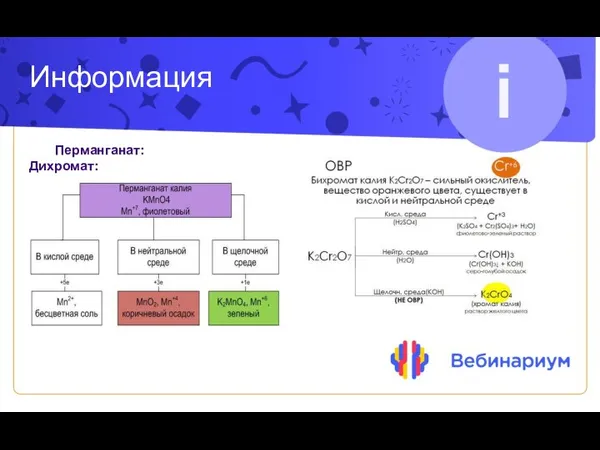
- 2. Информация Перманганат: Дихромат:
- 3. Окисление алкенов 1а) 3C2H4 + 2KMnO4 + 4H2O → 3CH2OH–CH2OH + 2MnO2 + 2KOH 1б) 5CH3CH=CHCH2CH3
- 4. Окисление алкинов 1) 5CH3C≡CH + 8KMnO4 + 12H2SO4 → 5CH3COOH + 5CO2 + 8MnSO4 + 4K2SO4
- 5. Окисление гомологов бензола C6H5CH3 +2KMnO4 → C6H5COOK + 2MnO2 + KOH + H2O C6H5CH2CH3 + 4KMnO4
- 6. Уравниваем!
- 7. Уравниваем!
- 8. Окисление спиртов Непосредственным продуктом окисления первичных спиртов являются альдегиды, а вторичных – кетоны. 1)3C2H5OH + K2Cr2O7
- 9. Окисление альдегидов и кетонов 1) 3CH3CHO + 2KMnO4 → CH3COOH + 2CH3COOK + 2MnO2 + H2O
- 10. Окисление альдегидов и кетонов 7) 5HCOH + 4KMnO4(изб) + 6H2SO4 (нагревание) → 4MnSO4 + 2K2SO4 +
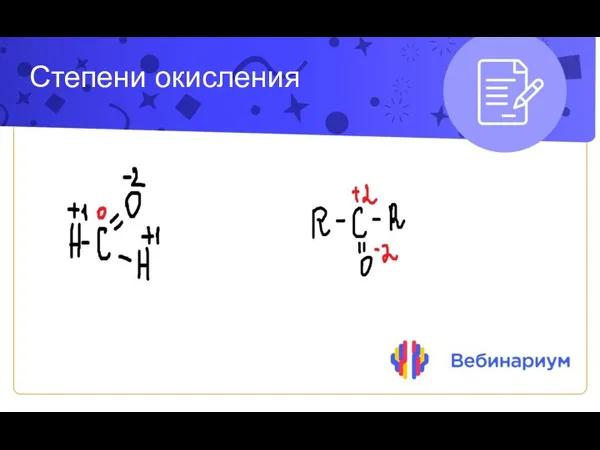
- 11. Степени окисления
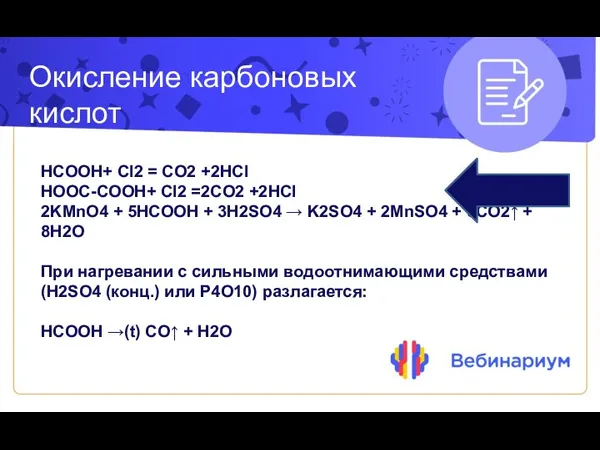
- 12. Окисление карбоновых кислот HCOOH+ Cl2 = CO2 +2HCl HOOC-COOH+ Cl2 =2CO2 +2HCl 2KMnO4 + 5HCOOH +
- 14. Скачать презентацию








 Гетероциклдік қосылыстар
Гетероциклдік қосылыстар Операции термической обработки
Операции термической обработки Липиды и обмен липидов
Липиды и обмен липидов Белоктар, пептидтер мен амин қышқылдары
Белоктар, пептидтер мен амин қышқылдары Презентация Изомерия
Презентация Изомерия  Особенности органических реакций
Особенности органических реакций Мини-проект по дисциплине: «Физико-химические методы исследования и техника лабораторных работ»
Мини-проект по дисциплине: «Физико-химические методы исследования и техника лабораторных работ» Синтетические моющие средства
Синтетические моющие средства Презентация по Химии "Гигиенические аспекты загрязнения пищевых продуктов чужеродными в-ми и меры профилактики" - скачать см
Презентация по Химии "Гигиенические аспекты загрязнения пищевых продуктов чужеродными в-ми и меры профилактики" - скачать см Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Концентраційні межі поширення полум'я
Концентраційні межі поширення полум'я Реакции координированных лигандов
Реакции координированных лигандов Строение электронных оболочек атомов
Строение электронных оболочек атомов Метод комплесонометрии
Метод комплесонометрии Периодический закон химических элементов Д. И. Менделеева и периодическая система
Периодический закон химических элементов Д. И. Менделеева и периодическая система Галогены
Галогены Практическое применение метанола
Практическое применение метанола 11-Step total synthesis of pallambins C and D
11-Step total synthesis of pallambins C and D Потенциометрия
Потенциометрия Химиялық, принципиалдық және технологиялық сызбанұсқалар. Технологиялқ процестерді ұйымдастыру принциптері
Химиялық, принципиалдық және технологиялық сызбанұсқалар. Технологиялқ процестерді ұйымдастыру принциптері Колообіг оксигену в природі. Озон. Застосування кисню та його біологічна роль
Колообіг оксигену в природі. Озон. Застосування кисню та його біологічна роль Адгезия және когезия құбылысының түсінігі. Адгезия және когезия жұмысы
Адгезия және когезия құбылысының түсінігі. Адгезия және когезия жұмысы Металлическая химическая связь. Тема 2.5
Металлическая химическая связь. Тема 2.5 Электрохимические цепи
Электрохимические цепи Специфические пути обмена отдельных аминокислот. Патология. (Лекция 12)
Специфические пути обмена отдельных аминокислот. Патология. (Лекция 12) Гормоны. Классификация гормонов. Общие свойства. Биохимия стероидных гормонов
Гормоны. Классификация гормонов. Общие свойства. Биохимия стероидных гормонов Многоатомные спирты. Фенол.
Многоатомные спирты. Фенол. Презентация по Химии "Все о пищевых добавках класса Е" - скачать смотреть
Презентация по Химии "Все о пищевых добавках класса Е" - скачать смотреть