Содержание
- 2. Менделеев Дмитрий Иванович Русский ученый-энциклопедист. Родился 27 января (8 февраля) 1834 в Тобольске. Менделеев был членом
- 3. Периодический закон и строение атома До открытия Д.И. Менделеева было сделано много попыток классификации и систематизации
- 4. Историческая справка В 1829 году немецкий ученый Д. В. Деберейнер, профессор химии, технологии и фармакологии университета
- 5. Периодический закон Д.И. Менделеева. Открыт в 1869 г. великим русским ученым Д.М. Менделеевым. В работе «Периодическая
- 6. Физический смысл порядкового номера в периодической системе определил Мозли. Закон Мозли: корень из частоты рентгеновского спектра
- 7. Современная формулировка периодического закона химических элементов: Химические свойства элементов находятся в периодической зависимости от заряда ядра
- 8. Периодическая система химических элементов – это система, классификация химических элементов, основанная на периодическом законе. Периодическая таблица
- 9. Периодическая система и периодическая таблица химических элементов
- 10. Периодическая система и периодическая таблица химических элементов Длинная ПТ (32-х клеточная) – все элементы каждого периода
- 12. Связь электронной конфигурации атома элемента с положением в ПС Порядковый номер элемента соответствует заряду ядра атома
- 13. Периоды (горизонтальные ряды) пронумерованы - от 1 до 7. Номер периода соответствует числу электронных слоев в
- 14. В короткой периодической системе все элементы составляют 7 периодов. Первый период включает 2 элемента - водород
- 15. Группы (колонки) обозначаются римскими цифрами - от I до VIII. Каждая группа делится на две подгруппы:
- 16. В таблице 8 главных и 8 побочных подгрупп: всего 16. Элементы семейства лантаноидов и актиноидов (по
- 17. Особенности современной периодической системы элементов Благородные газы рассматриваются как VIII A группа. Но только ксенон проявляет
- 18. Основные особенности изменения свойств элементов по периодам Элементы главных подгрупп различаются числом внешних электронов (s и
- 19. Периодически меняющиеся свойства атомов Атомные и ионные радиусы Потенциал ионизации (энергия ионизации) Сродство к электрону Электроотрицательность
- 20. Периодически меняющиеся свойства атомов Потенциал ионизации Энергия ионизации – энергия, которую необходимо затратить, чтобы удалить из
- 22. Потенциал ионизации По периоду первый ПИ увеличивается, что объясняется увеличением заряда ядра. Однако он изменяется не
- 23. Ионизация переходных d – и f – элементов существенно отличается. Сначала удаляются внешние s – электроны.
- 24. Сродство к электрону Сродство к электрону (F) – энергия, выделяющаяся при присоединении электрона к свободному атому.
- 25. Сродство к электрону атомов элементов 2-го и 3-го периодов
- 26. Атомный радиус Атомный радиус – условный радиус атома, вычисленный из длин связи этого атома с другими
- 27. Электроотрицательность Электроотрицательность (ЭО) атома - способность атома в молекуле притягивать электроны, связывающие его с другими атомами
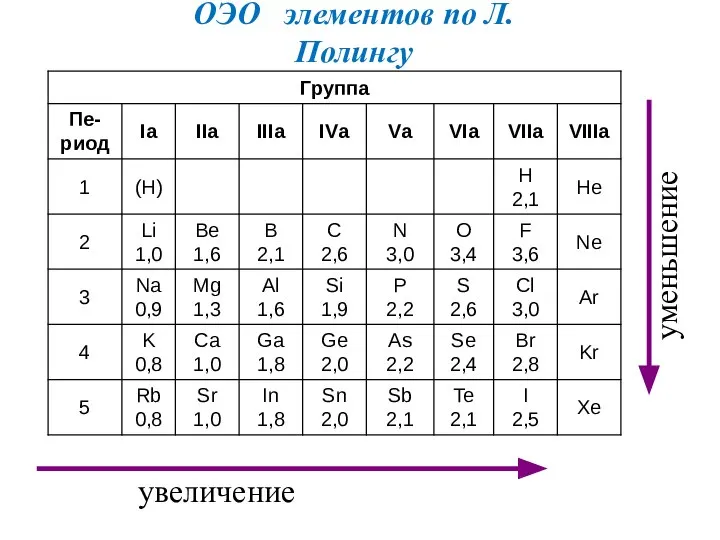
- 28. Шкала Полинга χ F = ½ (1700+310) = 1005 кДж/моль По Полингу χ Li условно принята
- 29. увеличение уменьшение ОЭО элементов по Л.Полингу
- 31. Скачать презентацию



























 Исследование свойств и применение в медицине алкалоидов. Извлечение алкалоидов из травы белены черной.
Исследование свойств и применение в медицине алкалоидов. Извлечение алкалоидов из травы белены черной.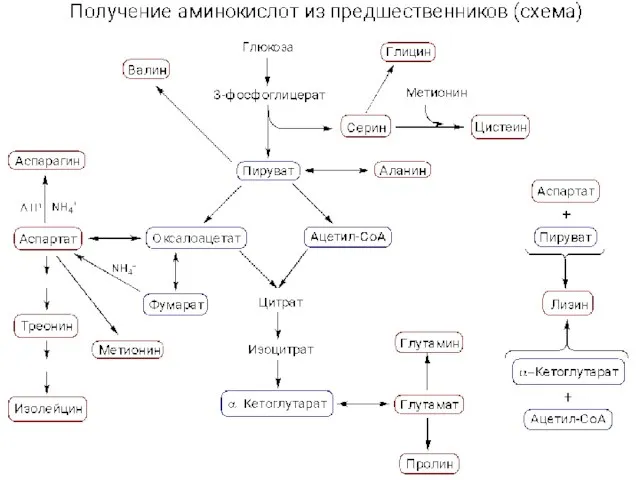 Cинтез аминокислот
Cинтез аминокислот Что изучает химия
Что изучает химия Основные сведения о строении атомов
Основные сведения о строении атомов Жиры. Определение и общая формула
Жиры. Определение и общая формула Лабораторное оборудование, посуда и средства защиты. Химическая лаборатория
Лабораторное оборудование, посуда и средства защиты. Химическая лаборатория Основні класи неорганічних речовин
Основні класи неорганічних речовин Строение и устойчивость дисперсий льда, стабилизированных гидрофобизированным нанокремнеземом
Строение и устойчивость дисперсий льда, стабилизированных гидрофобизированным нанокремнеземом Введение в биохимию
Введение в биохимию Металлическая химическая связь. Тема 2.5
Металлическая химическая связь. Тема 2.5 Именные реакции в органической химии
Именные реакции в органической химии Ферменты. Часть I
Ферменты. Часть I Кварц, опал, халцедоны, кварцсодержащие горные породы кремни, яшма, кварциты, окаменелое дерево, глаза
Кварц, опал, халцедоны, кварцсодержащие горные породы кремни, яшма, кварциты, окаменелое дерево, глаза Определение содержания солей в нефти
Определение содержания солей в нефти Способы выражения состава раствора
Способы выражения состава раствора Лекарственные растения и сырье, содержащие дубильные вещества
Лекарственные растения и сырье, содержащие дубильные вещества Уравнения химических реакций
Уравнения химических реакций Презентация по Химии "Самородки." - скачать смотреть бесплатно_
Презентация по Химии "Самородки." - скачать смотреть бесплатно_ Шкала рН
Шкала рН Українські вчені-хіміки
Українські вчені-хіміки Colligative properties of solutions
Colligative properties of solutions Химия органических соединений. Углеводороды
Химия органических соединений. Углеводороды Макро, микро и ультрамикроэлементы. Их роль
Макро, микро и ультрамикроэлементы. Их роль Химическая кинетика
Химическая кинетика Алюминий и его сплавы
Алюминий и его сплавы Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Ювелирное дело как вид ДПИ
Ювелирное дело как вид ДПИ Алкены
Алкены