Содержание
- 2. Щелочные металлы — это элементы главной подгруппы I группы : литий Li, натрий Nа, калий К,
- 3. Литий был открыт в 1817 г. А. Арфведсоном в минерале петалите. Берцелиус предложил назвать ее литионом
- 4. Сподуменн
- 5. Натрий (Natrium, от англ. и франц. Sodium, нем. Natrium от древнеевр. neter — бурлящее вещество. В
- 6. Галит
- 7. Калий (англ. Potassium, франц. Potassium, нем. Kalium) открыл в 1807 г. Г.Дэви, производивший электролиз твердого, слегка
- 8. Природные соединения калия Сильвин
- 9. Природные соединения калия Карналит
- 10. При спектроскопическом анализе минерала лепидолит (фторсиликат лития и алюминия) и обнаружились две новые красные линии в
- 11. Цезий (англ. Cesium, франц. Cesium, нем. Caesium) - первый элемент, открытый с помощью спектрального анализа. Р.Бунзен
- 12. Этот элемент был предсказан Д.И.Менделеевым (как Эка-цезий), и был открыт (по его радиоактивности) в 1939 г.
- 14. СТРОЕНИЕ АТОМОВ На внешнем энергетическом уровне атомы этих элементов содержат по одному электрону, находящемуся на сравнительно
- 15. Щелочные металлы - простые вещества
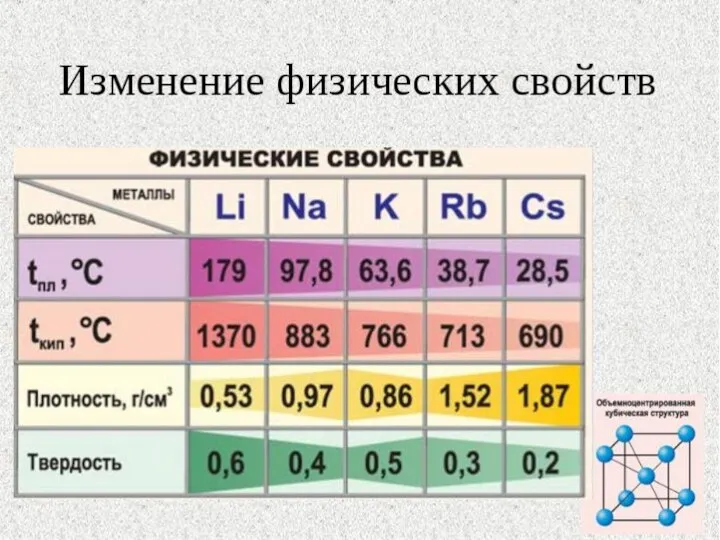
- 16. Серебристо-белые мягкие вещества (режутся ножом), с характерным блеском на свежесрезанной поверхности, кроме цезия (золотистый). Все они
- 18. Химические свойства
- 19. Все щелочные металлы чрезвычайно активны, во всех химических реакциях проявляют восстановительные свойства, отдают свой единственный валентный
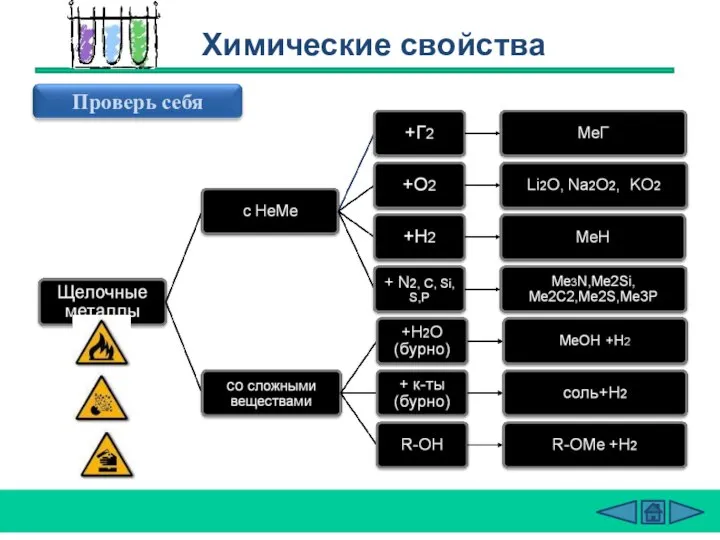
- 20. Химические свойства
- 21. Химические свойства 2Na + Cl2 = 2NaCl (в атмосфере F2 и Cl2 щелочные Me самовоспламеняются) 4Li
- 22. Щелочные металлы способны реагировать с разбавленными кислотами с выделением водорода, однако реакция будет протекать неоднозначно, поскольку
- 23. Взаимодействие с кислотами Me+H2SO4(к)=Me2SO4+H2S+H2O
- 24. Качественное определение щелочных металлов Li+ Na+ K+ Для распознавания соединений щелочных металлов по окраске пламени исследуемое
- 25. Применение металлов и их соединений
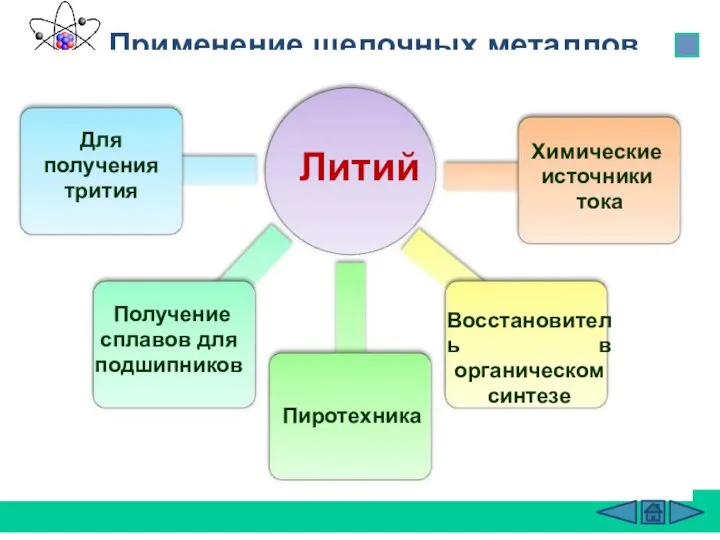
- 26. Применение щелочных металлов Литий Для получения трития Получение сплавов для подшипников Восстановитель в органическом синтезе Химические
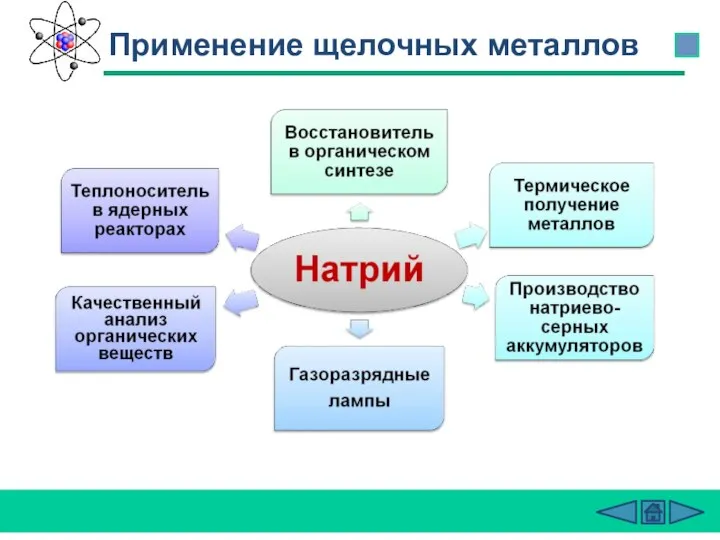
- 27. Применение щелочных металлов
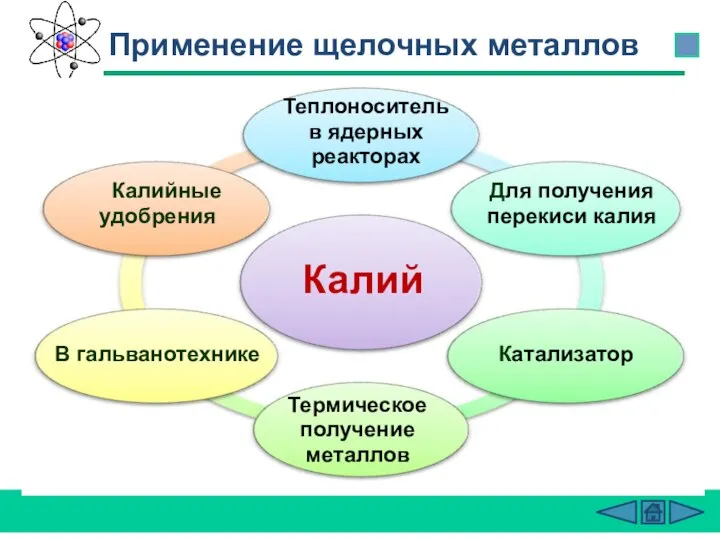
- 28. Применение щелочных металлов Калий В гальванотехнике Калийные удобрения Для получения перекиси калия Катализатор Термическое получение металлов
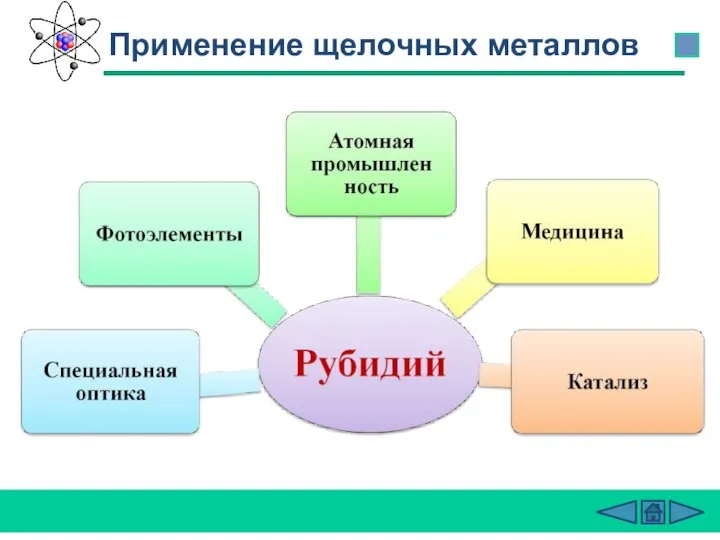
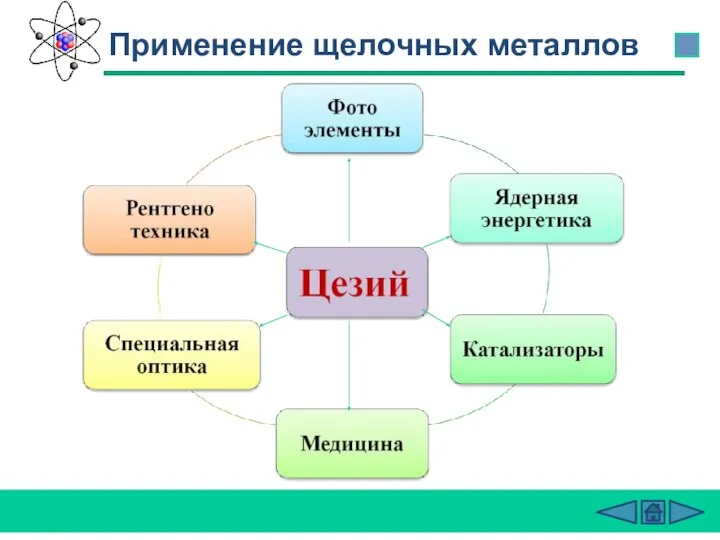
- 29. Применение щелочных металлов
- 30. Применение щелочных металлов
- 31. ОКСИДЫ ЩЕЛОЧНЫХ МЕТАЛЛОВ-ОСНОВНЫЕ Для получения оксидов натрия и калия нагревают смеси гидроксида, пероксида или надпероксида с
- 32. 1. Оксиды щелочных металлов обладают всеми свойствами, присущими основным оксидам: они реагируют с водой, кислотными и
- 33. Гидроксид натрия NаОН в технике известен под названиями едкий натр, каустическая сода, каустик. Техническое название гидроксида
- 34. Соли щелочных металлов — твердые кристаллические вещества ионного строения. . Nа2СO3 — карбонат натрия, образует кристаллогидрат
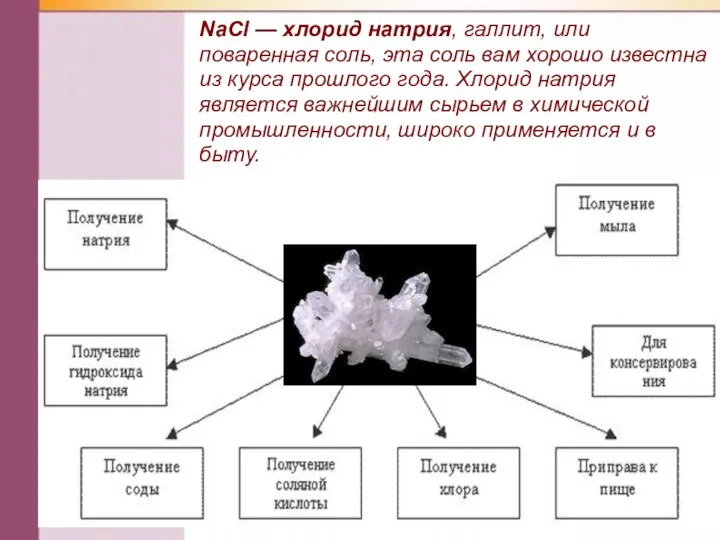
- 36. NаСl — хлорид натрия, галлит, или поваренная соль, эта соль вам хорошо известна из курса прошлого
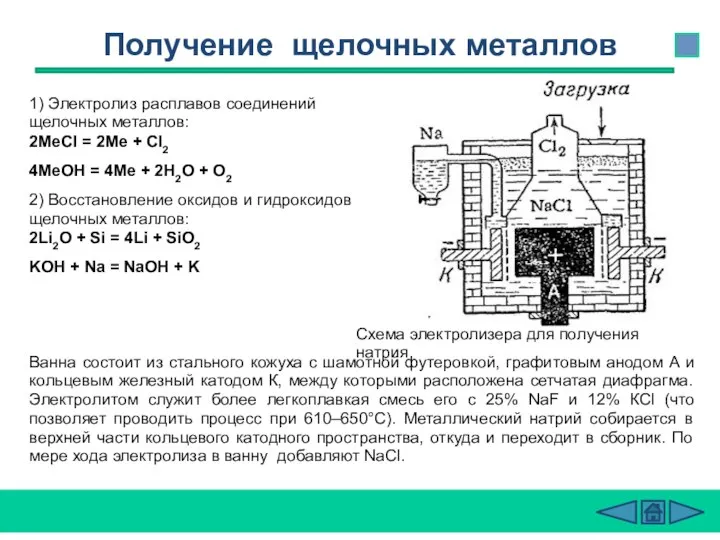
- 37. 1) Электролиз расплавов соединений щелочных металлов: 2МеCl = 2Ме + Cl2 4МеOH = 4Ме + 2Н2О
- 38. Физические свойства щелочных металлов Щелочные металлы - серебристо–белые вещества, за исключением цезия - серебристо-желтого цвета, с
- 39. 1. Предложил назвать калий от арабского «алкали» - щелочь И. Арфведсон Г.Деви Й. Берцеллиус 2. В
- 40. Спасибо за внимание!
- 41. Спасибо за внимание!
- 42. Спасибо за внимание!
- 43. Спасибо за внимание!
- 44. Спасибо за внимание!
- 45. Спасибо за внимание!
- 46. Спасибо за внимание!
- 48. Скачать презентацию



































 Неметаллы. Общая характеристика
Неметаллы. Общая характеристика Каталитический крекинг
Каталитический крекинг Жиры
Жиры Технология лаков и красок
Технология лаков и красок Бериллий (Beryllium) Be
Бериллий (Beryllium) Be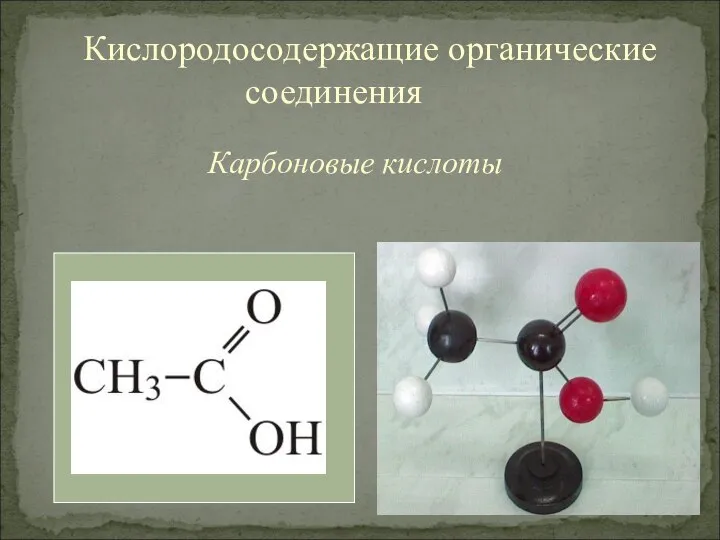 Презентация по Химии "КАРБОНОВЫЕ КИСЛОТЫ" - скачать смотреть
Презентация по Химии "КАРБОНОВЫЕ КИСЛОТЫ" - скачать смотреть  Буландырғыш аппараттарының құрылымдары
Буландырғыш аппараттарының құрылымдары Carbon and the molecular diversity of life. (Chapter 4)
Carbon and the molecular diversity of life. (Chapter 4) Неекономiчний фермент
Неекономiчний фермент Карбоксильные соединения. Гидроксикислоты, кетонокислоты
Карбоксильные соединения. Гидроксикислоты, кетонокислоты Строение углеводородов
Строение углеводородов Коррозия металлов
Коррозия металлов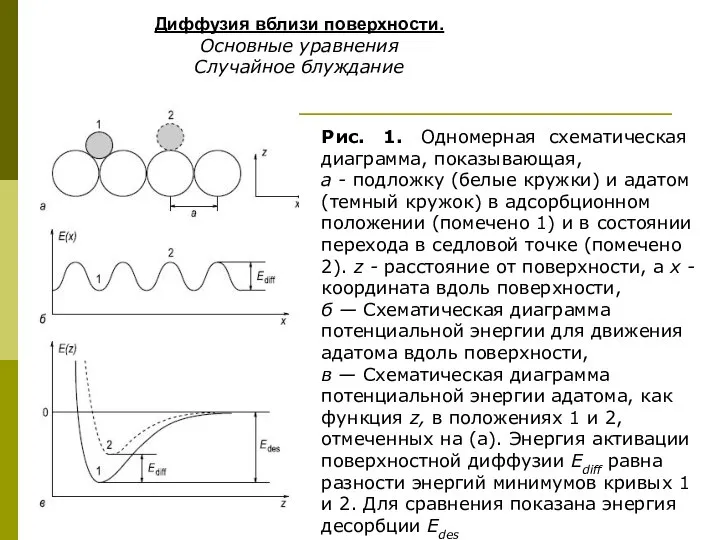 Диффузия вблизи поверхности
Диффузия вблизи поверхности Современные проблемы геологии. Изотопный взгляд на проблему
Современные проблемы геологии. Изотопный взгляд на проблему Методы защиты от коррозии
Методы защиты от коррозии Гидроксилпроизводные углеводородов
Гидроксилпроизводные углеводородов Группа щелочных габброидов
Группа щелочных габброидов Азотная кислота – HNO3 – «взрывоопасная царская особа» МБОУ «Рождественская средняя общеобразовательная школа» Собинско
Азотная кислота – HNO3 – «взрывоопасная царская особа» МБОУ «Рождественская средняя общеобразовательная школа» Собинско Состав и основные свойства янтаря и древесных смол
Состав и основные свойства янтаря и древесных смол Виды присадок к моторному топливу. Керосин
Виды присадок к моторному топливу. Керосин Кадмий
Кадмий Бензол. Тема 11
Бензол. Тема 11 Давайте повторим Заключительный урок в 8 классе
Давайте повторим Заключительный урок в 8 классе  ОВР в гетерогенных системах
ОВР в гетерогенных системах Метаболизм источников энергии
Метаболизм источников энергии Как вырастить кристалл
Как вырастить кристалл Три службы Менделеева для России
Три службы Менделеева для России Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты