Содержание
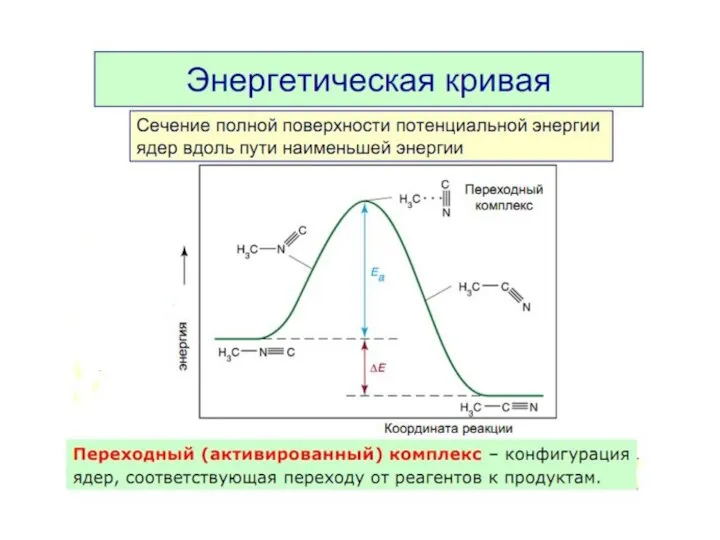
- 8. Энергия активации Еа — это энергия, которую надо сообщить 1 моль вещества, чтобы его молекулы стали
- 15. H2 + I2 = 2HI 1) I2 hν I· + ·I 2) ·I + H–H I
- 24. Формальным порядком реакции называется показатель степени в кинетическом уравнении реакции, определяемый экспериментально. Порядок реакции — это
- 25. Два способа экспериментального определения порядка реакции: 1) составляются кинетические уравнения для реакций 1-го, 2-го и 3-го
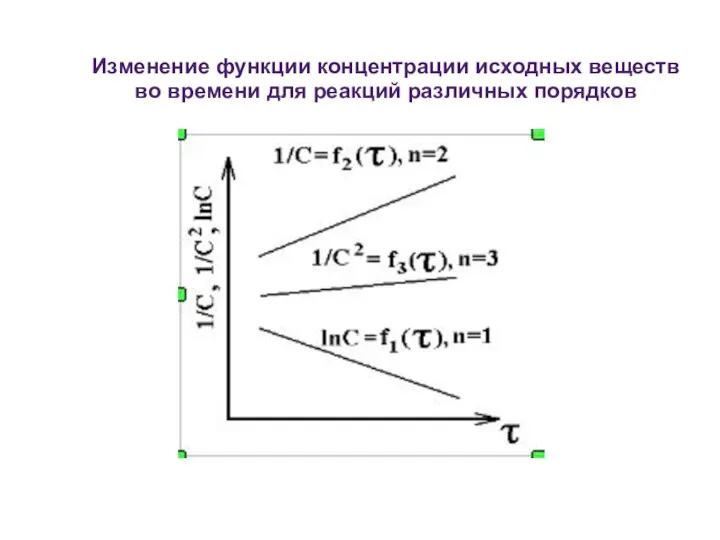
- 26. Изменение функции концентрации исходных веществ во времени для реакций различных порядков
- 27. 2) Используя логарифмическую форму кинетического уравнения r = k·cn , lgr = lgk + n·lgc из
- 28. Молекулярность реакции — число молекул, принимающих участие в элементарном акте химического превращения. Существуют одно-, двух- и
- 29. Зависимость скорости реакции от температуры и природы реагирующих веществ описывает уравнение Аррениуса: k — константа скорости
- 30. Каким образом можно ускорить реакцию? - увеличить температуру - снизить энергию активации Катализаторы — вещества, участвующие
- 31. Энергетическая диаграмма реакции без катализатора и с катализатором.
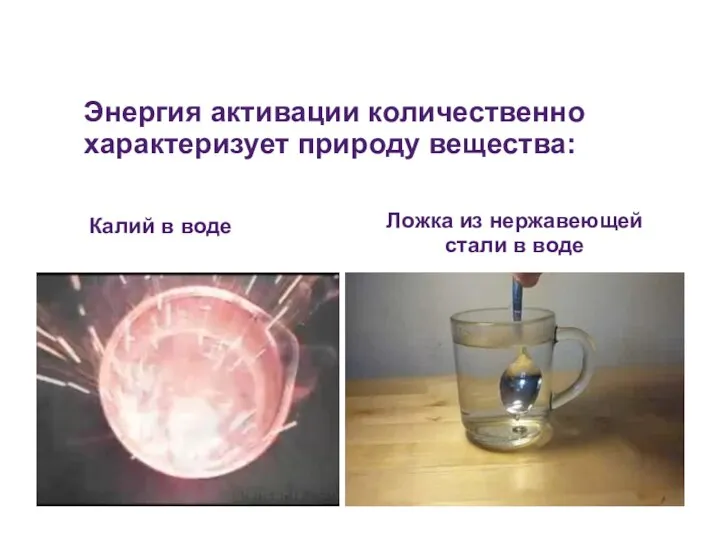
- 32. Энергия активации количественно характеризует природу вещества: Калий в воде Ложка из нержавеющей стали в воде
- 33. Определение энергии активации по константам реакции, определенным при двух температурах:
- 34. Если Еа лежит в диапазоне 50-100 кДж/моль, то влияние температуры на скорость можно оценить по эмпирическому
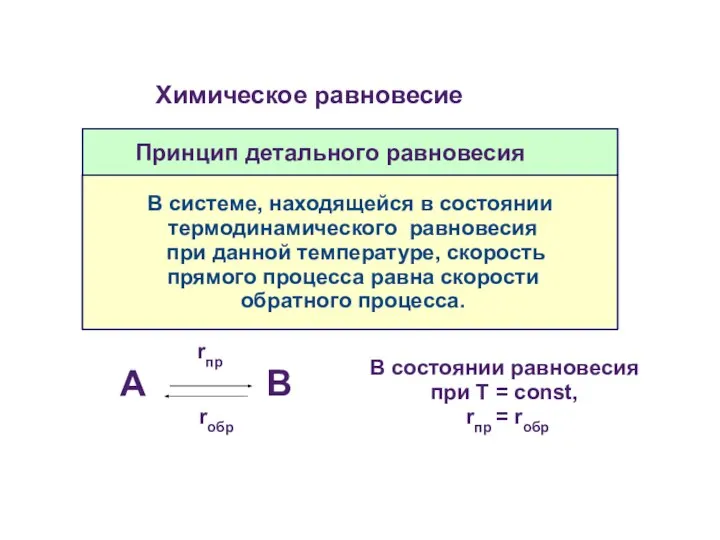
- 35. Принцип детального равновесия В системе, находящейся в состоянии термодинамического равновесия при данной температуре, скорость прямого процесса
- 36. Если на систему, находящуюся в равновесии, оказывается внешнее воздействие (Т, р, С), равновесие системы смещается в
- 37. Задача: В реакции синтеза аммиака исходные концентрации азота и водорода составляли соответственно 5 и 10 моль/л.
- 39. Скачать презентацию





























 Тема: Химическая связь и ее типы Урок химии в 11 классе
Тема: Химическая связь и ее типы Урок химии в 11 классе Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений
Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть
Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть  Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Alkanes. A “family” of hydrocarbons
Alkanes. A “family” of hydrocarbons Фенол Подготовил Ежов Сергей
Фенол Подготовил Ежов Сергей Орагническая химия. Теория А.М. Бутлерова
Орагническая химия. Теория А.М. Бутлерова Продолжение лекции «Химическая связь»
Продолжение лекции «Химическая связь»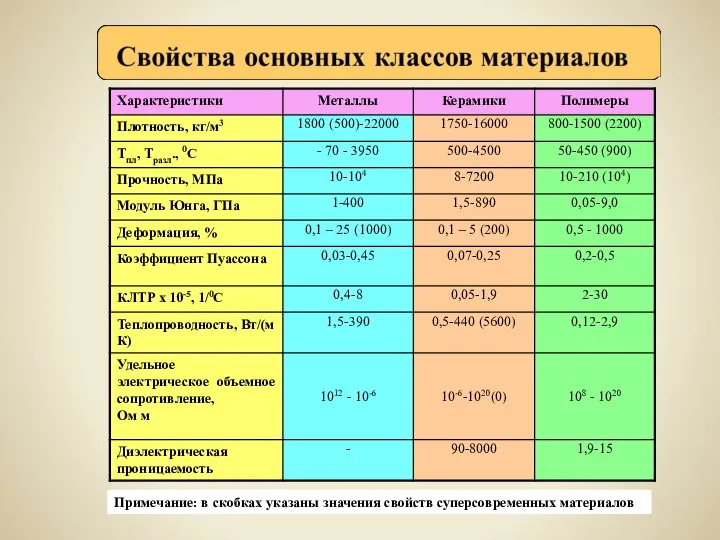 Свойства основных классов материалов
Свойства основных классов материалов Алканы и алкены
Алканы и алкены Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение Логическая структура модуля по дисциплине Аналитическая химия
Логическая структура модуля по дисциплине Аналитическая химия Аммофос өндірісі. Алыну әдісі
Аммофос өндірісі. Алыну әдісі Лабораторные занятия по теме: Методы защиты электрооборудования от коррозии
Лабораторные занятия по теме: Методы защиты электрооборудования от коррозии Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Гидролиз солей. Составила: Рудчинкова Л.Ю., учитель химии и биологии МОУ «СОШ им. М.М. Рудченко с. Перелюб Перелюбского района Сарато
Гидролиз солей. Составила: Рудчинкова Л.Ю., учитель химии и биологии МОУ «СОШ им. М.М. Рудченко с. Перелюб Перелюбского района Сарато Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Межкристаллитная коррозия МКК
Межкристаллитная коррозия МКК Механизмы двухсубстатных реакций
Механизмы двухсубстатных реакций Начала физической химии
Начала физической химии Альдегиды и кетоны: свойства, получение, применение
Альдегиды и кетоны: свойства, получение, применение Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом
Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом Липиды. Классификация липидов
Липиды. Классификация липидов Орбитали и связи
Орбитали и связи Общая и медицинская химия
Общая и медицинская химия Циклоалканы. Строение, изомерия, получение и свойства
Циклоалканы. Строение, изомерия, получение и свойства Белки. Структуры белков
Белки. Структуры белков