Содержание
- 3. Соли аммония Ион аммония по размерам и заряду близок к ионам щелочных металлов, поэтому соли аммония
- 6. 3.Разложение солей аммония при нагревании а)Соли летучих кислот: NH4Cl = NH3 + HCl (NH4)2CO3 = 2NH3
- 7. 3.Разложение солей аммония при нагревании б) Cоли нелетучих кислот: (NH4)2SO4 = NH4HSO4 + NH3↑ (NH4)3PO4 =
- 8. 3.Разложение солей аммония при нагревании в) Соли с анионом-окислителем: (NH4)2Cr2O7 = N2↑ + Cr2O3 + 4H2O
- 14. Скачать презентацию











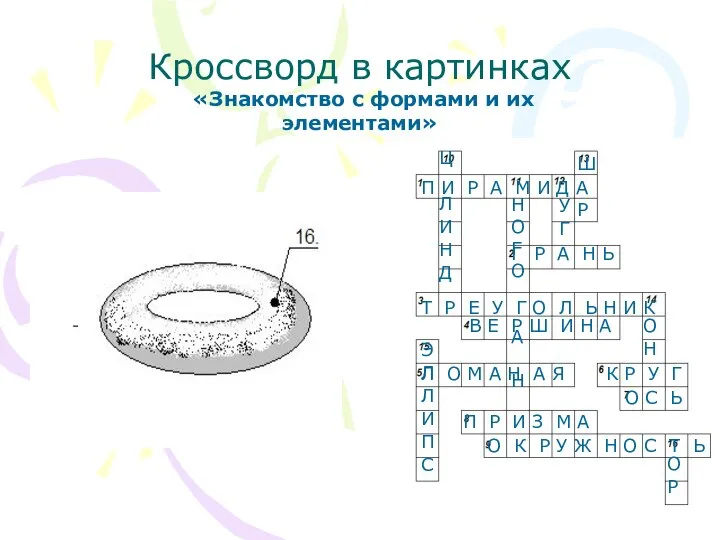 Кроссворд в картинках. Знакомство с формами и их элементами
Кроссворд в картинках. Знакомство с формами и их элементами Презентация к уроку по теме: «Алканы» Учитель химии Колесникова Г.Т.
Презентация к уроку по теме: «Алканы» Учитель химии Колесникова Г.Т. IVA группа С, Si, Ge, Sn, Pb (подгруппа титана)
IVA группа С, Si, Ge, Sn, Pb (подгруппа титана) Зависимость свойств веществ от их строения. Химическая связь. Основные виды химической связи
Зависимость свойств веществ от их строения. Химическая связь. Основные виды химической связи Определение химического состава почвы пришкольного участка
Определение химического состава почвы пришкольного участка Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар
Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар Алкены. Пропилен
Алкены. Пропилен Каталіз: каталітичне гідрування
Каталіз: каталітичне гідрування Класифікація, будова та номенклатура органічних сполук
Класифікація, будова та номенклатура органічних сполук Газификация тяжёлых нефтяных остатков. Конверсия природного газа
Газификация тяжёлых нефтяных остатков. Конверсия природного газа Основы химической термодинамики
Основы химической термодинамики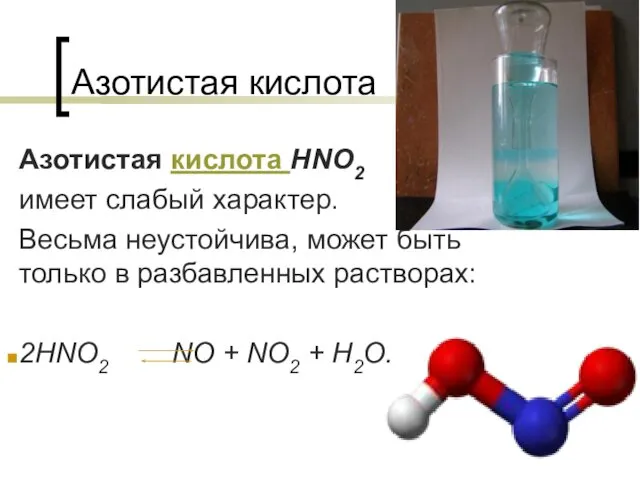 Азотистая кислота
Азотистая кислота Кислоты, основания, соли в свете ТЭД подготовила: Мартынова Е.Ю._
Кислоты, основания, соли в свете ТЭД подготовила: Мартынова Е.Ю._ Непредельные углеводороды: этилен
Непредельные углеводороды: этилен Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии»
Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии» Коллоидная химия
Коллоидная химия Изоморфизм, изоморфизмнің түрлері. Полиморфизм. Сульфидтер класының жалпы сипаттамасы
Изоморфизм, изоморфизмнің түрлері. Полиморфизм. Сульфидтер класының жалпы сипаттамасы Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Полимеры и их использование
Полимеры и их использование Важнейшие минералы
Важнейшие минералы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химическая кинетика
Химическая кинетика Презентация по Химии "Изотопы" - скачать смотреть
Презентация по Химии "Изотопы" - скачать смотреть  Презентация по Химии "Д.И. Менделеев – основоположник русской агрохимии" - скачать смотреть
Презентация по Химии "Д.И. Менделеев – основоположник русской агрохимии" - скачать смотреть  Кристалічні та аморфні тіла. Рідкі кристали та їх властивості. Підготувала учениця 10 класу Стрельчук Катерина
Кристалічні та аморфні тіла. Рідкі кристали та їх властивості. Підготувала учениця 10 класу Стрельчук Катерина  Полипропилен
Полипропилен