Содержание
- 2. Теория химического строения Бутлеров Александр Михайлович 1861г Свойства веществ зависят не только от их состава, но
- 3. Электронный эффект Смещение электронной плотности по системе химических связей, вызванное присутствием заместителя, отличающегося электроотрицательностью (ЭО) от
- 4. Индуктивный эффект ( I ) Передача электронного влияния заместителя по цепи σ-связей. Передаётся по цепи σ-связей
- 5. Графически индуктивный эффект обозначается стрелкой по валентному штриху в сторону более ЭО атома: +I -I СН3
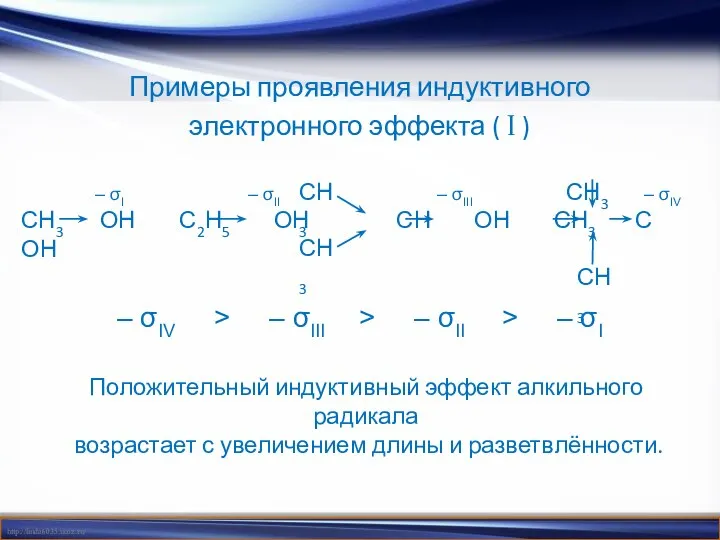
- 6. Примеры проявления индуктивного электронного эффекта ( I ) – σIV > – σIII > – σII
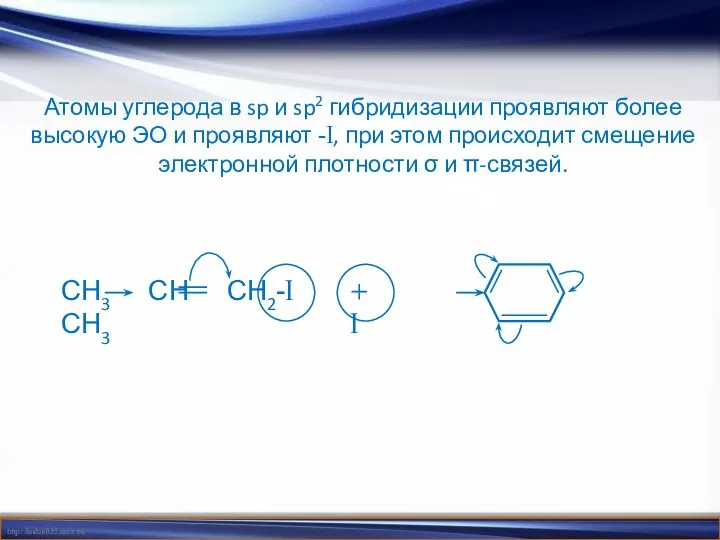
- 7. Атомы углерода в sp и sp2 гибридизации проявляют более высокую ЭО и проявляют -I, при этом
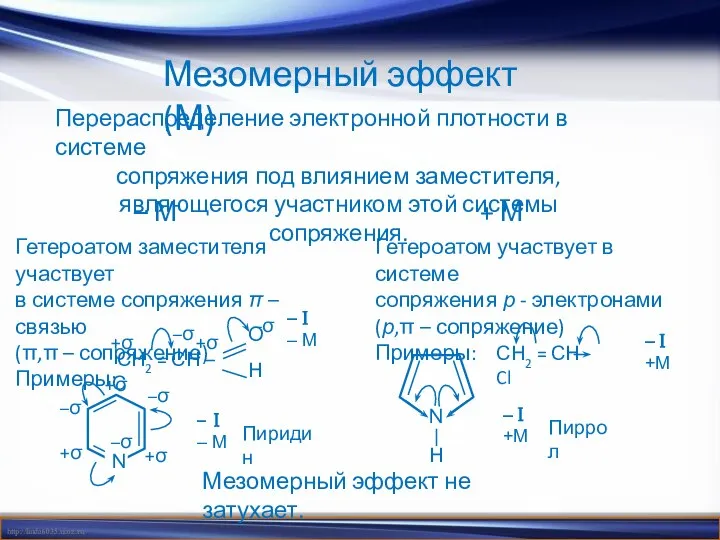
- 8. Мезомерный эффект (М) Перераспределение электронной плотности в системе сопряжения под влиянием заместителя, являющегося участником этой системы
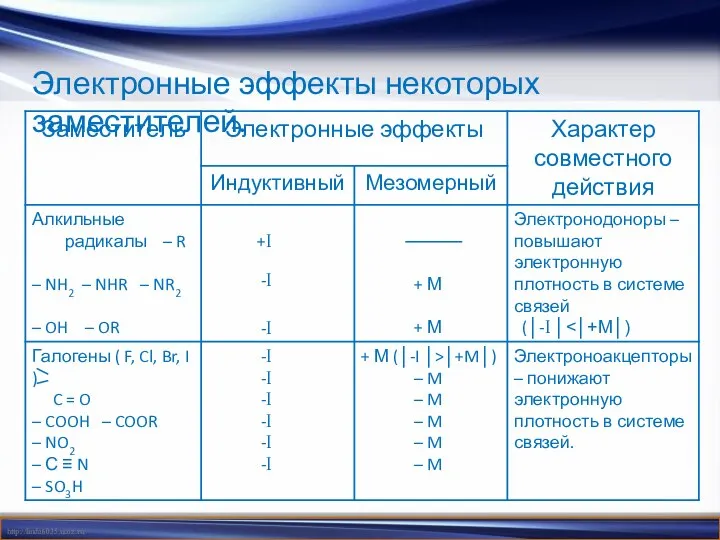
- 9. Электронные эффекты некоторых заместителей.
- 10. Протолитическая теория Бренстеда - Лоури Протолиты Кислоты Основания Амфолиты Нейтральные молекулы или ионы, способные отдавать протон
- 11. Кислотно – основное взаимодействие НА + В А – + ВН+ кислота основание сопряжённое основание сопряжённая
- 12. Качественная оценка силы кислоты определяется стабильностью сопряжённого основания (аниона). Факторы, обуславливающие стабильность аниона: I Природа атома
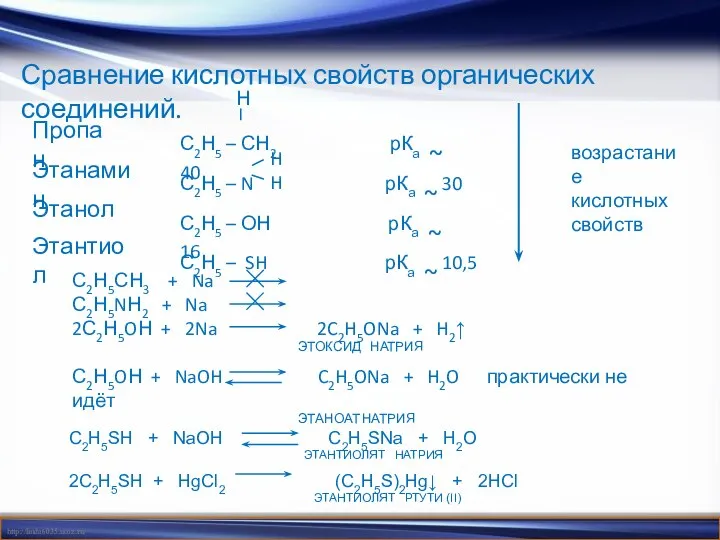
- 13. Сравнение кислотных свойств органических соединений. Пропан С2Н5 – СН2 рКа ~ 40 Н возрастание кислотных свойств
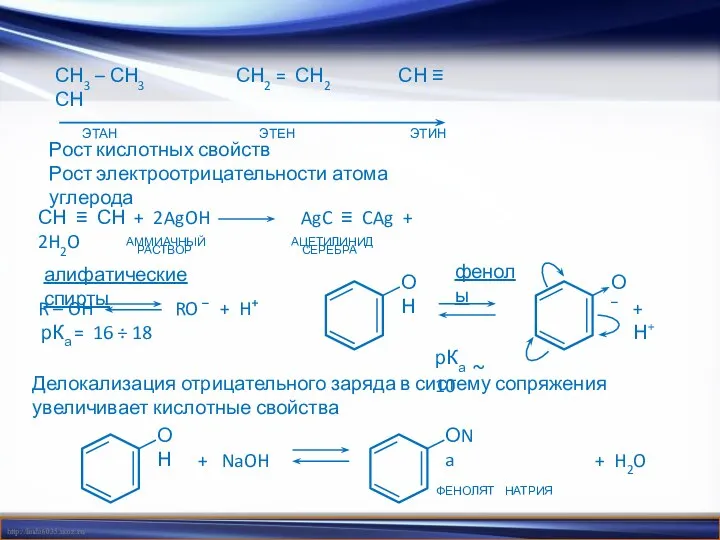
- 14. СН3 – СН3 СН2 = СН2 СН ≡ СН ЭТАН ЭТЕН ЭТИН Рост кислотных свойств Рост
- 15. Карбоновые кислоты проявляют наиболее высокие кислотные свойства Влияние радикала на карбоксильную группу приводит к изменению кислотных
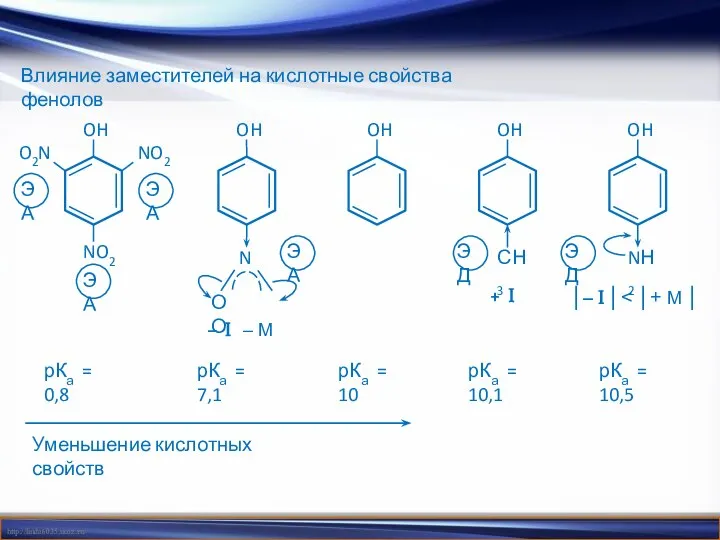
- 16. Влияние заместителей на кислотные свойства фенолов Уменьшение кислотных свойств O2N NO2 NO2 N О О –
- 17. Основание Бренстеда Присоединяют протон с образованием солей. Сила основания определяется доступностью для протона пары электронов гетероатома.
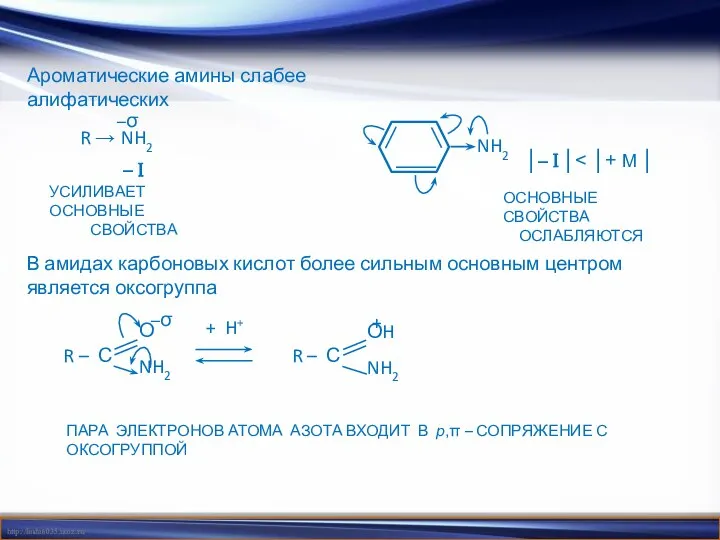
- 18. Ароматические амины слабее алифатических В амидах карбоновых кислот более сильным основным центром является оксогруппа R →
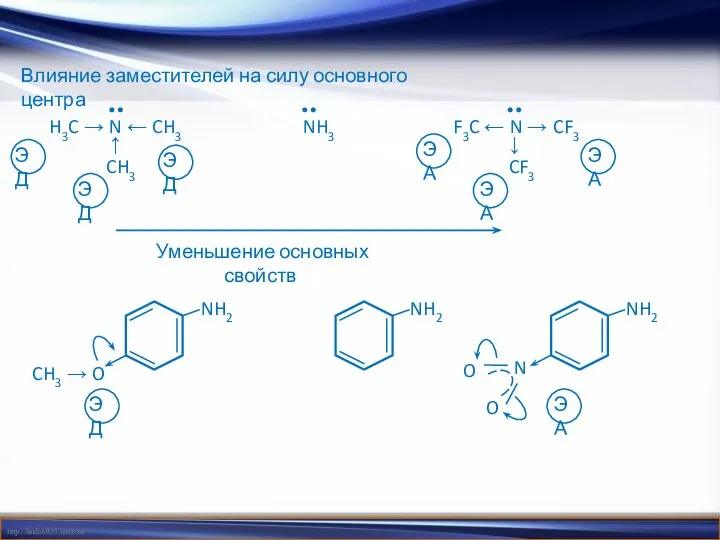
- 19. Влияние заместителей на силу основного центра Уменьшение основных свойств H3C → N ← CH3 ↑ CH3
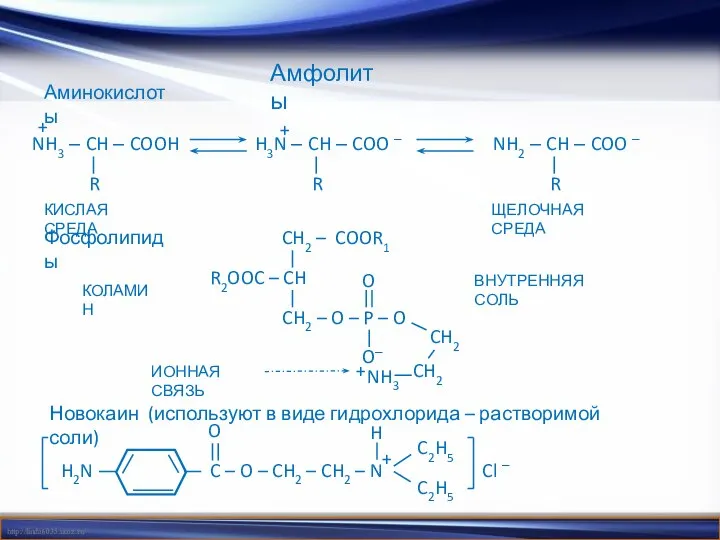
- 20. Амфолиты Аминокислоты Фосфолипиды Новокаин (используют в виде гидрохлорида – растворимой соли) + NH3 – CH –
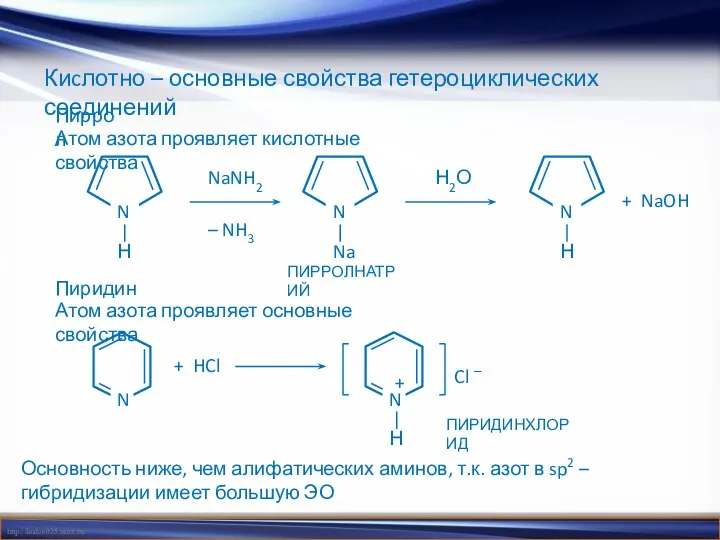
- 21. Киcлотно – основные свойства гетероциклических соединений Пиррол Атом азота проявляет кислотные свойства Пиридин Атом азота проявляет
- 23. Скачать презентацию









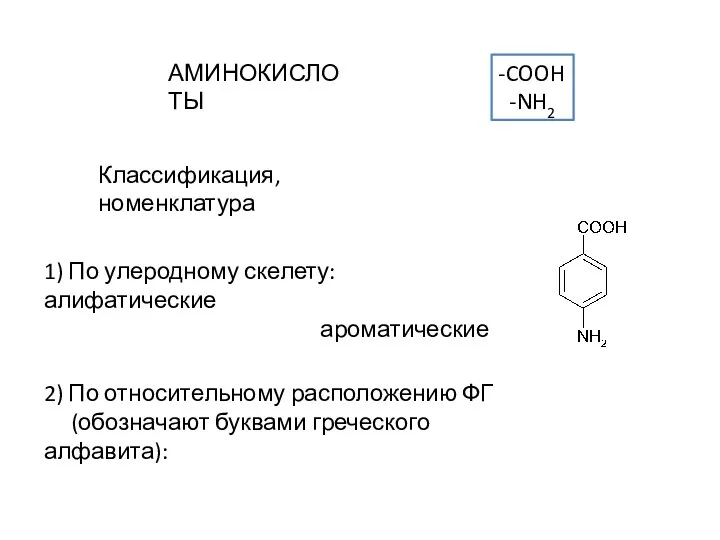 Аминокислоты. Классификация, номенклатура
Аминокислоты. Классификация, номенклатура Фазовые равновесия
Фазовые равновесия Электролитическая диссоциация
Электролитическая диссоциация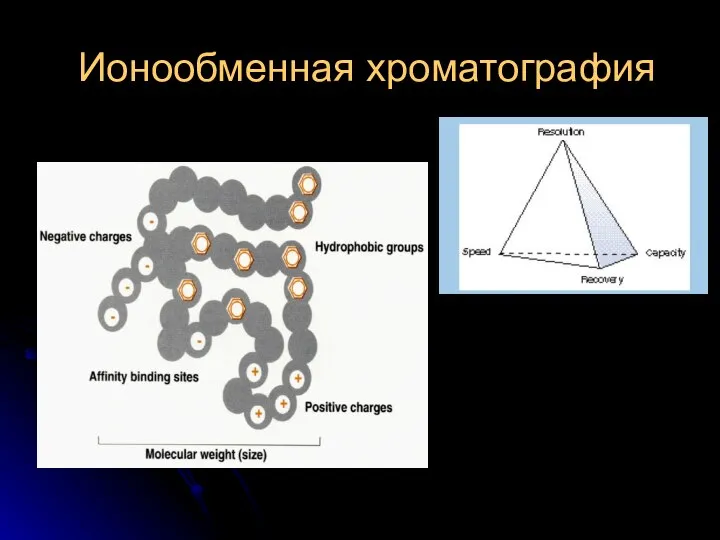 Ионообменная хроматография
Ионообменная хроматография Мұнай құрамындағы тұздың мөлшерін анықтау
Мұнай құрамындағы тұздың мөлшерін анықтау Биохимия печени
Биохимия печени Потенциометрия. Методы потенциометрии, и их применение в медицине. Плюсы и минусы методов ПТ
Потенциометрия. Методы потенциометрии, и их применение в медицине. Плюсы и минусы методов ПТ Кристаллические решетки
Кристаллические решетки Атомные спектры
Атомные спектры Азотная кислота и ее соли. Раскаленный уголек, брошенный в концентрированную азотную кислоту, продолжает гореть, при этом выде
Азотная кислота и ее соли. Раскаленный уголек, брошенный в концентрированную азотную кислоту, продолжает гореть, при этом выде Высокопроизводительное моторное масло для бензиновых и дизельных двигателей
Высокопроизводительное моторное масло для бензиновых и дизельных двигателей Добавки, красители и консерванты в пищевых продуктах
Добавки, красители и консерванты в пищевых продуктах «Адамсит». Дигидрофенарсазинхлорид HN(C6H4)2AsCl
«Адамсит». Дигидрофенарсазинхлорид HN(C6H4)2AsCl Метасоматический процесс
Метасоматический процесс Относительная атомная масса
Относительная атомная масса Адские задания. ЕГЭ по химии
Адские задания. ЕГЭ по химии Презентация по Химии "Хімія в повсякденному житті" - скачать смотреть бесплатно
Презентация по Химии "Хімія в повсякденному житті" - скачать смотреть бесплатно Классификация неорганических веществ
Классификация неорганических веществ Ферроцен. Свойства, получение и применение
Ферроцен. Свойства, получение и применение Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ
Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ Спирт. Спирты в природе. Влияние спирта на человека
Спирт. Спирты в природе. Влияние спирта на человека Физические и химические свойства воды
Физические и химические свойства воды Электрохимические методы. (Лекция 3)
Электрохимические методы. (Лекция 3) Такая знакомая сода
Такая знакомая сода Электролиз. 9 класс
Электролиз. 9 класс Биохимия лёгких
Биохимия лёгких Кафедры биохимии УГМУ в прошлом и настоящем
Кафедры биохимии УГМУ в прошлом и настоящем Состав вещества
Состав вещества