Содержание
- 2. Атом - наименьшая частица химического элемента, сохраняющая все его химические свойства Молекула - наименьшая частица вещества,
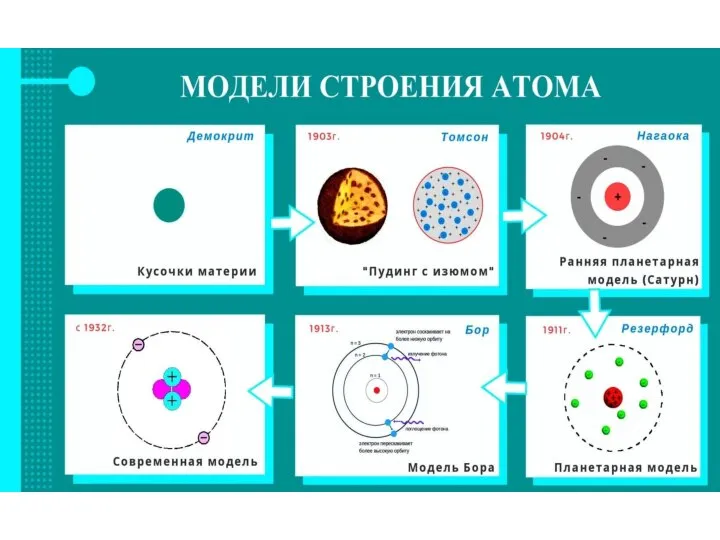
- 3. Первые представления о том, что вещество состоит из отдельных неделимых частиц, появились в глубокой древности. Атомизм
- 5. Официально утверждено в 1860 году на международном съезде химиков
- 7. Долгое время господствовало мнение, что атомы неделимы. Однако в конце 19 века был установлен ряд факторов,
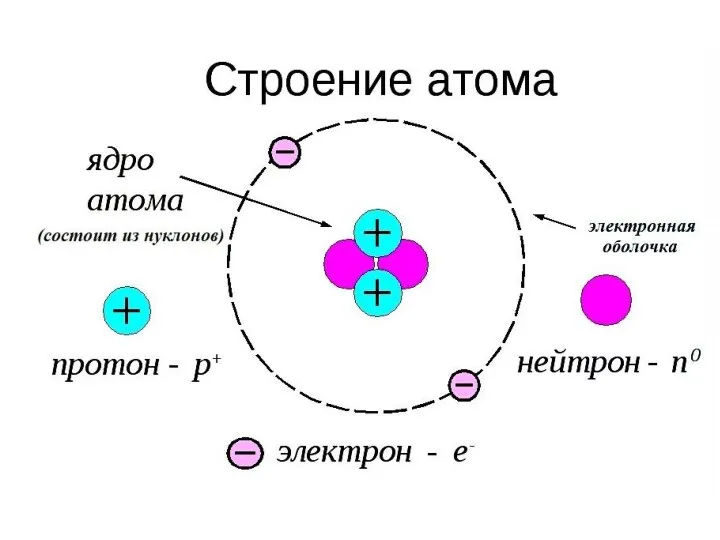
- 10. Сумма масс протонов и нейтронов называется массовым числом атома (ядра) и выражает его атомную массу: p+
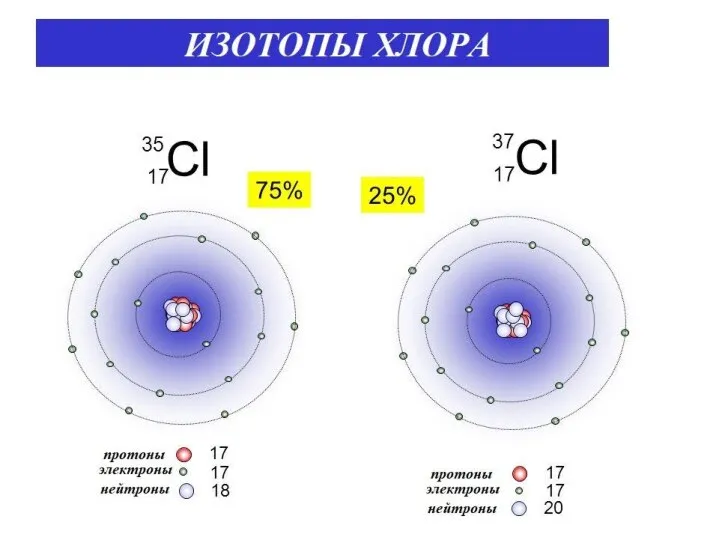
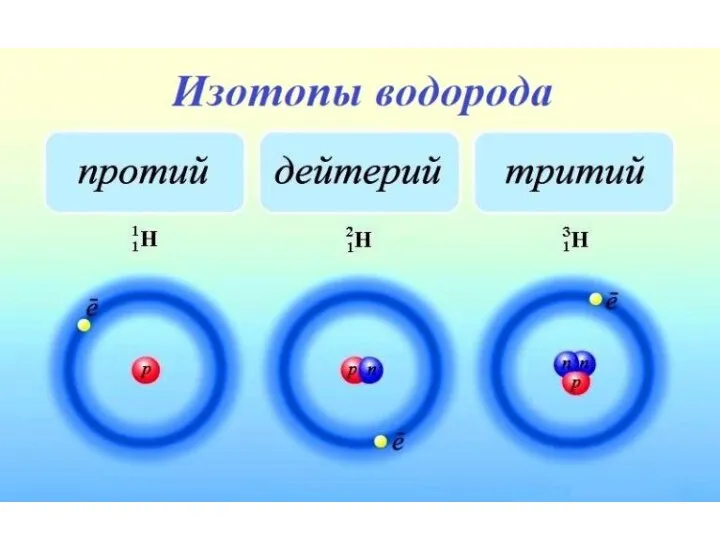
- 11. Изотопы - атомы одного и того же элемента с разной массой. Ядра этих атомов содержат одинаковое
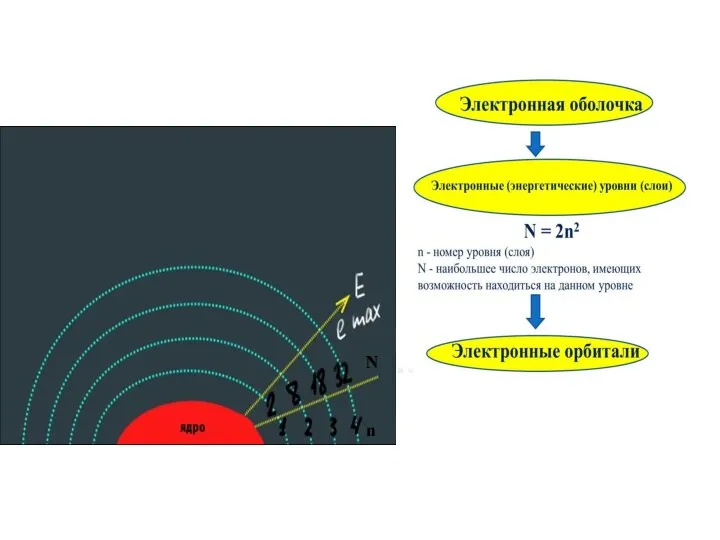
- 14. Электронная оболочка атома распадается на несколько энергетических уровней (слоёв). Электроны каждого следующего слоя находятся на более
- 15. n N
- 16. Для характеристики атомных орбиталей используют квантовые числа, которые полностью описывают состояние электронов в атоме. Главное квантовое
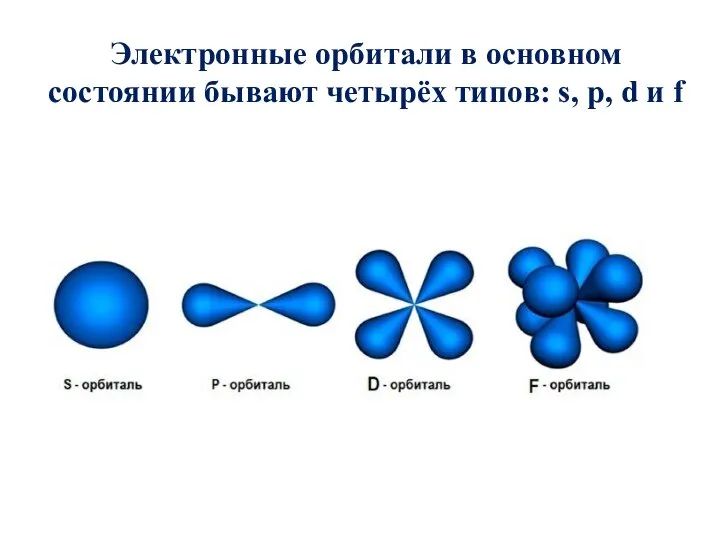
- 17. Электронные орбитали в основном состоянии бывают четырёх типов: s, p, d и f
- 18. На первом энергетическом уровне (n = 1) орбитальное квантовое число l принимает единственное значение l =
- 19. Магнитное квантовое число (ml) характеризует положение электронной орбитали в пространстве и принимает целочисленные значения от -l
- 20. Спиновое квантовое число (ms) характеризует магнитный момент, возникающий при вращении электрона вокруг своей оси. Принимает только
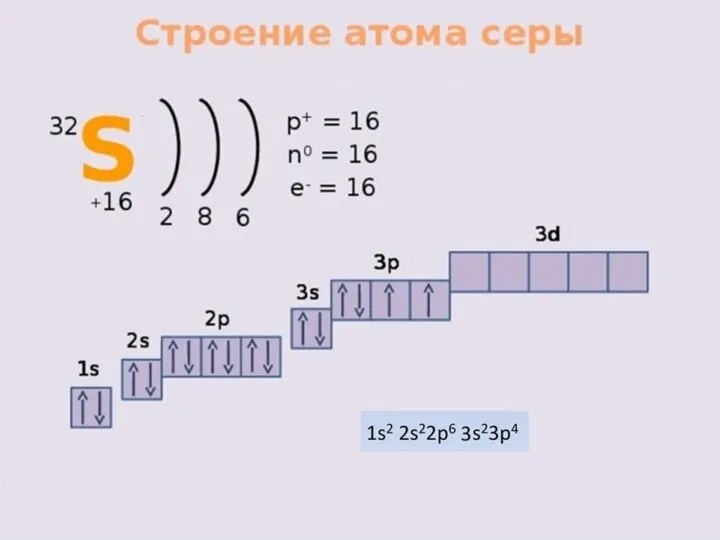
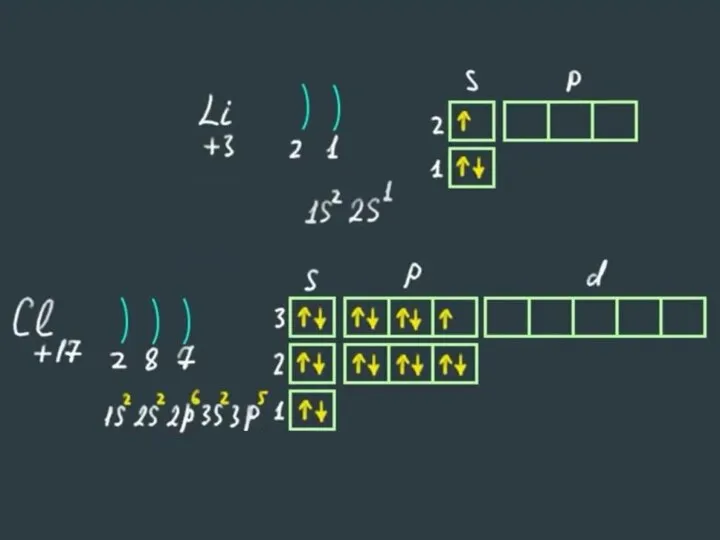
- 21. Строение энергетических уровней
- 22. Правила заполнения электронных орбиталей: 1. Сначала заполняются орбитали с наименьшей энергией, и только после этого переходят
- 23. Порядковый номер в Периодической системе Д.И. Менделеева - важнейшая константа элемента, выражающая: а) число протонов в
- 24. Алгоритм составления электронных формул строения атомов Записываем знак химического элемента и заряд ядра его атома (№
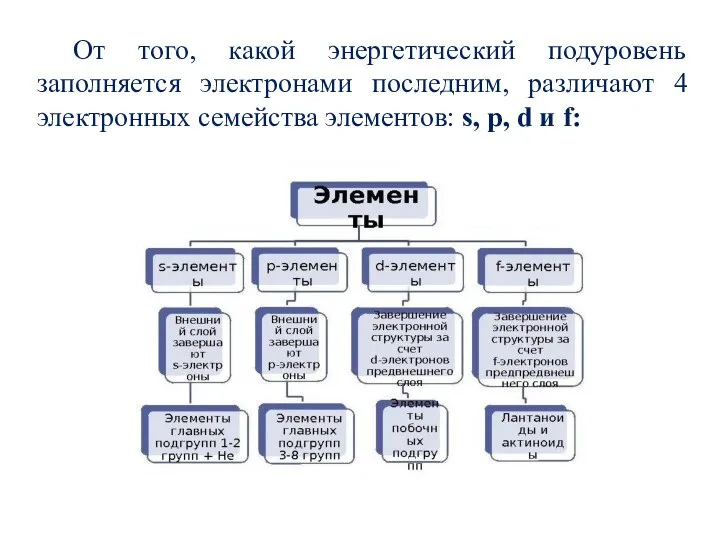
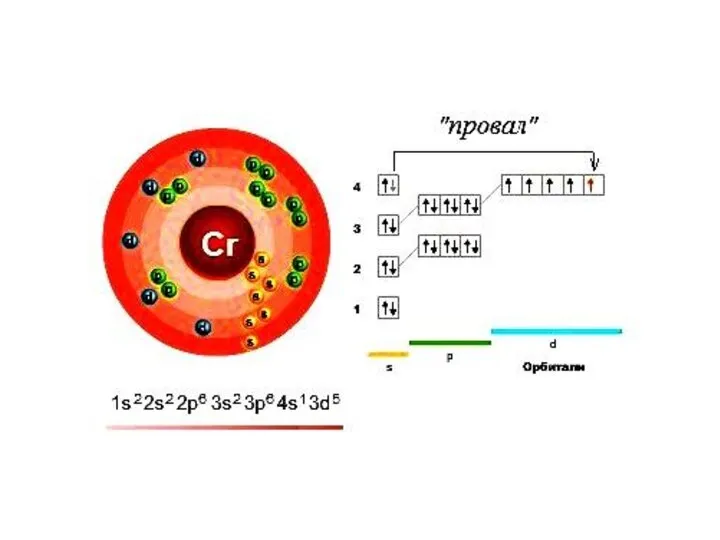
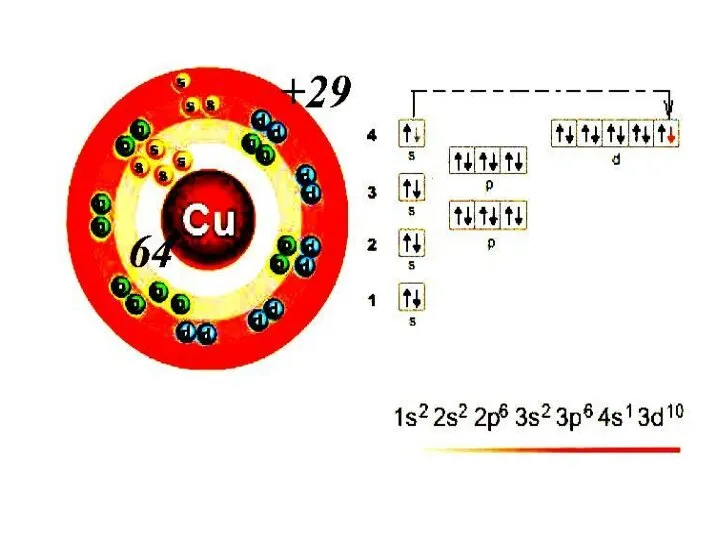
- 28. От того, какой энергетический подуровень заполняется электронами последним, различают 4 электронных семейства элементов: s, p, d
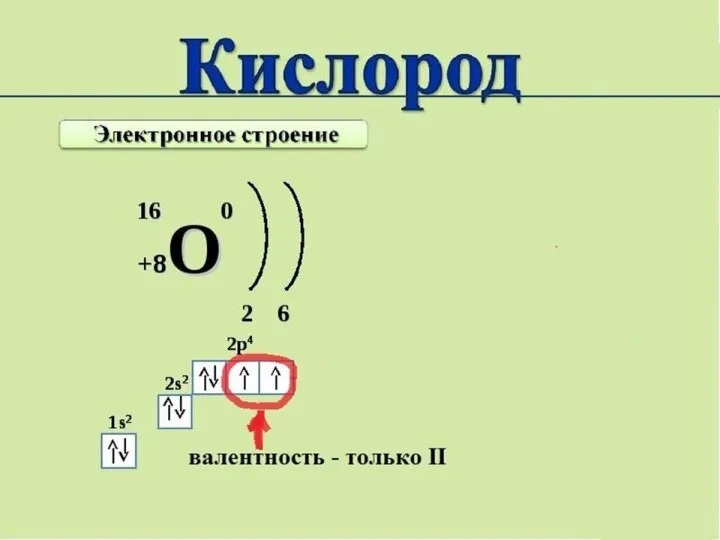
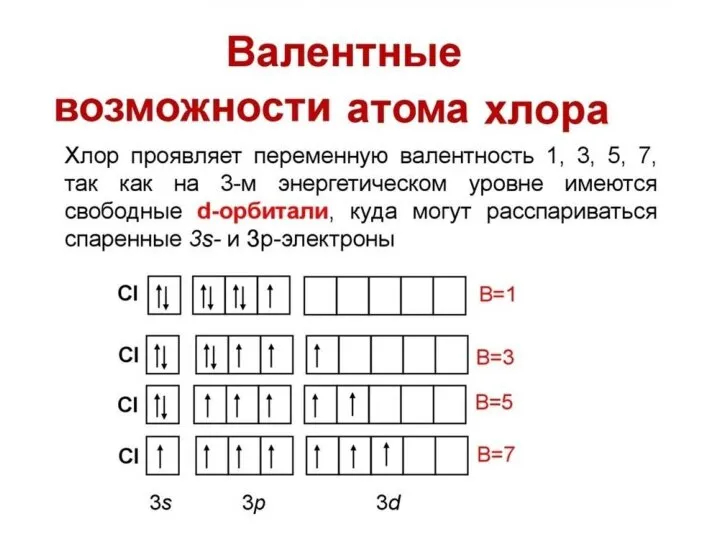
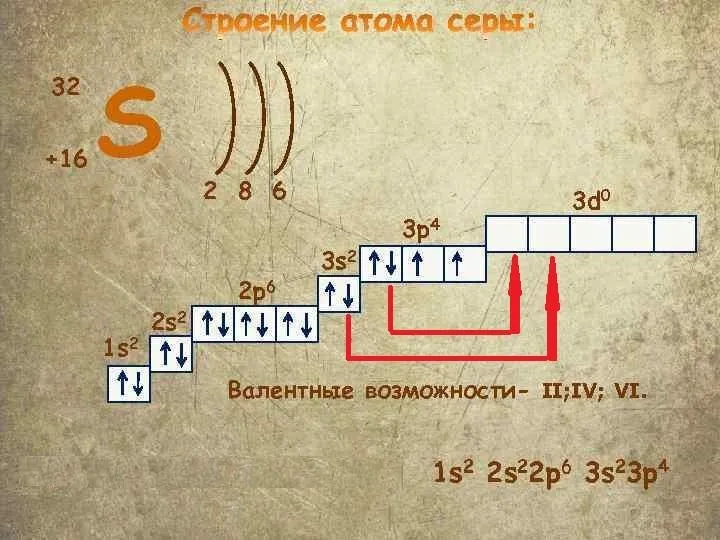
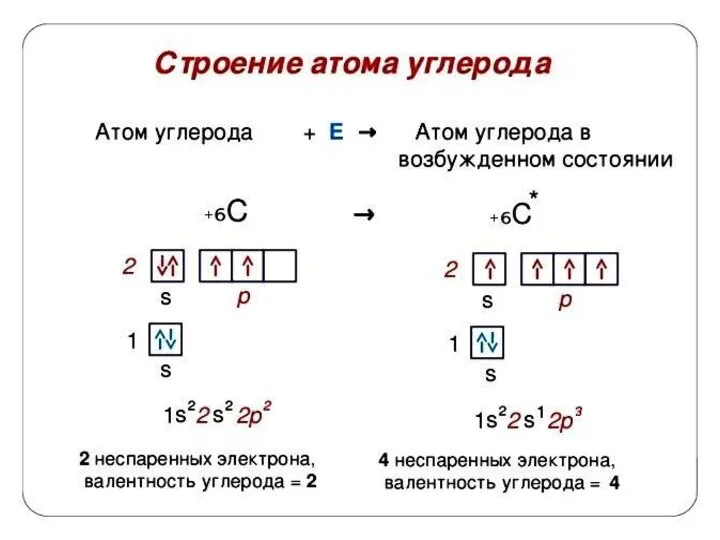
- 32. Валентность атома химического элемента определяется, в первую очередь, числом неспаренных электронов, принимающих участие в образовании химической
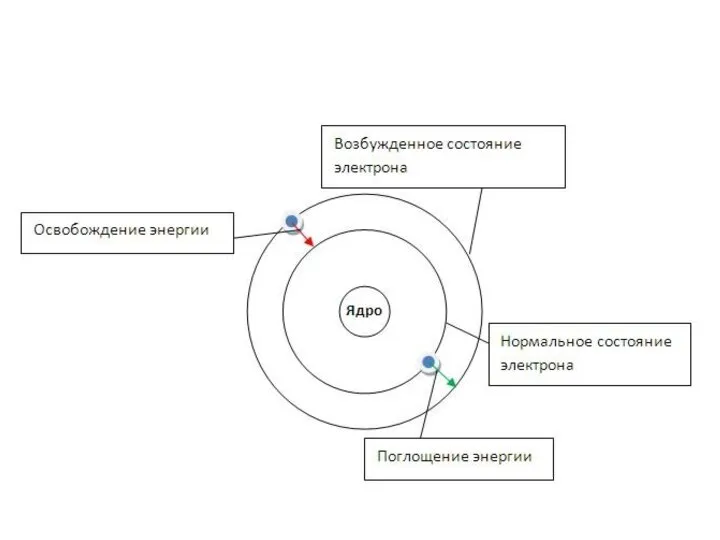
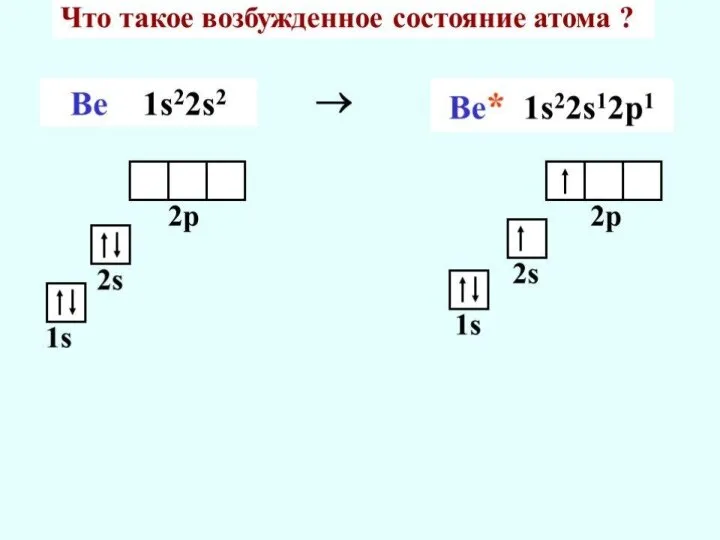
- 34. Атомы устойчивы лишь в некоторых стационарных состояниях, которым отвечают определённые значения энергии. Наинизшее из разрешённых энергетических
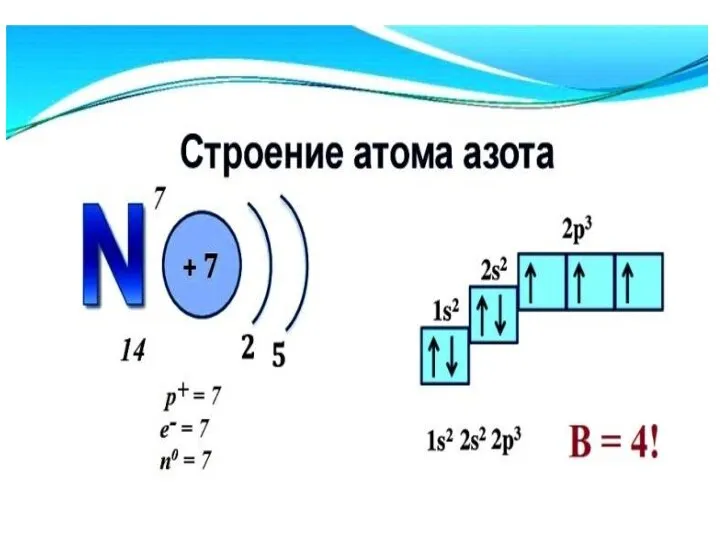
- 42. Азот находится во втором периоде главной подгруппы V группы Периодической системы химических элементов. Его электронная конфигурация
- 44. Скачать презентацию























 Виды частиц в органической химии. Типы реакций
Виды частиц в органической химии. Типы реакций Предельные углеводороды. Насыщенные алифатические углеводороды. Алканы или Парафины
Предельные углеводороды. Насыщенные алифатические углеводороды. Алканы или Парафины Нуклеиновые кислоты
Нуклеиновые кислоты Ситуационная задача по биохимии
Ситуационная задача по биохимии Зат алмасу
Зат алмасу Процессы комплексообразования
Процессы комплексообразования Практическая работа. Химический состав клетки
Практическая работа. Химический состав клетки Голубое золото
Голубое золото Карбон Характеристика елемента та утворених ним сполук, кругообіг елемента в природі
Карбон Характеристика елемента та утворених ним сполук, кругообіг елемента в природі  Вода: строение, свойства и значение
Вода: строение, свойства и значение Альдегиды и кетоны: свойства, получение, применение
Альдегиды и кетоны: свойства, получение, применение Органическое часть почвы
Органическое часть почвы Молекулярно-кинетические свойства
Молекулярно-кинетические свойства Методы разделения и концентрирования. Хроматографические методы
Методы разделения и концентрирования. Хроматографические методы Растительное сырье содержащее флавоноиды
Растительное сырье содержащее флавоноиды Презентация по Химии "Знаки химических элементов" - скачать смотреть
Презентация по Химии "Знаки химических элементов" - скачать смотреть  Презентация по Химии "Виды газовых разрядов" - скачать смотреть
Презентация по Химии "Виды газовых разрядов" - скачать смотреть  Вода. Твердість води
Вода. Твердість води  Вода та її властивості
Вода та її властивості Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов
Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов Современные сплавы на основе циркония
Современные сплавы на основе циркония Классификация топлива, масел и спецжидкостей
Классификация топлива, масел и спецжидкостей Цвет и другие диагностические признаки осадочных пород
Цвет и другие диагностические признаки осадочных пород Номенклатура и изомерия Соловова Е.А., учитель химии высшей квалификационной категории МОУ «СОШ №15 г. Балашова Саратовской облас
Номенклатура и изомерия Соловова Е.А., учитель химии высшей квалификационной категории МОУ «СОШ №15 г. Балашова Саратовской облас Алкины (Ацетилены)
Алкины (Ацетилены) Знание химии в строительном деле на бытовом уровне
Знание химии в строительном деле на бытовом уровне Химическая реакция
Химическая реакция Алкены
Алкены