Содержание
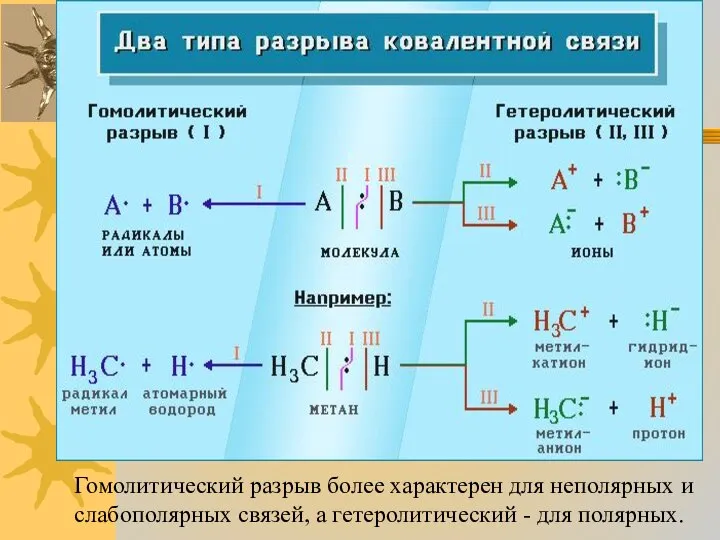
- 2. Классификация реакций по механизму разрыва связей В зависимости от способа разрыва ковалентной связи в реагирующей молекуле
- 3. Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим:
- 5. Гомолитический разрыв более характерен для неполярных и слабополярных связей, а гетеролитический - для полярных.
- 6. Органические ионы и радикалы Органические катионы, анионы и свободные радикалы являются неустойчивыми промежуточными частицами. Они возникают
- 7. Органические ионы и радикалы От устойчивости промежуточных частиц зависит направление реакции. Чем ниже энергия промежуточной частицы
- 9. Радикальные реакции Реакции, в которых происходит гомолитический разрыв связей и образуются свободно-радикальные промежуточные частицы, называются радикальными
- 10. Радикальные реакции Реакции с участием свободных радикалов характерны для соединений с неполярными и слабополярными связями. Такие
- 11. Ионные реакции Реакции, в которых происходит гетеролитический разрыв связей и образуются промежуточные частицы ионного типа, называются
- 12. Общая схема реакции: (CH3)3C-Cl + H2O → (CH3)3C-OH + HCl Стадии процесса:
- 13. Органические катионы и анионы - неустойчивые промежуточные частицы. В отличие от неорганических ионов, постоянно присутствующих в
- 14. Электрофильные реакции Электрофильной называется реакция, в которой молекула органического вещества подвергается действию электрофильного реагента. Электрофильные ("любящие
- 15. Электрофильное присоединение: CH2=CH2 + HCl → CH3CH2Cl (электрофил - H+ в составе HCl) Стадии: I. CH2=CH2
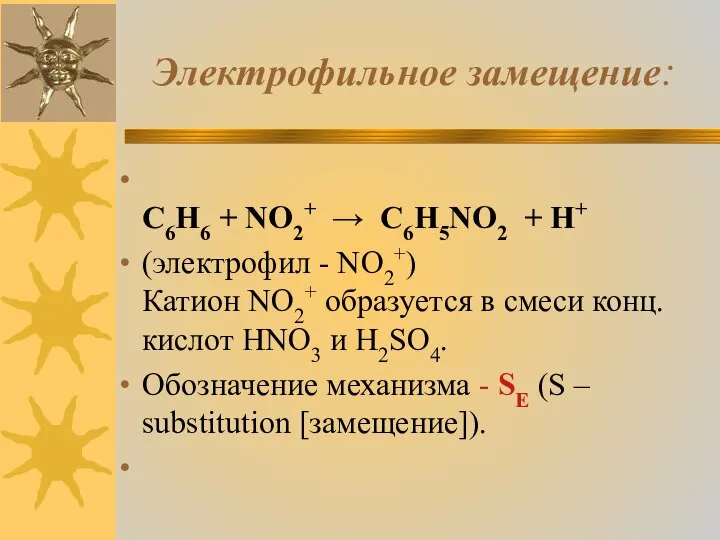
- 16. Электрофильное замещение: C6H6 + NO2+ → C6H5NO2 + H+ (электрофил - NO2+) Катион NO2+ образуется в
- 17. Нуклеофильные реакции Нуклеофильной называется реакция, в которой молекула органического вещества подвергается действию нуклеофильного реагента. Нуклеофильные ("любящие
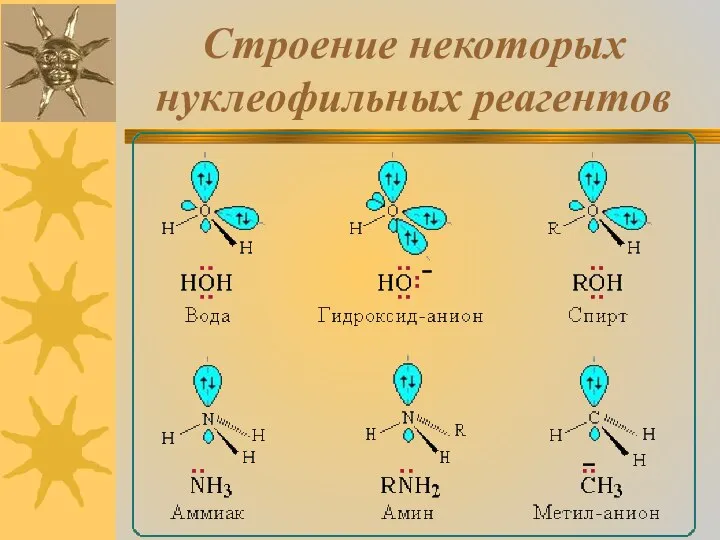
- 18. Строение некоторых нуклеофильных реагентов
- 19. Нуклеофильные реакции Благодаря подвижности π-электронов, нуклеофильными свойствами обладают также молекулы, содержащие π-связи: CH2=CH2, CH2=CH–CH=CH2, C6H6 и
- 21. Скачать презентацию















 ПОЛИЭТИЛЕН
ПОЛИЭТИЛЕН  Матчворк Підготувала учениця 11-А класу Шведюк Людмила
Матчворк Підготувала учениця 11-А класу Шведюк Людмила  Коллоидтық химия және беттік құбылыстар химиясының негізгі түсініктемелері
Коллоидтық химия және беттік құбылыстар химиясының негізгі түсініктемелері Степень окисления Автор презентации: учитель химии МОУ лицея «Технический» г. Обнинска Калужской области Яснова Юлия Анатоль
Степень окисления Автор презентации: учитель химии МОУ лицея «Технический» г. Обнинска Калужской области Яснова Юлия Анатоль Количественный анализ. Гравиметрия
Количественный анализ. Гравиметрия Жиры. Мыла. СМС. 10 класс
Жиры. Мыла. СМС. 10 класс Ненасыщенные углеводороды этиленового ряда
Ненасыщенные углеводороды этиленового ряда Физико-химическое явление электролиз
Физико-химическое явление электролиз Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Одорант природный
Одорант природный Презентация по Химии "Соли" - скачать смотреть
Презентация по Химии "Соли" - скачать смотреть  Прикладная химия. Теплоперенос в химических реакторах и теплообменники
Прикладная химия. Теплоперенос в химических реакторах и теплообменники Химическая связь. Строение веществ
Химическая связь. Строение веществ Исследование состава и свойств минеральной воды Авторы:
Исследование состава и свойств минеральной воды Авторы:  Викторина «Своя игра» в рамках декады по биологии, географии и химии
Викторина «Своя игра» в рамках декады по биологии, географии и химии  Растворы. Часть 2
Растворы. Часть 2 Сложные реакции
Сложные реакции Пиридин. Строение пиридина
Пиридин. Строение пиридина Фотосинтез. Суммарное уравнение, общий вид
Фотосинтез. Суммарное уравнение, общий вид Виды полимеризации
Виды полимеризации Коллоидная химия
Коллоидная химия Капилярлық конденсация. Дәріс 14
Капилярлық конденсация. Дәріс 14 Биохимия нервной ткани. Биологические мембраны
Биохимия нервной ткани. Биологические мембраны Валентность связи и локальный баланс валентности
Валентность связи и локальный баланс валентности Аммиак. Образование молекулы аммиака
Аммиак. Образование молекулы аммиака Метаболизм процесіндегі липидтер мен нуклеин қышқылдарының орны
Метаболизм процесіндегі липидтер мен нуклеин қышқылдарының орны Алкадиены. Физические свойства
Алкадиены. Физические свойства Презентация по Химии "Основные классы неорганических соединений" - скачать смотреть
Презентация по Химии "Основные классы неорганических соединений" - скачать смотреть