Содержание
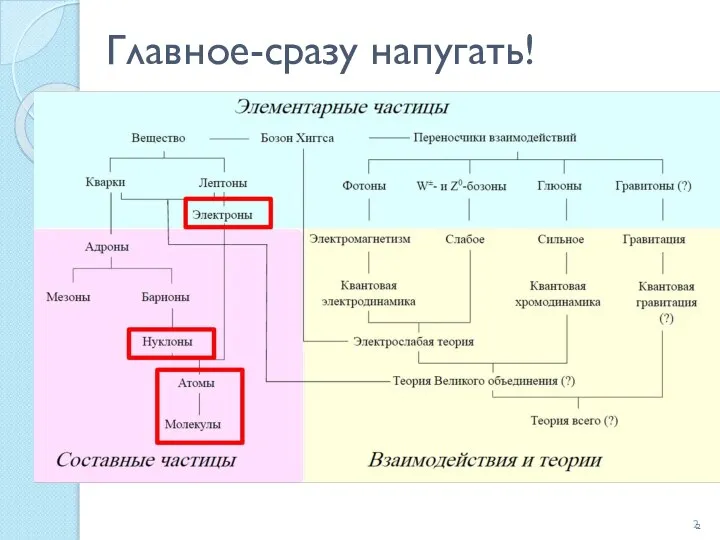
- 2. Главное-сразу напугать!
- 3. Строение атома He C
- 4. Типы атомных орбиталей
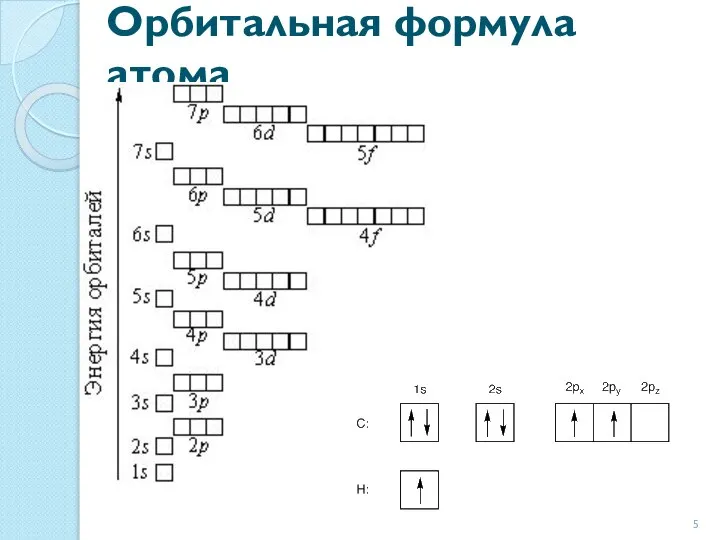
- 5. Орбитальная формула атома
- 6. Каждый уважающий себя атом стремится к электронному состоянию инертного газа! Нужно отдать электрон – ты донор,
- 7. Чем сильнее атому нужен электрон, тем он электроотрицательнее
- 8. Приобрёл стабильность – стал ионом!
- 9. Понял, что нужно атому – понял, что такое валентность
- 10. Химическая связь Ковалентная Одноэлектронная n е Одинарная/кратная е Полярная Неполярная Трёхцентровая/многоцентровая n n Сэндвичева Металлическая Ионная
- 11. Структура кристалла Кристаллы NaCl под бинокуляром
- 12. Вода, ее свойства и роль в организмах К+
- 13. Водородные связи Поверхностное натяжение воды, вязкость Поддержание структуры белка Поддержание структуры нуклеиновых кислот Поддержание структуры углеводных
- 14. Гидрофобные взаимодействия Правило первое: полярному хорошо с полярным Правило второе: неполярному хорошо с неполярным
- 15. Гидрофобность и гидрофильность
- 16. Ван-дер-ваальсовы взаимодействия Сцепление частиц малых астероидов кольца́ Сатурна Способность гекконов взбираться по гладким поверхностям, например, по
- 17. Элементный состав человеческого организма
- 18. Карбон (углерод) Органические соединения Карбонаты, оксиды Карбона (СО, СО₂)
- 19. Оксиген (кислород) Вода Простые вещества (О₂, окислитель) Органические вещества Соли неорганических кислот (фосфаты, карбонаты) Карбонат-анион Фосфат-анион
- 20. Гидроген Простые вещества (катионы водорода Н⁺) Вода Все органические соединения Неорганические кислоты Хлоридная кислота Аррениус Если
- 21. Нитроген Тройная связь в молекуле азота (N₂) Аминокислоты , белки Хлорофилл Продукты метаболизма (алкалоиды растений, мочевина
- 23. Скачать презентацию


















 Снежинки. Рождение снежинки
Снежинки. Рождение снежинки Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я.
Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я. Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.
Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А. Хлороводород. Соляная кислота. Хлориды
Хлороводород. Соляная кислота. Хлориды СПИРТЫ Урок химии в 9-10 классе
СПИРТЫ Урок химии в 9-10 классе Регуляция и патология липидного обмена
Регуляция и патология липидного обмена Влияние pH на микроорганизмы
Влияние pH на микроорганизмы Пирогова Т.В.учитель химии МОУ «Куженерская средняя общеобразовательная школа № 2»
Пирогова Т.В.учитель химии МОУ «Куженерская средняя общеобразовательная школа № 2»  Органические вещества
Органические вещества Мир химии.
Мир химии. Папайя-сarica papaya L. Сырьё - fructus caricae. Семейство кариковые caricaceae
Папайя-сarica papaya L. Сырьё - fructus caricae. Семейство кариковые caricaceae Презентация Изомерия
Презентация Изомерия  Ионные кристаллы
Ионные кристаллы  Алкены. Пропилен
Алкены. Пропилен Расчет энтропии образования и теплоемкости органических веществ методом Бенсона
Расчет энтропии образования и теплоемкости органических веществ методом Бенсона Ֆլավանոիդներ պարունակող դեղաբույսեր եվ հումք
Ֆլավանոիդներ պարունակող դեղաբույսեր եվ հումք Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ
Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ Биологически активные низкомолекулярные вещества
Биологически активные низкомолекулярные вещества Свойства идеального газа на примере воздуха
Свойства идеального газа на примере воздуха Методы решения ОВР с участием органических соединений
Методы решения ОВР с участием органических соединений Состояние электронов в атомах
Состояние электронов в атомах Химический состав и физические свойства продовольственных товаров
Химический состав и физические свойства продовольственных товаров Оксид серы(IV). Сернистая кислота. Учитель химии МБОУ «Елховская СОШ» Альметьевского муниципального района Республики Татарстан Г
Оксид серы(IV). Сернистая кислота. Учитель химии МБОУ «Елховская СОШ» Альметьевского муниципального района Республики Татарстан Г Проект познавательно-исследовательской деятельности. Удивительная соль
Проект познавательно-исследовательской деятельности. Удивительная соль Технологические методы производства деталей машин из ПКМ, содержащих дисперсные наполнители
Технологические методы производства деталей машин из ПКМ, содержащих дисперсные наполнители Идеальный и реальный газ
Идеальный и реальный газ Природні джерела вуглеводнів Підготувала: Савчук Ірина
Природні джерела вуглеводнів Підготувала: Савчук Ірина  6 КАЗ Изохинолин туынд
6 КАЗ Изохинолин туынд