Содержание
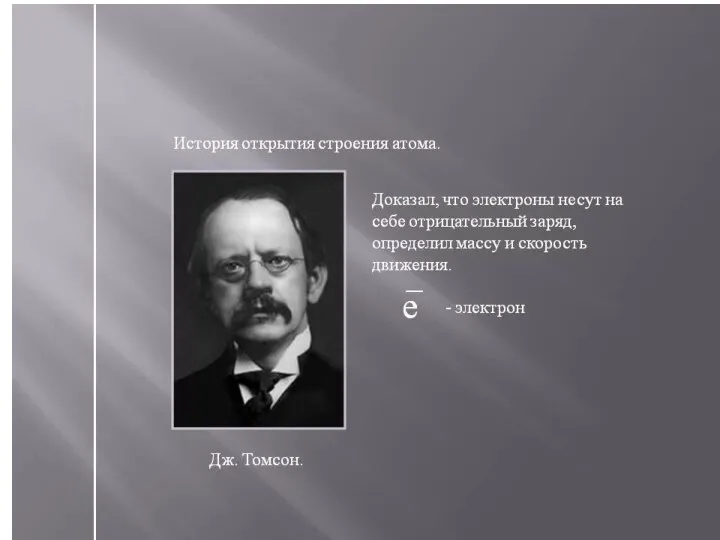
- 8. Планетарная модель атома 1. в центре атома - положительно заряженное ядро: заряд ядра q = Z·e,
- 9. электроны движутся с большой скоростью, образуя электронную оболочку атома.
- 10. Современной теории строения атома предшествовали открытия: 1. Открытие квантования энергии (Планк , 1900) 2. Применение «старой
- 11. 4. Построение квантовой и волновой механики (В . Гейзенберг , 1925;) Принцип Гейзенберга: невозможно одновременно и
- 12. 6. Принцип Паули для многоэлектронных систем (В . Паули , 1925) 7. Орбитальная модель многоэлектронных систем
- 13. Постулаты Бора. Первый постулат: Атомы имеют ряд стационарных состояний соответствующих определенным значениям энергий: Е1, Е2...En. Находясь
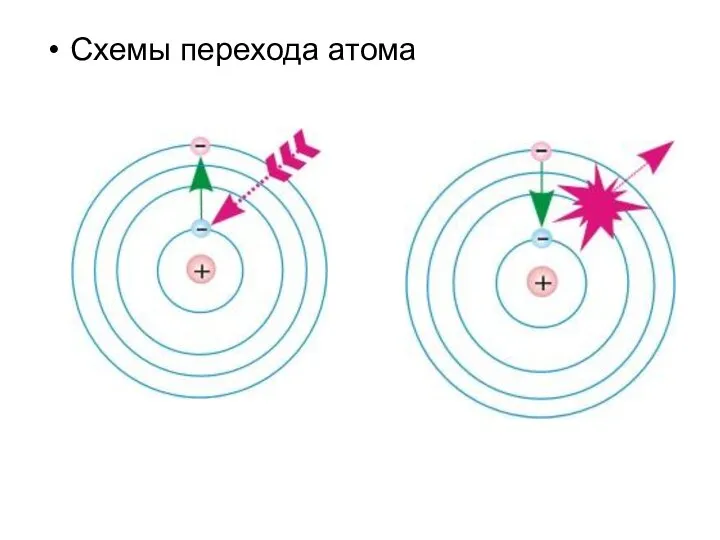
- 14. Третий постулат: Излучение или поглощение энергии атомом происходит при переходе его из одного стационарного состояния в
- 15. Схемы перехода атома
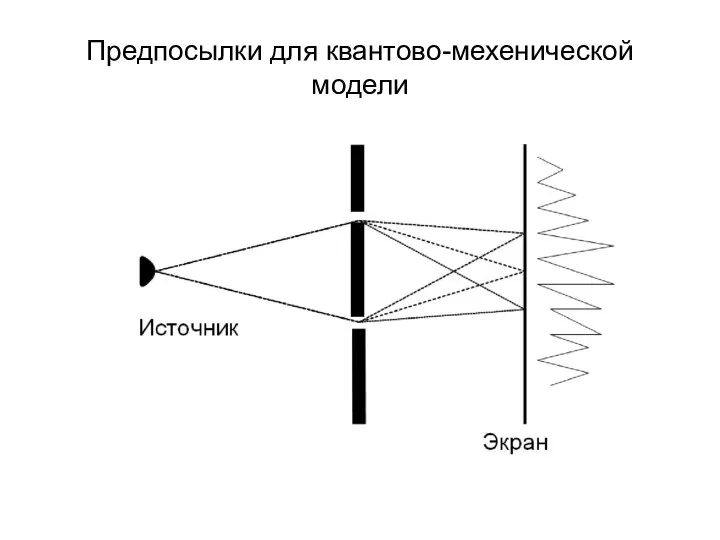
- 16. Квантово-механическая модель строения атома В основу модели положена квантовая теория атома, согласно которой электрон обладает как
- 17. Предпосылки для квантово-мехенической модели
- 18. Уравнение Шредингера – фундаментальное уравнение квантовой механики, которое описывает поведение электрона в атоме. H ψ =
- 19. Решения уравнения Шредингера Волновые функции Энергии Ψ1(x, y, z, t) E1 Ψ2(x, y, z, t) E2
- 20. Волновая функция ψ характеризует свойства квантовой системы. Особенности волновой функции: -является функцией координат ψ (x, y,
- 21. Квантовые числа. Квантовые числа и их значения являются следствием решений уравнений Шредингера и условий однозначности, непрерывности
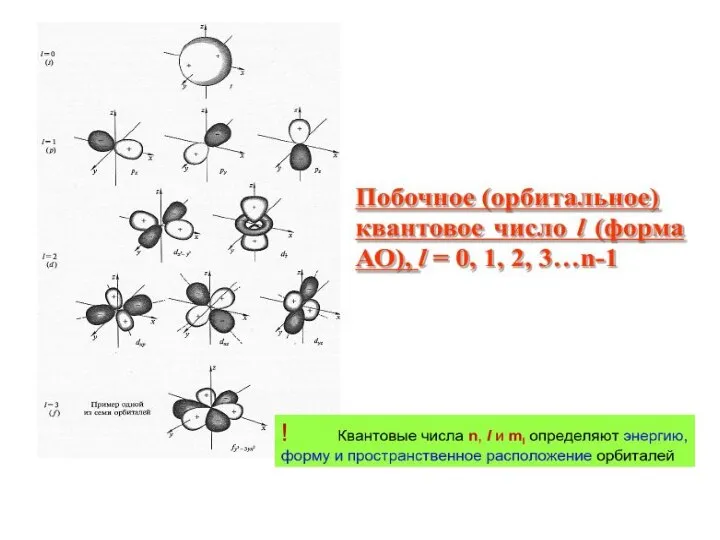
- 22. l - орбитальное квантовое число, которое при заданном n принимает значения 0,1,2,3,…(n-1), т. е. всего n
- 24. Для объяснения тонкой структуры спектральных линий американские физики Д. Уленбек (1900-1974) и С. Гаудсмит (1902-1979) предположили,
- 25. Итак, состояние электрона в атоме однозначно определяется набором четырех квантовых чисел: главного n (n =1, 2,
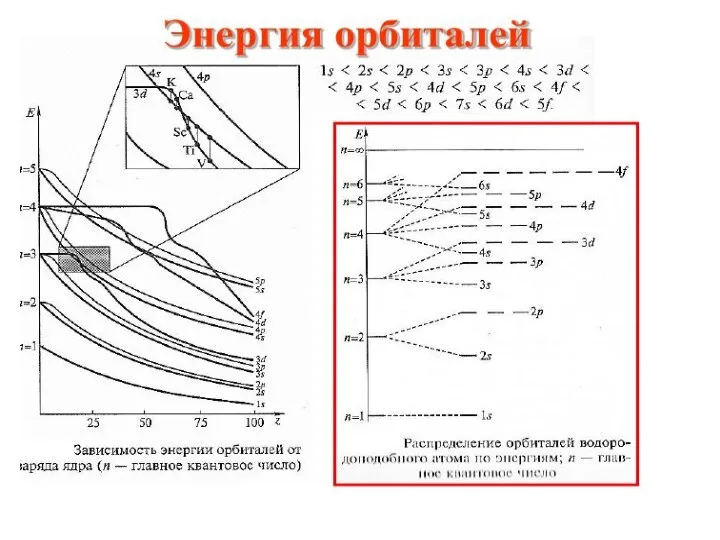
- 26. Распределение электронов в атоме по состояниям. Принципы и правила. 1.Принцип наименьшей энергии: из всех возможных состояний
- 27. Атом водорода (протий). 1H1 Ядро атома водорода состоит из одного протона. А атом водорода из одного
- 29. Литий. Z=3. 1. n=1,l=0, ml =0, ms=+1/2 2. n=1,l=0, ml =0, ms=-1/2 3. n=2 l=0, ml
- 31. Электронные формы атомов
- 32. Почему у азота электроны на 3р-подуровне располагаются на разных орбиталях? Правило Хунда: в пределах подуровня электроны
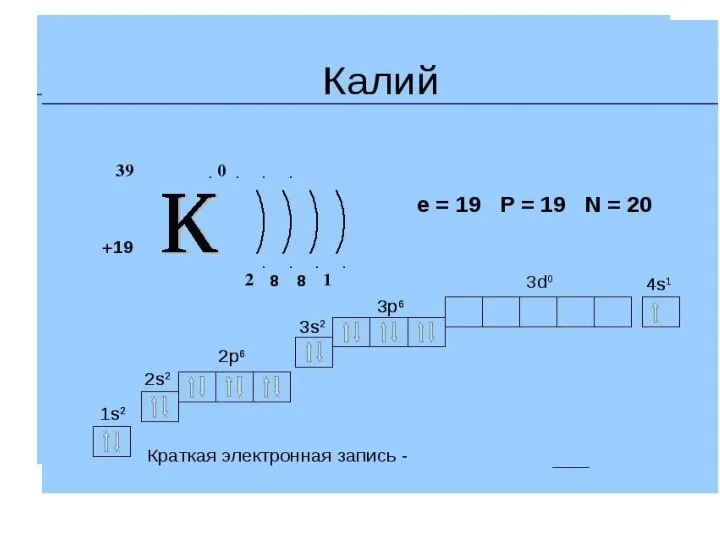
- 35. Почему у калия последний внешний электрон располагается на 4s –орбитали, а не на 3d? По первому
- 37. 24Cr напрашивается:1s22s22p63s23p63d44s2, но самом деле : 1s22s22p63s23p63d54s1. Оказалось, что состояние с наполовину заполненным d-подуровнем является более
- 39. Скачать презентацию





























 Простой борный суперфосфат
Простой борный суперфосфат Алканы. Физические и химические свойства
Алканы. Физические и химические свойства Горение жидкостей
Горение жидкостей Интернет-семинар (вебинар). Методика подготовки к олимпиадам и интеллектуальным турнирам по химии. Часть 1
Интернет-семинар (вебинар). Методика подготовки к олимпиадам и интеллектуальным турнирам по химии. Часть 1 Масс-Спектроскопия
Масс-Спектроскопия Аминокислоты. Изомерия. Белки
Аминокислоты. Изомерия. Белки Растворы. Определения и понятия
Растворы. Определения и понятия Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Застосування електролізу
Застосування електролізу Химический состав зеленого чая и его влияние на организм человека
Химический состав зеленого чая и его влияние на организм человека Дисперсные системы
Дисперсные системы Массообменные процессы
Массообменные процессы Геохимия природных процессов. Мономинеральный баланс рубидия в гранодиорите. (Лекция 4)
Геохимия природных процессов. Мономинеральный баланс рубидия в гранодиорите. (Лекция 4) Презентация по Химии "Углеводы" - скачать смотреть
Презентация по Химии "Углеводы" - скачать смотреть  Органические вяжущие. Битумы
Органические вяжущие. Битумы Электрохимия. Окислительно-восстановительные реакции
Электрохимия. Окислительно-восстановительные реакции Експертиза коштовного каміння
Експертиза коштовного каміння Влияние кислотности среды на свойство белка
Влияние кислотности среды на свойство белка Тяжелые р – элементы -полуметаллы
Тяжелые р – элементы -полуметаллы Свойства неметаллов и их соединений. Практическая работа №4
Свойства неметаллов и их соединений. Практическая работа №4 Закон сохранения массы веществ. Уравнения химических реакций
Закон сохранения массы веществ. Уравнения химических реакций Вводные понятия к установке кристаллов
Вводные понятия к установке кристаллов Природній газ
Природній газ  Обед под микроскопом. Минеральные вещества
Обед под микроскопом. Минеральные вещества Энергосиловое оборудование промышленных предприятий. Топливо и его виды
Энергосиловое оборудование промышленных предприятий. Топливо и его виды Алкины
Алкины Электролитическая диссоциация
Электролитическая диссоциация Класс «оксиды»
Класс «оксиды»