Строение и свойства атомов в свете квантовомеханической теории. Периодический закон – основа основ химии
Содержание
- 2. План 1. Принцип неопределенности В. Гейзенберга. 2. Уравнение Э. Шредингера. Атомная орбиталь. 3. Квантовые числа. 4.
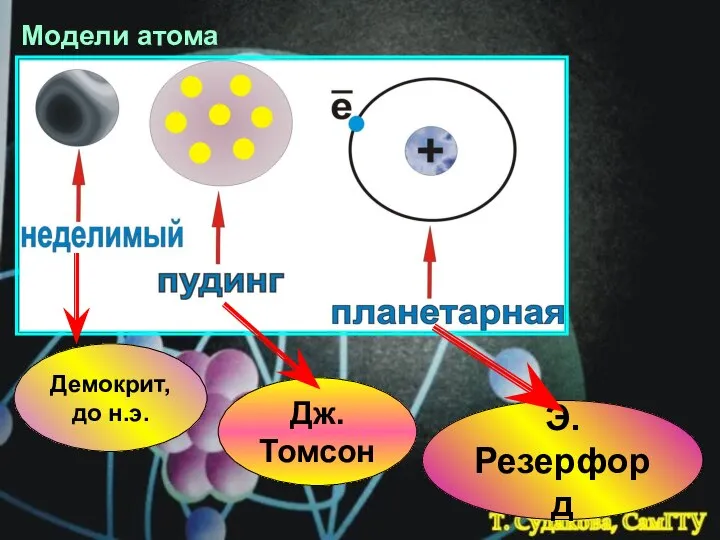
- 3. Модели атома Демокрит, до н.э. Дж. Томсон Э. Резерфорд
- 4. у микромира свои законы! ядро +n В. Гейзенберг Э. Шредингер Волновой характер движения электрона (корпускулярно- волновой
- 5. Принцип неопределенности Невозможно в любой данный момент времени одновременно получить точные сведения и о скорости движения
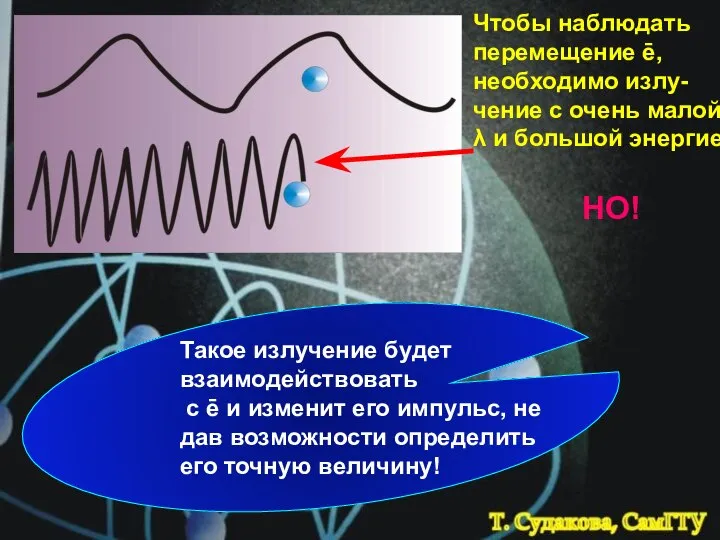
- 6. Чтобы наблюдать перемещение ē, необходимо излу-чение с очень малой λ и большой энергией НО! Такое излучение
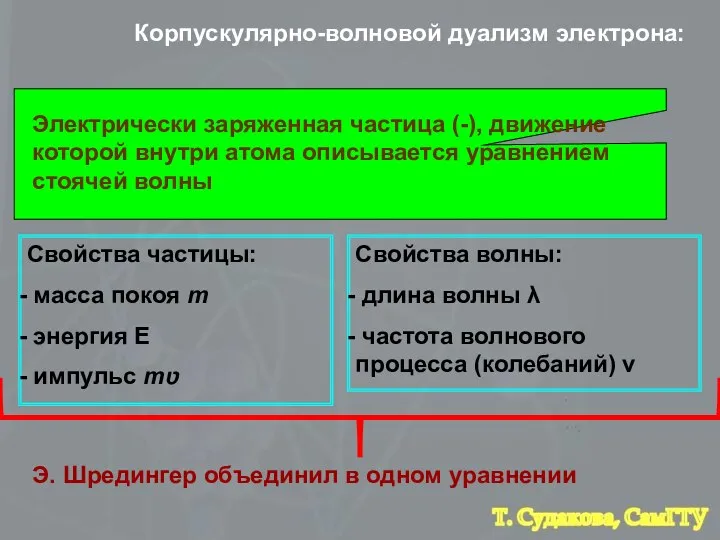
- 7. Корпускулярно-волновой дуализм электрона: Электрически заряженная частица (-), движение которой внутри атома описывается уравнением стоячей волны Свойства
- 8. Уравнение Шрёдингера: (∂2ψ/∂х2 + ∂2ψ/∂y2 + ∂2ψ/∂z2) + 8mπ2/h2 (E – U)ψ = 0 Δ2 ψ
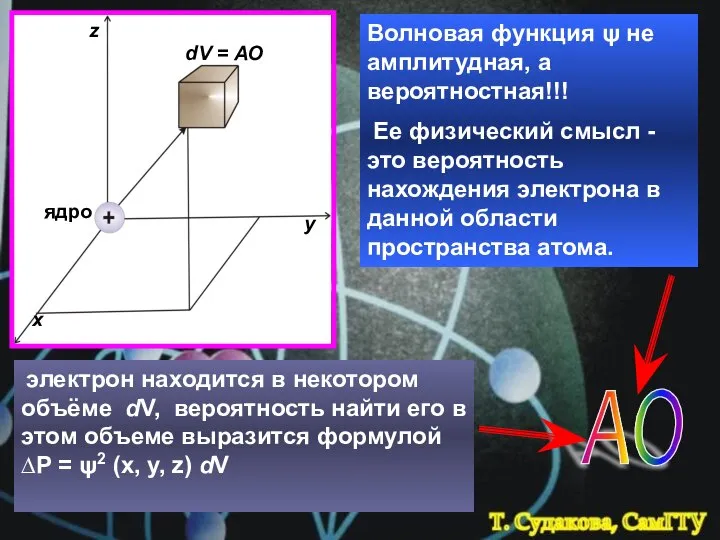
- 9. Волновая функция ψ не амплитудная, а вероятностная!!! Ее физический смысл - это вероятность нахождения электрона в
- 10. Атомная орбиталь (АО) - волновая функция ψ(x, y, z), определяющая область наиболее вероятного нахождения электрона в
- 11. Решение волнового уравнения Волновая функция и АО, существующие при определенных значениях некоторых целых чисел Квантовые числа
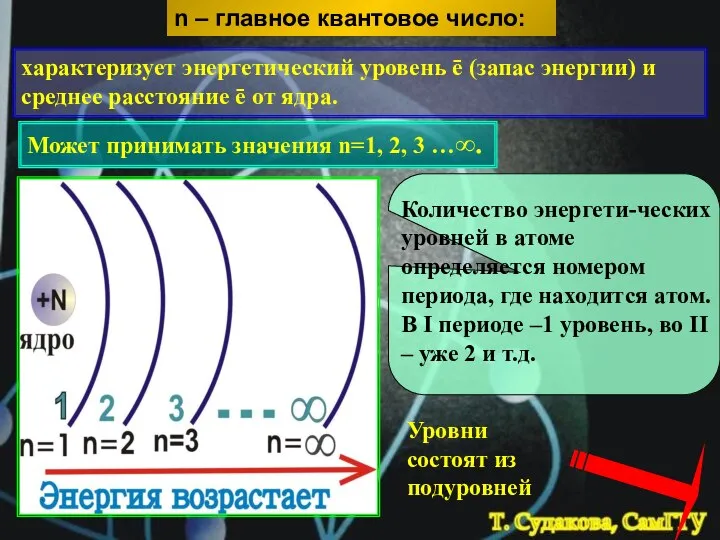
- 12. n – главное квантовое число: характеризует энергетический уровень ē (запас энергии) и среднее расстояние ē от
- 13. l – орбитальное квантовое число: определяет запас энергии электрона на подуровне и форму АО. l может
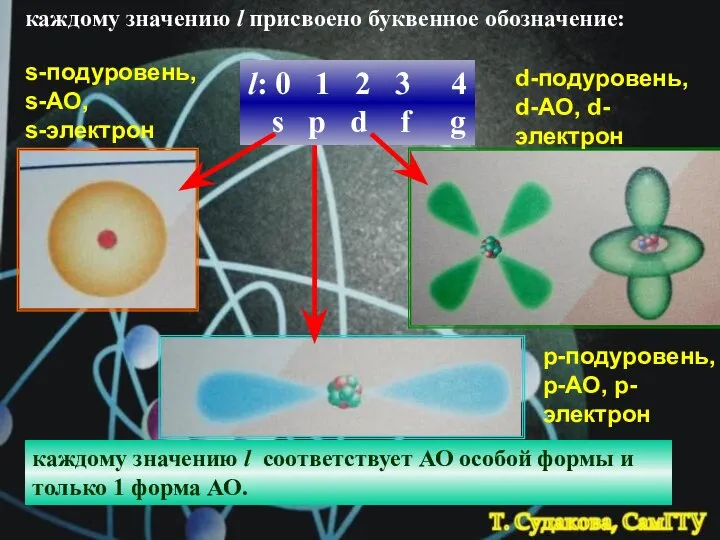
- 14. каждому значению l соответствует АО особой формы и только 1 форма АО. каждому значению l присвоено
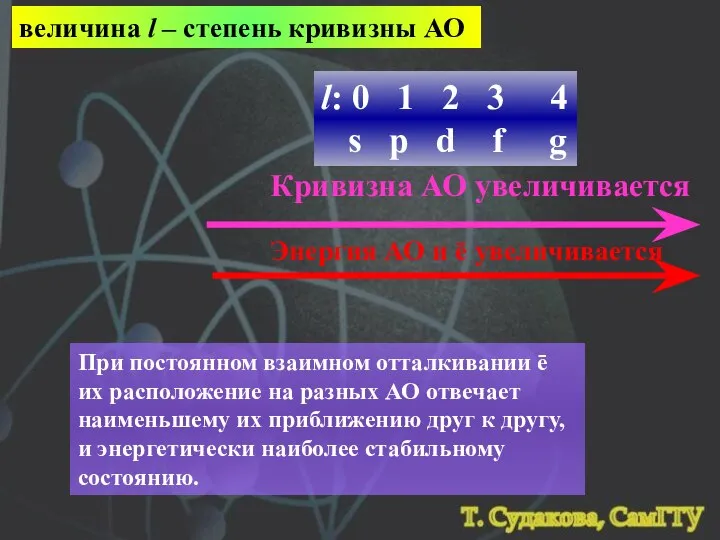
- 15. l: 0 1 2 3 4 s p d f g величина l – степень кривизны
- 16. Магнитное квантовое число m: характеризует ориентацию АО в пространстве. Число ориентаций АО – это количество значений
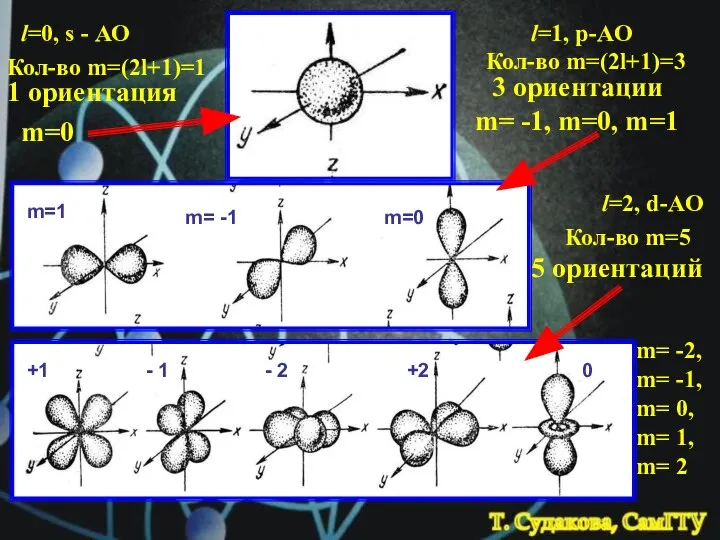
- 17. l=0, s - АО Кол-во m=(2l+1)=1 m=0 1 ориентация l=1, p-AO Кол-во m=(2l+1)=3 3 ориентации m=
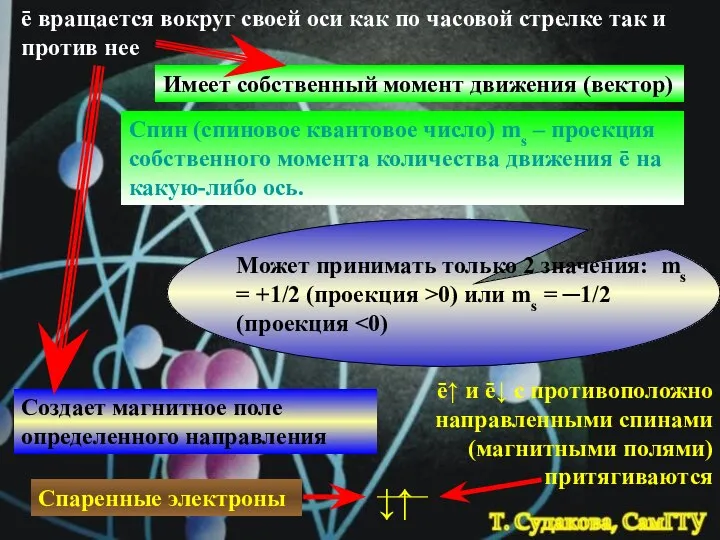
- 18. ē вращается вокруг своей оси как по часовой стрелке так и против нее Имеет собственный момент
- 19. ПРАВИЛА РАСПРЕДЕЛЕНИЯ ЭЛЕКТРОНОВ В АТОМАХ 1. Принцип запрета Вольфганга Паули - в атоме не может быть
- 20. 2. Принцип наименьшей энергии: электроны заполняют АО в атоме в порядке увеличения их энергии. Энергия 2s–AO
- 21. 3. Правило Фридриха Хунда (Гунда): электроны в пределах данного подуровня располагаются сначала по одному в свободных
- 22. 4. Правила Клечковского: А) заполнение электронных уровней с увеличением атомного номера элемента происходит последовательно в порядке
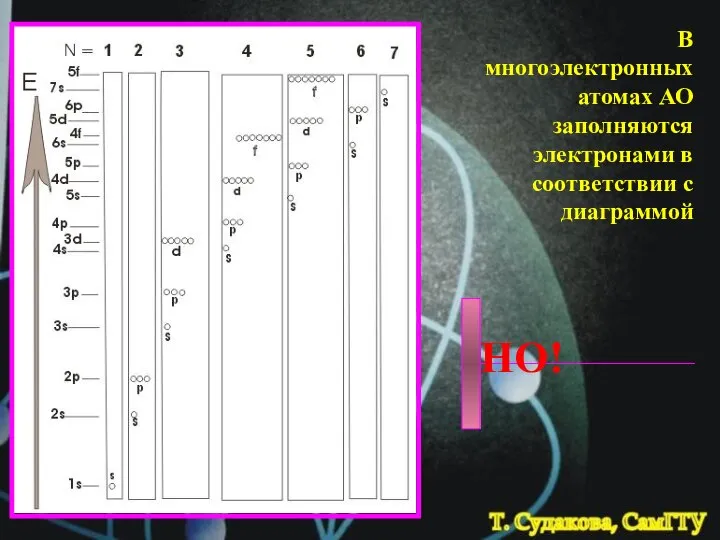
- 23. В многоэлектронных атомах АО заполняются электронами в соответствии с диаграммой НО!
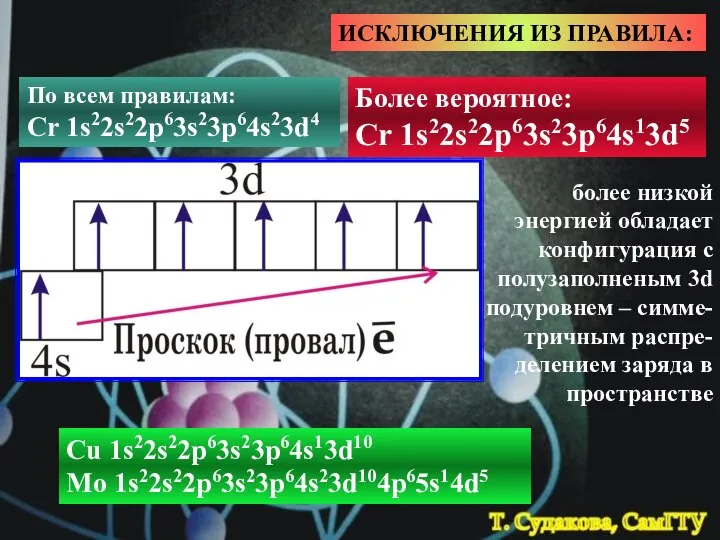
- 24. более низкой энергией обладает конфигурация с полузаполненым 3d подуровнем – симме-тричным распре-делением заряда в пространстве ИСКЛЮЧЕНИЯ
- 25. свойства атомов 1) Потенциал (энергия) ионизации: А → А+n + nē катион Энергия ионизации – энергия,
- 26. Для многоэлектронных атомов: Отрыв 1-го ē – первый потенциал ионизации I1 Отрыв 2-го ē – второй
- 27. I изменяется периодически: в периодах увеличива-ется, в группах - уменьшается
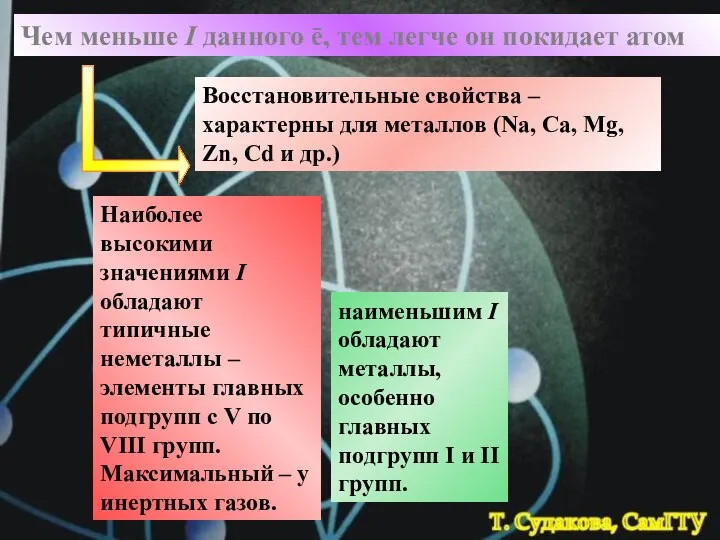
- 28. наименьшим I обладают металлы, особенно главных подгрупп I и II групп. Чем меньше I данного ē,
- 29. 2) ЭНЕРГИЯ СРОДСТВА АТОМА К ЭЛЕКТРОНУ А + nē → An─ анион Энергия сродства атома к
- 30. Энергия сродства к ē также находится в периодической зависимости от заряда ядра: в периоде с ↑
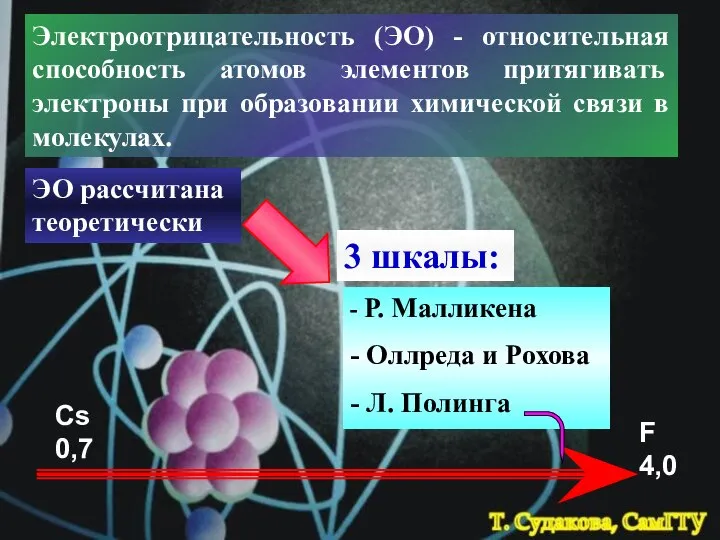
- 31. Электроотрицательность (ЭО) - относительная способность атомов элементов притягивать электроны при образовании химической связи в молекулах. ЭО
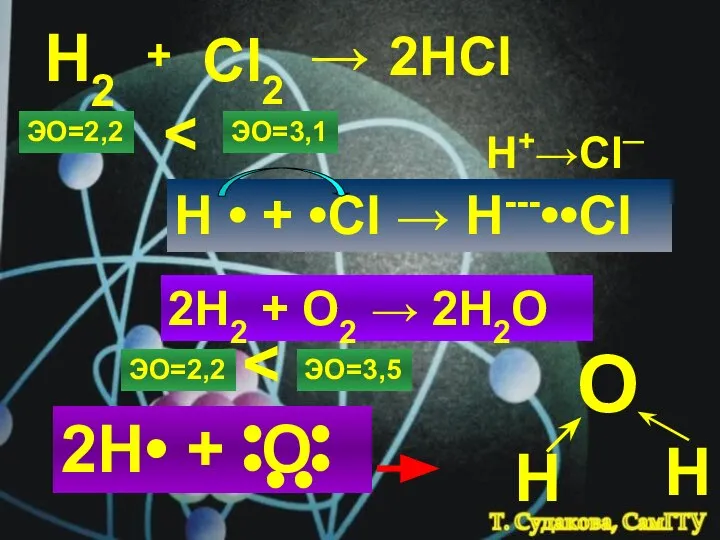
- 32. Н2 + Cl2 → 2HCl ЭО=2,2 ЭО=3,1 H • + •Cl → H---••Cl H+→Cl─ 2H2 +
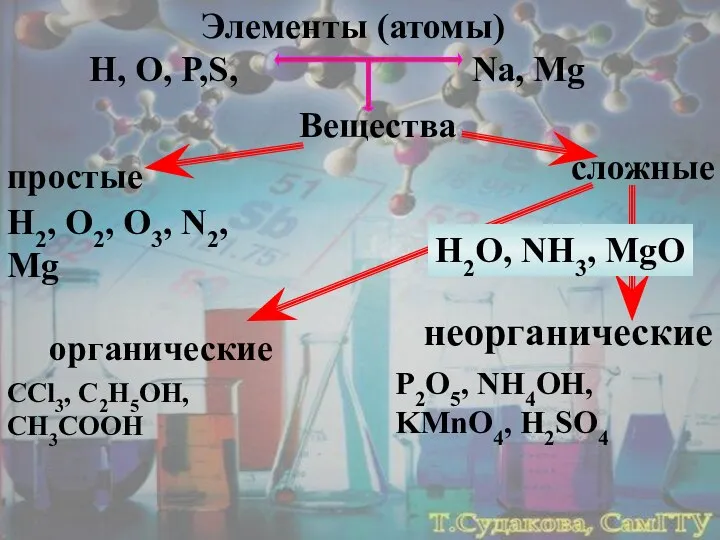
- 33. Элементы (атомы) H, O, P,S, Na, Mg Вещества простые сложные H2, O2, O3, N2, Mg органические
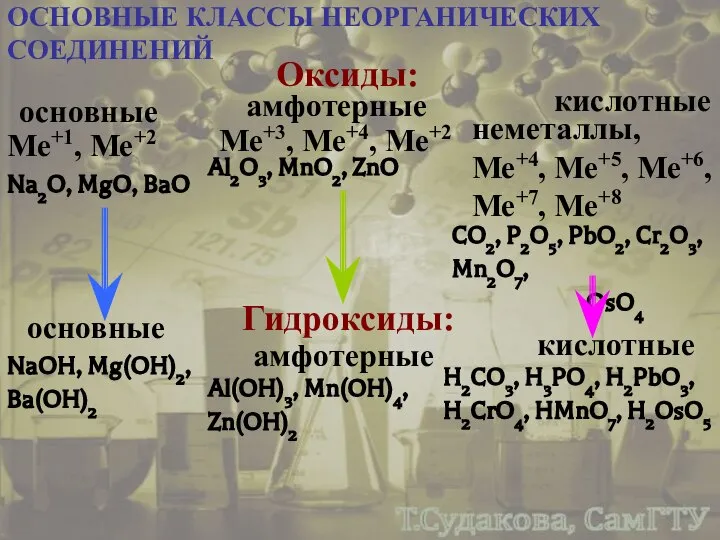
- 34. ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Оксиды: основные амфотерные кислотные Ме+1, Ме+2 Ме+3, Ме+4, Ме+2 неметаллы, Ме+4, Ме+5,
- 35. Химические свойства оксидов и гидроксидов 1) Кислотные оксиды и гидроксиды реагируют с основными и амфотерными оксидами
- 36. 2) Основные оксиды и гидроксиды реагируют с кислотными и амфотерными оксидами и гидроксидами (см. предыдущий слайд):
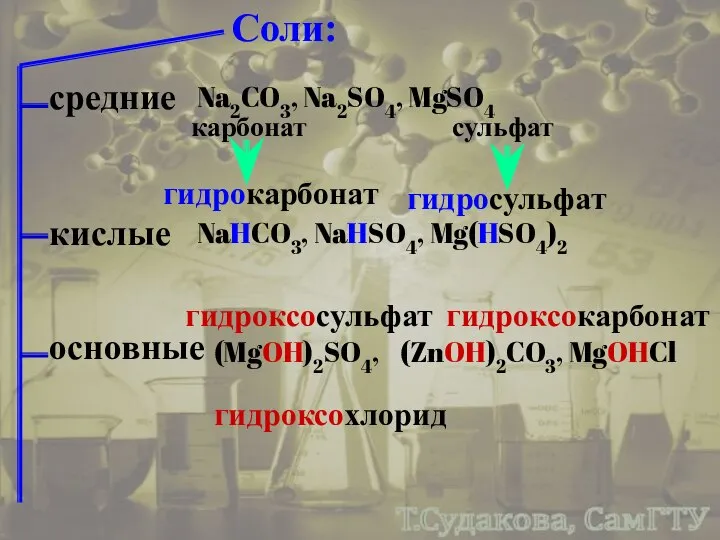
- 37. Соли: средние Na2CO3, Na2SO4, MgSO4 кислые NaHCO3, NaHSO4, Mg(HSO4)2 карбонат гидрокарбонат сульфат гидросульфат основные (MgOH)2SO4, (ZnOH)2CO3,
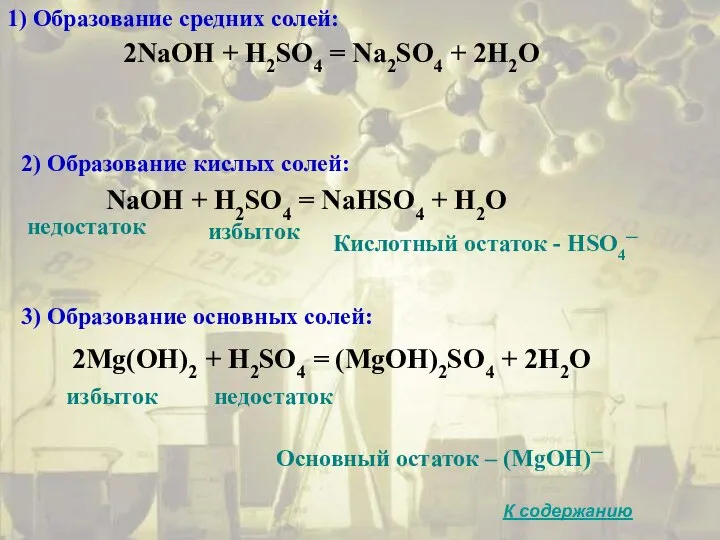
- 38. 1) Образование средних солей: 2NaOH + H2SO4 = Na2SO4 + 2H2O 2) Образование кислых солей: NaOH
- 40. Скачать презентацию



















 Органические вещества. Предмет органической химии
Органические вещества. Предмет органической химии Реакция обменного разложения веществ водой - гидролиз
Реакция обменного разложения веществ водой - гидролиз Кислородсодержащие. Углеводы. Подготовка к ЕГЭ
Кислородсодержащие. Углеводы. Подготовка к ЕГЭ Буферные растворы
Буферные растворы Протолитическая теория кислот и оснований
Протолитическая теория кислот и оснований Консерванты для косметики и парфюмерных изделий
Консерванты для косметики и парфюмерных изделий Получение калийной селитры
Получение калийной селитры Кристаллическая структура
Кристаллическая структура Амиды кислот. Азо- и диазосоединения
Амиды кислот. Азо- и диазосоединения Сернистый ангидрид SO2. Диоксид серы
Сернистый ангидрид SO2. Диоксид серы ЙОД
ЙОД  Силикатная промышленность
Силикатная промышленность Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Презентация по Химии "Первичная переработка нефти" - скачать смотреть бесплатно
Презентация по Химии "Первичная переработка нефти" - скачать смотреть бесплатно Структура и физическое состояние полимеров
Структура и физическое состояние полимеров Фізичні та хімічні явища. (7 клас)
Фізичні та хімічні явища. (7 клас) Тема: Ионные уравнения реакции Вспомним реакцию нейтрализации.
Тема: Ионные уравнения реакции Вспомним реакцию нейтрализации.  Нина Кара 24 группа коррозия металлов
Нина Кара 24 группа коррозия металлов Алифатические углеводороды. Алканы, их свойства
Алифатические углеводороды. Алканы, их свойства Коллигативные свойства растворов. Осмос. Осмотическое давление. (Лекция 4)
Коллигативные свойства растворов. Осмос. Осмотическое давление. (Лекция 4) Выполнила студентка ХБ-4 Ширяева София
Выполнила студентка ХБ-4 Ширяева София Химические реакции. Скорость реакции
Химические реакции. Скорость реакции Механика полимеров
Механика полимеров Соли «Na2SO4»
Соли «Na2SO4» Приборы для измерения температуры
Приборы для измерения температуры Етилен і ацетилен – ненасичені вуглеводні
Етилен і ацетилен – ненасичені вуглеводні Химические реакции 11 кл Учитель химии МОУ СОШ с.Ильинское МО «Томаринский городской округ» Сахалинской области Чуб И.В.
Химические реакции 11 кл Учитель химии МОУ СОШ с.Ильинское МО «Томаринский городской округ» Сахалинской области Чуб И.В. Белки. Структуры белков
Белки. Структуры белков