Содержание
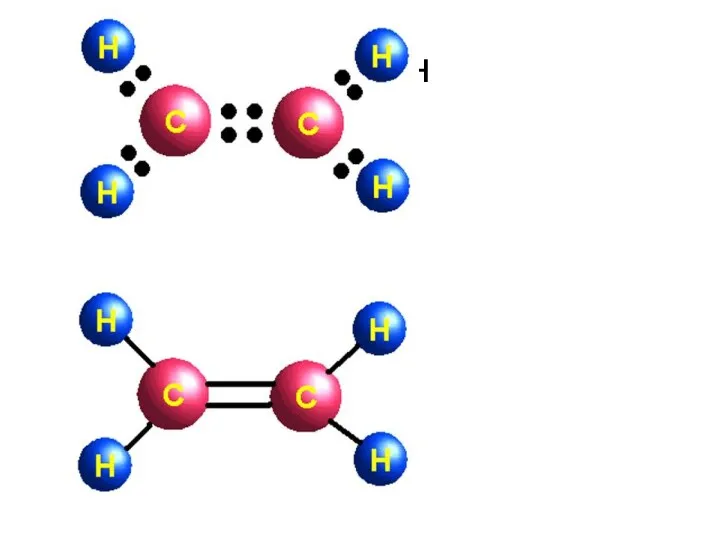
- 2. Двойная связь связь C=C, образована двумя обобществленными электронными парами C::C. Но состояние каждой из них не
- 3. Три гибридных облака каждого из углеродных атомов этилена участвуют в образовании трех σ-связей (второе валентное состояние
- 4. этилен
- 6. одна из электронных пар двойной связи между атомами углерода осуществляют обычную σ-связь вторая электронная пара образуется
- 7. Связь, осуществляемую такой парой электронов, называют π-связью, а образующие ее электроны - π- электронами. π-связь возникает
- 8. Тройная связь C≡C образована тремя парами обобществленных электронов Состояние этих пар не одинаково, так же как
- 9. При образовании тройной связи в каждом углеродном атоме гибридизируется одно s- и одно p- состояния электронов
- 10. Два гибридных облака каждого атома С в ацетилене участвуют в образовании двух σ-связей (третье валентное состояние
- 11. Изомерия
- 12. Еще в 1814 г. французский ученый Гей-Люссак установил, что некоторые вещества при одном и том же
- 13. Это явление, заключающееся в существовании нескольких химических соединений с одинаковым качественным и количественным составом, но отличных
- 14. Первый изомер углеводорода бутана C4H10 имеет прямую (нормальную) цепь. Второй изомер – изобутан – разветвленную цепь
- 15. С увеличением числа атомов углерода в молекуле резко возрастает число изомеров. Известны все 9 структурных изомерных
- 16. Изомерия характерна не только для линейных, но и для циклических молекул
- 17. Структурная изомерия может иметь место и при одинаковом углеродном скелете, если функциональные группы занимают различное положение
- 19. Органические соединения образуют гомологические ряды. Каждый последующий член гомологического ряда отличается от предыдущего на метиленовую группу
- 20. Ациклические насыщенные (предельные) углеводороды (парафины, алканы)
- 21. Наиболее простыми органическими соединениями являются вещества, молекулы которых построены только из атомов углерода и водорода и
- 22. Значение углеводородов заключается еще и в том, что все остальные, более сложные по составу органические вещества
- 23. Углеводороды, в молекулах которых углеродные атомы образуют открытые, незамкнутые цепи, называют ациклическими углеводородами, или углеводородами жирного
- 24. К классу насыщенных углеводородов относят такие углеводороды, в молекулах которых углеродные атомы соединены друг с другом
- 25. Физические свойства насыщеных углеводородов Насыщенные углеводороды – бесцветные вещества, практически не растворимые в воде, с плотностью
- 26. Метан, этан, пропан и бутан при обычных условиях представляют собой газы; они почти не имеют запаха.
- 27. Температуры кипения и плавления углеводородов зависят и от их строения. Нормальные углеводороды кипят выше, чем углеводороды
- 28. Химические свойства насыщенных углеводородов
- 29. Насыщенные (предельные) углеводороды – это вещества, трудно вступающие реакции при обычных температурах. Для всех углеводородов гомологического
- 30. Взаимодействие с галогенами В обычных условиях хлор и бром реагируют с насыщенными углеводородами, но лишь очень
- 32. Реакция с азотной кислотой (реакция нитрования) Концентрированная азотная кислота при нагревании окисляет насыщенные углеводороды, а на
- 33. Образующиеся вещества называют нитросоединениями. В их молекулах азот нитрогрупы непосредственно связан с углеродом. Впоследствии было разработано
- 34. Если исходный углеводород содержит различные углеродные атомы – первичные, вторичные или третичные, то образуется смесь изомерных
- 35. Нитросоединения жирного ряда – бесцветные жидкости, не растворимые в воде, со слабым эфирным запахом.
- 36. Отношение к действию окислителей и высоких температур При низких температурах предельные углеводороды устойчивы даже к действию
- 37. Действие кислорода воздуха. При высоких температурах под действием кислорода воздуха предельные воспламеняются и сгорают с образованием
- 38. Крекинг углеводородов . При нагревании углеводородов до высоких температур (450—550 С) без доступа воздуха они распадаются
- 39. Реакция дегидрирования. Эта реакция заключается в отщеплении от молекул предельных углеводородов атомов водорода и приводит к
- 41. Скачать презентацию





































 Сутегі. Оттегі. Сутекті алу және оның қасиеттерін зерттеу
Сутегі. Оттегі. Сутекті алу және оның қасиеттерін зерттеу «Жизнь есть способ существования белковых тел…» (Ф.Энгельс) Выполнила преподаватель химии: Шилькиева И.А. г. Астрахань
«Жизнь есть способ существования белковых тел…» (Ф.Энгельс) Выполнила преподаватель химии: Шилькиева И.А. г. Астрахань  Массообменные процессы
Массообменные процессы Взаимосвязь обмена веществ
Взаимосвязь обмена веществ Производные изоникотиновой кислоты: изониазид
Производные изоникотиновой кислоты: изониазид Повторение 8 класса. Основные понятия химии
Повторение 8 класса. Основные понятия химии Підготувала учениця 11-А класу Білецька Олеся
Підготувала учениця 11-А класу Білецька Олеся  Silicates
Silicates Минералы и их свойства
Минералы и их свойства Кислород как элемент
Кислород как элемент Презентация по Химии "Класифікація хімічних речовин" - скачать смотреть бесплатно
Презентация по Химии "Класифікація хімічних речовин" - скачать смотреть бесплатно Характерные дефекты в монокристаллах кремния и их влияние на свойства. Методы диагностики
Характерные дефекты в монокристаллах кремния и их влияние на свойства. Методы диагностики Химическая связь
Химическая связь Характеристика органических соединений
Характеристика органических соединений Решение 33 задания
Решение 33 задания Колообіг карбону у природі. Виконали: учениці 10-А класу Кирлейза Софія Мустіпан Вікторія
Колообіг карбону у природі. Виконали: учениці 10-А класу Кирлейза Софія Мустіпан Вікторія  Кислотность и основностьорганических соединений
Кислотность и основностьорганических соединений Непредельные углеводороды АЛКЕНЫ Алферова Мария Владимировна учитель химии ГБОУ лицей №486 Выборгского района г. Санкт-Петербу
Непредельные углеводороды АЛКЕНЫ Алферова Мария Владимировна учитель химии ГБОУ лицей №486 Выборгского района г. Санкт-Петербу Классификация минералов по химическому принципу
Классификация минералов по химическому принципу Минералы. Классы минералов
Минералы. Классы минералов Фосфонсірке қышқылының антипирендік қасиеттерін зерттеу
Фосфонсірке қышқылының антипирендік қасиеттерін зерттеу Алюминий и его сплавы
Алюминий и его сплавы Нәруыз. Қасиеті және қызметі
Нәруыз. Қасиеті және қызметі Алюміній
Алюміній  Волокно капрон
Волокно капрон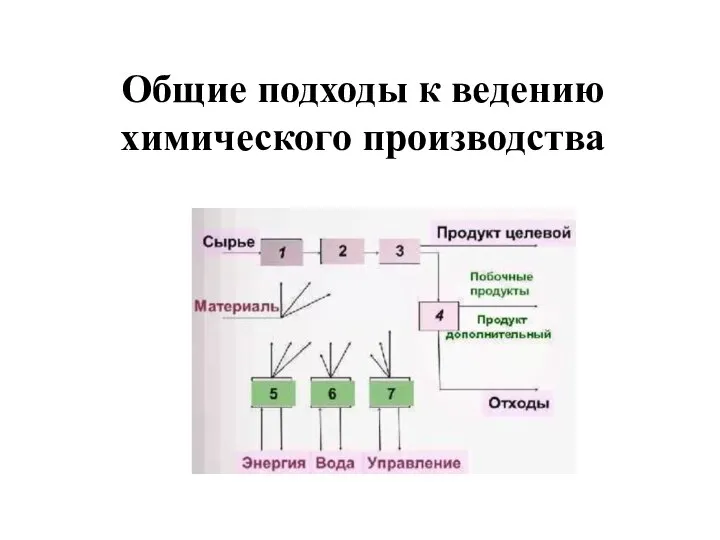 Общие подходы к ведению химического производства
Общие подходы к ведению химического производства Век медный, бронзовый, железный Тужилкина Полина 9 Б класс МОУ «СОШ №92»
Век медный, бронзовый, железный Тужилкина Полина 9 Б класс МОУ «СОШ №92» Парниковий ефект
Парниковий ефект