Содержание
- 2. Супрамолекулярная химия Супрамолекулярная химия – химия межмолекулярных связей.
- 3. Природа супрамолекулярных взаимодействий Супрамолекулярная химия имеет дело с нековалентными связывающими взаимодействиями. Ион-ионные взаимодействия Ион-дипольные взаимодействия Диполь-дипольные
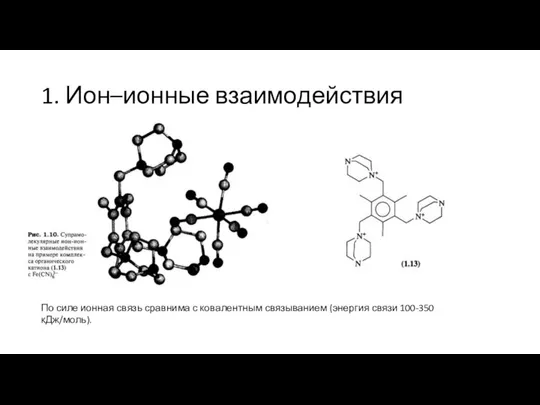
- 4. 1. Ион–ионные взаимодействия По силе ионная связь сравнима с ковалентным связыванием (энергия связи 100-350 кДж/моль).
- 5. 2. Ион-дипольные взаимодействия (50-200 кД/моль) Пример ион-дипольного взаимодействия - связывание иона Na+ с такой полярной молекулой,
- 6. 3. Диполь-дипольные взаимодействия (5-50 кДж/моль) Взаимная ориентация одного диполя относительно другого может приводить к значительным притягивающим
- 7. 4. Водородные связи (4-120 кДж/моль) Водородную связь можно рассматривать как особый вид диполь-дипольного взаимодействия, в котором
- 8. (5-80 кДж/моль) ???
- 9. 6. 7. 8. не важно
- 28. Скачать презентацию
























 Химические методы определения U, Pu, Th
Химические методы определения U, Pu, Th Метасоматический процесс
Метасоматический процесс Теоретические и экспериментальные методы исследования в химии
Теоретические и экспериментальные методы исследования в химии Карбон кыш
Карбон кыш Титрування. Хімічний посуд в титриметричному аналізі
Титрування. Хімічний посуд в титриметричному аналізі Полезные продукты на основе 4-хлоризотиазолов
Полезные продукты на основе 4-хлоризотиазолов Органическая химия. Глицерин
Органическая химия. Глицерин Синтетичні лікарські препарати
Синтетичні лікарські препарати  Семь чудес света и роль металлов в их создании
Семь чудес света и роль металлов в их создании Принципы защиты от коррозии
Принципы защиты от коррозии Полярные электронные эффекты в органических соединениях
Полярные электронные эффекты в органических соединениях Хроматографія. Мікрогетерогенні дисперсні системи
Хроматографія. Мікрогетерогенні дисперсні системи Радиохимия аспиранты
Радиохимия аспиранты Неорганические вещества. Минеральные соли и кислоты
Неорганические вещества. Минеральные соли и кислоты Требование к оформлению отчета лабораторной работы
Требование к оформлению отчета лабораторной работы Структура основных тканей зуба. (Лекция 2)
Структура основных тканей зуба. (Лекция 2) Презентация по Химии "карбон кышкылдары" - скачать смотреть
Презентация по Химии "карбон кышкылдары" - скачать смотреть  Влияние растворителя на процесс комплексообразования
Влияние растворителя на процесс комплексообразования Изохинолин туындыларының дәрілік заттарын талдау
Изохинолин туындыларының дәрілік заттарын талдау Виды твердых тел
Виды твердых тел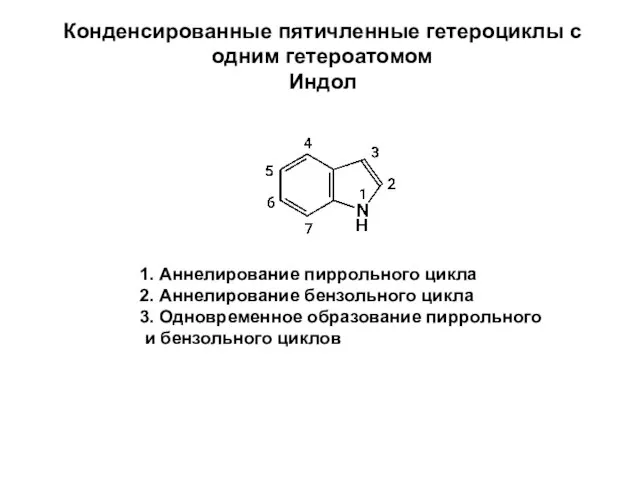 Конденсированные пятичленные гетероциклы с одним гетероатомом. Индол
Конденсированные пятичленные гетероциклы с одним гетероатомом. Индол В мире минералов и горных пород
В мире минералов и горных пород Нафтопереробна промисловість України
Нафтопереробна промисловість України  Виды присадок к моторным топливам
Виды присадок к моторным топливам Презентация по Химии "Вода для жизни!" - скачать смотреть бесплатно
Презентация по Химии "Вода для жизни!" - скачать смотреть бесплатно Строение электронной оболочки атома
Строение электронной оболочки атома Теория растворов (лекция 1)
Теория растворов (лекция 1) Презентация по Химии "Химический КВН" - скачать смотреть
Презентация по Химии "Химический КВН" - скачать смотреть