Содержание
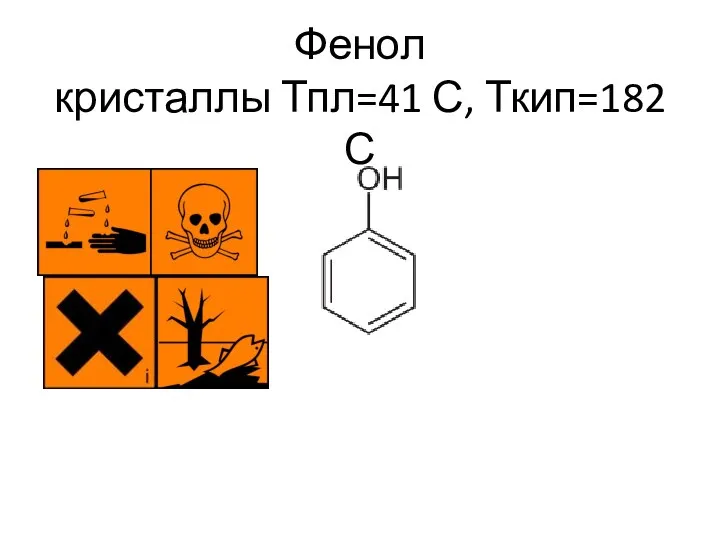
- 2. Фенол кристаллы Тпл=41 С, Ткип=182 С
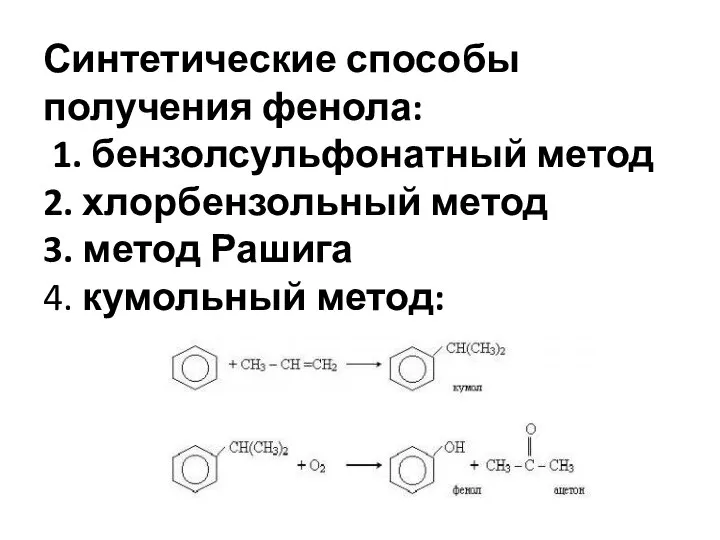
- 3. Синтетические способы получения фенола: 1. бензолсульфонатный метод 2. хлорбензольный метод 3. метод Рашига 4. кумольный метод:
- 4. Ближайшие гомологи фенолов - крезолы
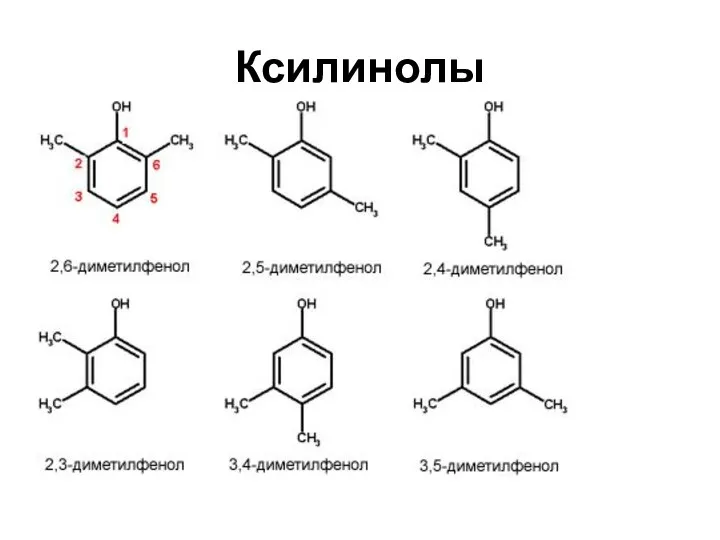
- 5. Ксилинолы
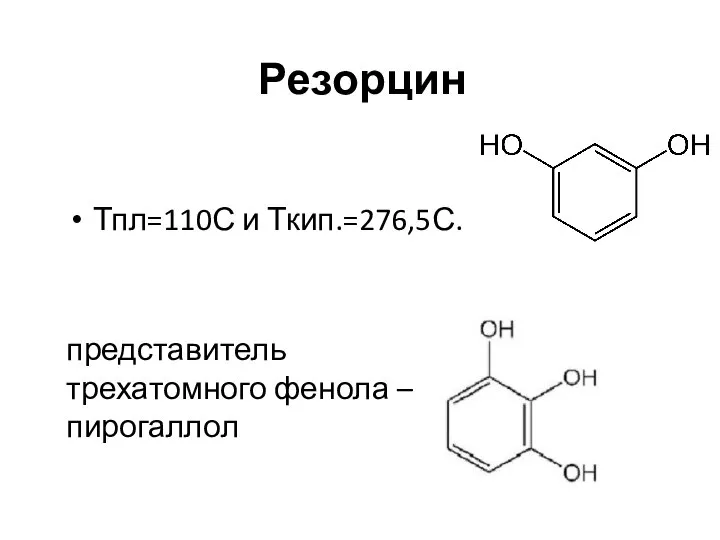
- 6. Резорцин Тпл=110С и Ткип.=276,5С. представитель трехатомного фенола – пирогаллол
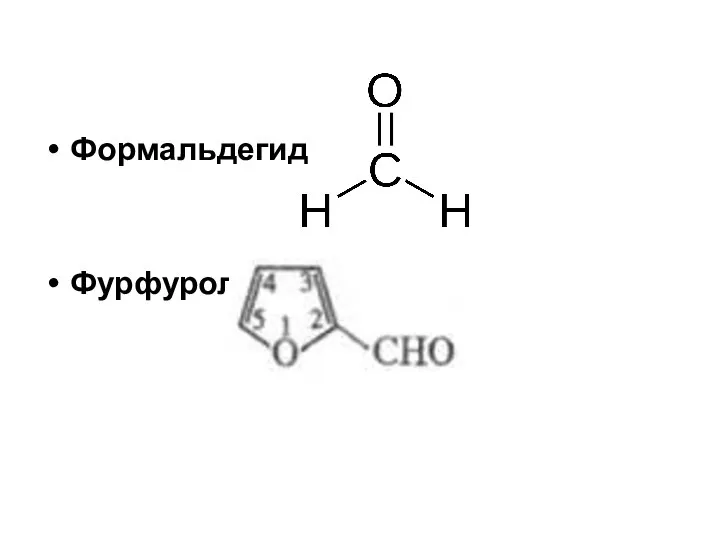
- 7. Формальдегид Фурфурол
- 8. Синтез фенолальдегидных полимеров При поликонденсации фенола и его гомологов с альдегидами могут образовываться как термопласты, так
- 9. Основные факторы, определяющие строение и свойства фенолальдегидных полимеров: функциональность фенола мольное соотношение фенола и альдегида рН
- 10. Функциональность фенолов – число атомов водорода в феноле и его гомологах, способных взаимодействовать с альдегидами Трифункциональные:
- 11. При поликонденсации формальдегида и фурфурола с трифункциональными фенолами - как термопластичные, так и термореактивные олигомеры. Бифункциональные
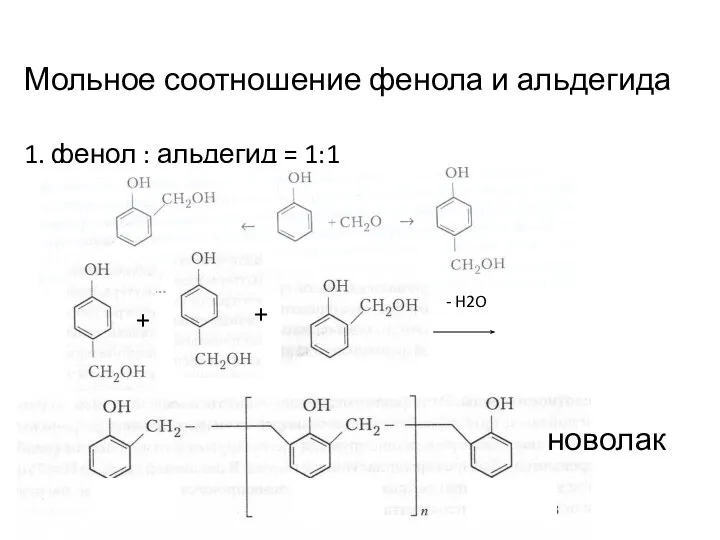
- 12. Мольное соотношение фенола и альдегида 1. фенол : альдегид = 1:1 + + - H2O новолак
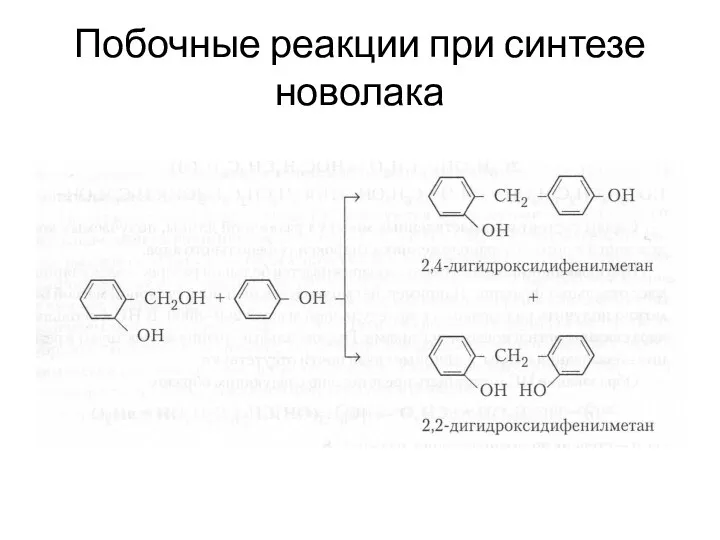
- 13. Побочные реакции при синтезе новолака
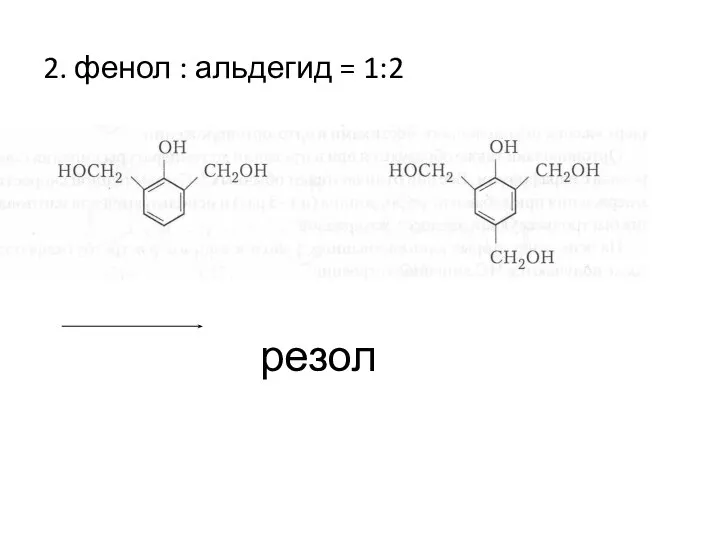
- 14. 2. фенол : альдегид = 1:2 резол
- 15. Кислотность среды Кислая среда (рН Щелочная среда (рН > 7): фенолоспирты устойчивы → конденсация при нагревании
- 16. Взаимодействие трифункциональных фенолов с формальдегидом Образование новолака Избыток фенола (фенол/формальдегид=1/ 0,78-0,86). Кислая среда. При отсутствии избытка
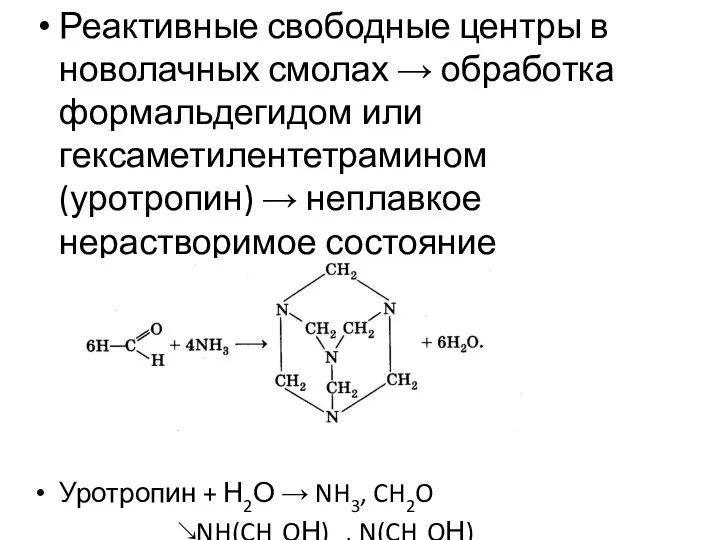
- 17. Реактивные свободные центры в новолачных смолах → обработка формальдегидом или гексаметилентетрамином (уротропин) → неплавкое нерастворимое состояние
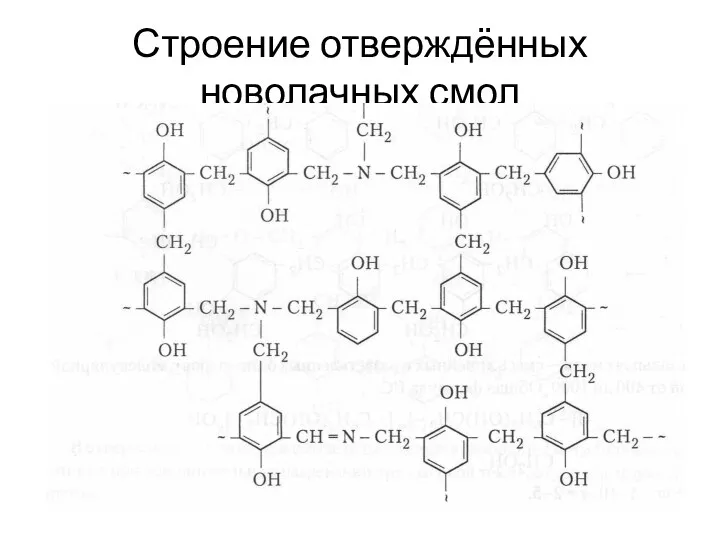
- 18. Строение отверждённых новолачных смол
- 19. Резол – смесь линейных и разветвлённых продуктов общей формулы:
- 20. Синтез резольной смолы
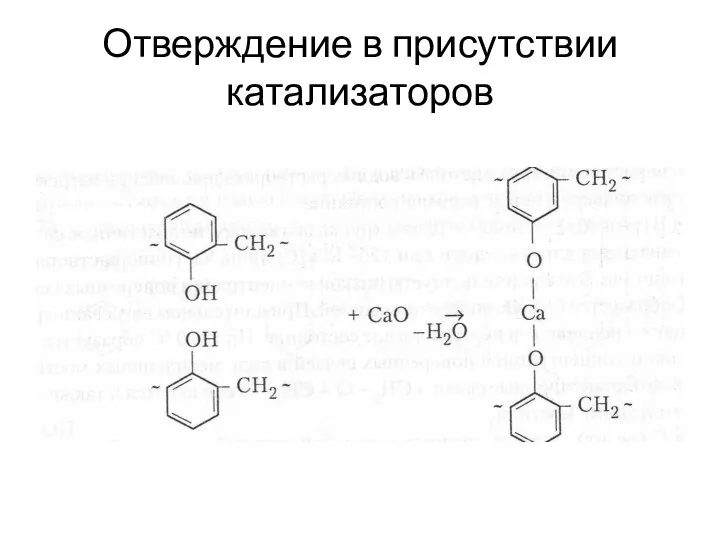
- 21. Отверждение в присутствии катализаторов
- 22. Стадии отверждения Стадия А (резольная) – олигомер по свойствам близок к новолаку (плавится, растворяется в щелочах
- 23. Строение резита
- 25. Скачать презентацию











 Тема: Химическая связь и ее типы Урок химии в 11 классе
Тема: Химическая связь и ее типы Урок химии в 11 классе Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений
Строение и переваривание липидов. Классификация и роль жирных кислот. Нутриомика. Липофильных соединений Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть
Презентация по Химии "Глюкоза. Строение. Физические и химические свойства" - скачать смотреть  Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Alkanes. A “family” of hydrocarbons
Alkanes. A “family” of hydrocarbons Фенол Подготовил Ежов Сергей
Фенол Подготовил Ежов Сергей Орагническая химия. Теория А.М. Бутлерова
Орагническая химия. Теория А.М. Бутлерова Продолжение лекции «Химическая связь»
Продолжение лекции «Химическая связь»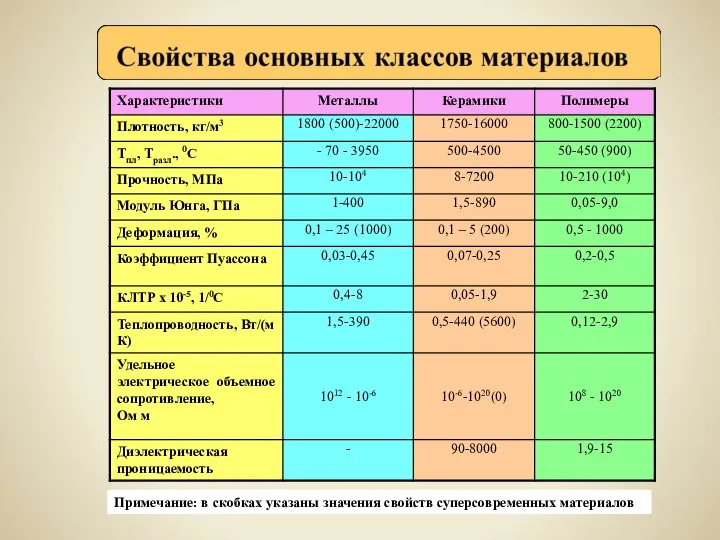 Свойства основных классов материалов
Свойства основных классов материалов Алканы и алкены
Алканы и алкены Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение Логическая структура модуля по дисциплине Аналитическая химия
Логическая структура модуля по дисциплине Аналитическая химия Аммофос өндірісі. Алыну әдісі
Аммофос өндірісі. Алыну әдісі Лабораторные занятия по теме: Методы защиты электрооборудования от коррозии
Лабораторные занятия по теме: Методы защиты электрооборудования от коррозии Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Гидролиз солей. Составила: Рудчинкова Л.Ю., учитель химии и биологии МОУ «СОШ им. М.М. Рудченко с. Перелюб Перелюбского района Сарато
Гидролиз солей. Составила: Рудчинкова Л.Ю., учитель химии и биологии МОУ «СОШ им. М.М. Рудченко с. Перелюб Перелюбского района Сарато Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Межкристаллитная коррозия МКК
Межкристаллитная коррозия МКК Механизмы двухсубстатных реакций
Механизмы двухсубстатных реакций Начала физической химии
Начала физической химии Альдегиды и кетоны: свойства, получение, применение
Альдегиды и кетоны: свойства, получение, применение Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом
Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом Липиды. Классификация липидов
Липиды. Классификация липидов Орбитали и связи
Орбитали и связи Общая и медицинская химия
Общая и медицинская химия Циклоалканы. Строение, изомерия, получение и свойства
Циклоалканы. Строение, изомерия, получение и свойства Белки. Структуры белков
Белки. Структуры белков