Содержание
- 2. План лекции Свойства растворов электролитов Закон разбавления Оствальда Теория сильных электролитов Ионная сила раствора Закон Дебая-Хюккеля
- 3. Растворы электролитов Имеют более высокое, чем по закону Вант-Гоффа, осмотическое давление Кипят при более высокой температуре
- 4. Изотонический коэффициент i π = СRT π = iСRT Показывает, во сколько раз наблюдаемое осмотическое давление
- 5. Степень диссоциации α Кол-во продиссоциированных молекул α = ----------------------------------------------------------- в долях, % Общее кол-во молекул Сильные
- 6. Степень диссоциации зависит: От температуры От концентрации раствора От природы растворенного вещества От диэлектрической проницаемости растворителя
- 7. Константа диссоциации Константа равновесия, отвечающая диссоциации слабого электролита CH3COOH ⮀ H+ + CH3COO- V1 = K1[CH3COOH]
- 8. Многоосновные кислоты, основания двух- и более валентных металлов диссоциируют ступенчато: 1.H3PO4 ⮀ H+ + H2PO4- 2.H2PO4-
- 9. Закон разбавления Оствальда При разбавлении раствора слабого электролита степень диссоциации увеличивается CH3COOH ⮀ CH3COO- + H+
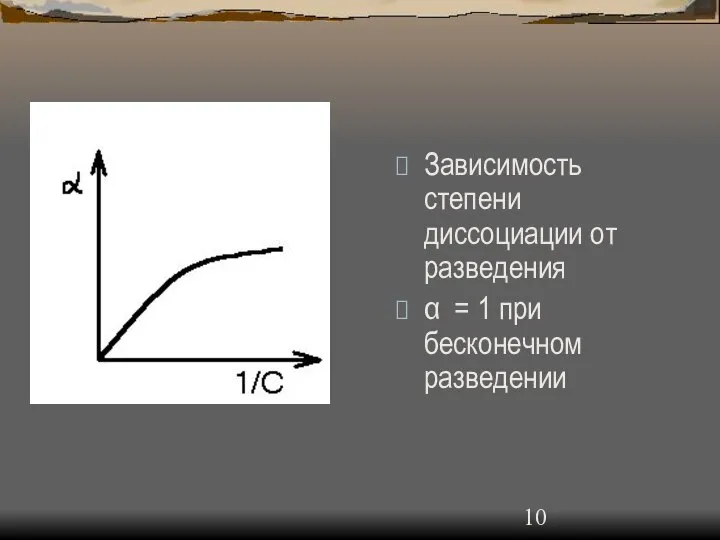
- 10. Зависимость степени диссоциации от разведения α = 1 при бесконечном разведении
- 11. Теория сильных электролитов В водных растворах электролитов концентрация ионов велика Расстояние между отдельными ионами невелико; между
- 12. Релаксационный эффект Ионная сфера и гидратная оболочка тормозят движение иона Электролит проявляет меньшую степень диссоциации, чем
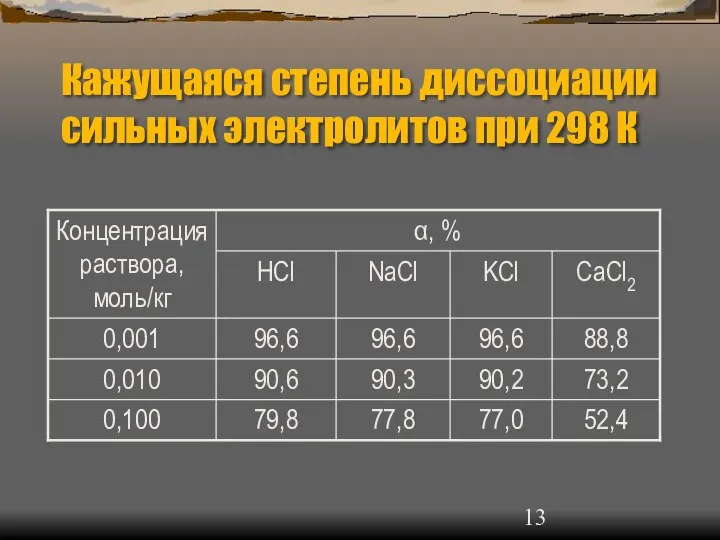
- 13. Кажущаяся степень диссоциации сильных электролитов при 298 К
- 14. Активность иона а Та эффективная условная концентрация иона, соответственно которой он действует при химических реакциях а
- 15. При очень больших концентрациях растворов некоторых электролитов f может быть больше 1, а > С. Это
- 16. Ионная сила раствора I Величина, измеряемая полусуммой произведений концентраций каждого иона на квадрат его заряда I
- 17. Закон Дебая-Хюккеля В разбавленных растворах сильных электролитов с одинаковой ионной силой коэффициенты активности катионов и анионов
- 18. Активность ионов является эффективной концентрацией, проявляющей себя при химических реакциях Если пользоваться активность вместо концентрации, то
- 19. Эффект Гиббса-Доннана Сн2 Х = ------------- Св + 2Сн
- 20. Если до начала перераспределения концентрация Naн+ была значительно выше, чем внутри клетки Сн >> Cв Сн2
- 21. При соприкосновении клетки с раствором электролита некоторое количество электролита перейдет в клетку. Поэтому осмотическое давление, зависящее
- 22. Влияние электролитов на растворимость газов Закон Генри-Дальтона Количество газа, растворенного при данной температуре в определенном объеме
- 23. Закон Сеченова Растворимость газов в жидкостях в присутствии электролитов понижается; происходит высаливание газов С = С0
- 24. Физиологическое действие ионов Антагонизм Молибден и медь: увеличивая содержание Cu можно снизить токсичность Mo и наоборот
- 26. Скачать презентацию





















 Природные и синтетические полимеры. Способы получения полимеров
Природные и синтетические полимеры. Способы получения полимеров Ароматические углеводороды
Ароматические углеводороды Строение атома
Строение атома Углеводороды (УВ)
Углеводороды (УВ) Презентация по химии Карбоновые кислоты и их производные
Презентация по химии Карбоновые кислоты и их производные  Типы первичных химических источников тока
Типы первичных химических источников тока Химический состав водотоков архипилага Новая земля и их воздействие на прибрежную зону
Химический состав водотоков архипилага Новая земля и их воздействие на прибрежную зону Галогены. Свойства галогенов
Галогены. Свойства галогенов Аминокислоты
Аминокислоты Сравнительная характеристика бензольного кольца и олимпийских колец
Сравнительная характеристика бензольного кольца и олимпийских колец Антуан Лоран Лавуазье 1743–1794 гг. Заложил основу анализа органических соединений
Антуан Лоран Лавуазье 1743–1794 гг. Заложил основу анализа органических соединений Техника безопасности для учащихся в кабинете химии.
Техника безопасности для учащихся в кабинете химии.  Серная кислота H2SO4
Серная кислота H2SO4 Изменение числа электронов на внешнем энергетическом уровне атомов химических элементов. Ионная связь
Изменение числа электронов на внешнем энергетическом уровне атомов химических элементов. Ионная связь Жоғары температурағы асқын өткізгіштер
Жоғары температурағы асқын өткізгіштер Хром. Основні характеристики
Хром. Основні характеристики Визначення якості мила за його лужністю
Визначення якості мила за його лужністю Обмен жиров в организме
Обмен жиров в организме Типы химических реакций
Типы химических реакций Оксид кальция (СаО)
Оксид кальция (СаО) Алканы: физические и химические свойства, получение
Алканы: физические и химические свойства, получение Окислительно-восстановительные процессы. Лекция 8
Окислительно-восстановительные процессы. Лекция 8 Йод в организме человека
Йод в организме человека Презентация Классификация полимеров 11 класс
Презентация Классификация полимеров 11 класс  Обмен липидов
Обмен липидов Химическое загрязнение почвы
Химическое загрязнение почвы Способы количественного определения белка. (Лекция 10)
Способы количественного определения белка. (Лекция 10) Нуклеофильное замещение у насыщенного атома углерода, SN у Csp3
Нуклеофильное замещение у насыщенного атома углерода, SN у Csp3