Содержание
- 2. Химические реакции или химические явления – это процессы, в результате которых из одних веществ образуются другие.
- 3. По каким признакам можно определить химические реакции? Выделение газа; Образование осадка; Выделение (поглощение) тепла и света;
- 4. Каковы условия возникновения реакций? Растворение; Измельчение; Смешивание веществ; Нагревание.
- 5. Химические реакции Как классифицировать?
- 6. Реакции соединения 2Аl+ 3I2 = 2 All3 NH3 + HCl = NH4Cl 1.
- 7. Реакции, в которых из нескольких простых или сложных веществ образуется одно более сложное вещество, наз. реакциями
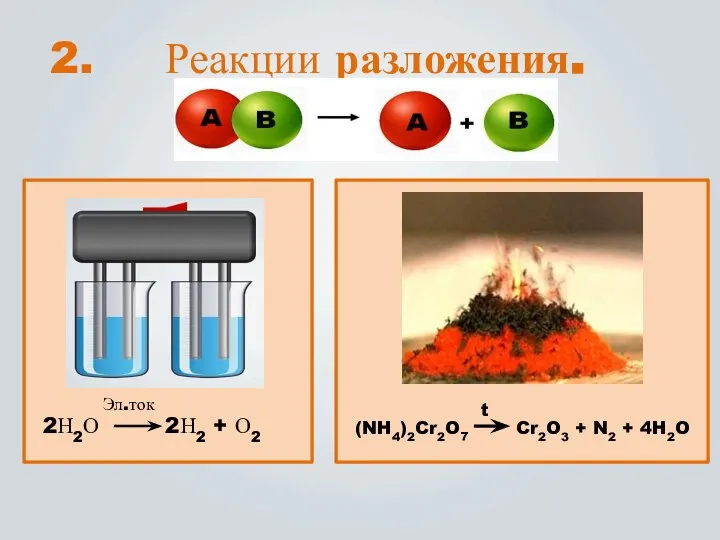
- 8. Реакции разложения. (NH4)2Cr2O7 Cr2O3 + N2 + 4H2O t 2Н2О 2Н2 + О2 Эл.ток 2.
- 9. Реакции, в которых из одного сложного вещества получается два или несколько простых или сложных веществ, наз.
- 10. Реакции замещения. SnCl2 + Zn = ZnCl2 + Sn H2SO4 + Zn = ZnSO4 + H2↑
- 11. Реакции, протекающие между простыми и сложными веществами, при которых атомы простого вещества замещают атомы одного из
- 12. Реакции обмена. Pb(NO3)2 +2KI = PbI2↓+2KNO3 2 NaOH + H2SO4 = Na2SO4 + 2H2O 4.
- 13. Реакции, происходящие между сложными веществами, в результате которых они меняются своими составными частями, наз. реакциями обмена.
- 14. Реакции обмена С выпадением осадка С выделением газа С выделением воды ↓ ↑
- 15. Реакции обмена в растворах электролитов протекают в тех случаях, когда: 1. Образуется осадок. AgNO3 + NaCl
- 16. 2. Образуется газ (или легколетучие вещества). Na2S + H2SO4 = Na2SO4 + H2S↑ молекулярное уравнение реакции
- 17. 3. Образуется слабый электролит (малодиссоциирующее соединение). NaOH + HCl = NaCl + H2O молекулярное уравнение реакции
- 18. В том случае, если образующиеся вещества - сильные электролиты, хорошо растворимые в воде и полностью диссоциирующие
- 20. Скачать презентацию
















 Строение, получение и применение полимеров
Строение, получение и применение полимеров Презентация Нефть и способы ее переработки
Презентация Нефть и способы ее переработки Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные
Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные Аттестаионная работа. Сахар. Изучаем и исследуем
Аттестаионная работа. Сахар. Изучаем и исследуем Химический состав клетки. Неорганические вещества клетки
Химический состав клетки. Неорганические вещества клетки Презентация по Химии "Химическое загрязнение среды промышленностью." - скачать смотреть бесплатно
Презентация по Химии "Химическое загрязнение среды промышленностью." - скачать смотреть бесплатно Презентация по Химии "Косметичні засоби" - скачать смотреть бесплатно
Презентация по Химии "Косметичні засоби" - скачать смотреть бесплатно Влияние шампуня на состояние волос человека
Влияние шампуня на состояние волос человека Презентация по Химии "Комплексные соединения" - скачать смотреть
Презентация по Химии "Комплексные соединения" - скачать смотреть  Аналитическая химия и химический анализ. (Лекция 1)
Аналитическая химия и химический анализ. (Лекция 1) Углеводы. Моносахариды. Лекция 5
Углеводы. Моносахариды. Лекция 5 Гетерогенные и лигандообменные равновесия и процессы
Гетерогенные и лигандообменные равновесия и процессы Детонаційна стійкість бензину
Детонаційна стійкість бензину Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола
Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола Энергетика химических процессов. Энтропия и энергия Гиббса
Энергетика химических процессов. Энтропия и энергия Гиббса Химитариум. Погрузись в мир занимательной химии
Химитариум. Погрузись в мир занимательной химии Роль минеральных веществ в организме человека
Роль минеральных веществ в организме человека Поверхностные явлении и дисперсные системы (коллоидная химия)
Поверхностные явлении и дисперсные системы (коллоидная химия) Производство топлив и масел
Производство топлив и масел Полимеры, пластмассы и товары на их основе
Полимеры, пластмассы и товары на их основе Альдегиды и кетоны
Альдегиды и кетоны Физико-химическая и механическая миграция
Физико-химическая и механическая миграция Свойства снега и льда (окружающий мир, 3 класс)
Свойства снега и льда (окружающий мир, 3 класс) Роль воды в жизни и хозяйстве
Роль воды в жизни и хозяйстве Магнитті қатты материалдар және оны техникада қолдану әдістері
Магнитті қатты материалдар және оны техникада қолдану әдістері Презентация Угольная кислота
Презентация Угольная кислота Кальцій і Магній
Кальцій і Магній  Фотометрический анализ III курс, д/о Преподаватель Ельчищева Юлия Борисовна
Фотометрический анализ III курс, д/о Преподаватель Ельчищева Юлия Борисовна