Содержание
- 2. Термодинамическая теория фазовых равновесий, основанная на экспериментальных данных, позволяет оптимизировать условия получения различных веществ, в том
- 3. Общий случай фазовых равновесий любых систем описывается правилом фаз Гиббса. Это один из наиболее общих законов
- 4. Основные понятия и определения Фаза – это совокупность одинаковых по химическому составу, химическим и физическим свойствам
- 5. Системы, содержащие одну фазу, называются гомогенными, две и более - гетерогенными. Примеры различных систем
- 6. Компонент – это составная часть системы, включающая одно простое или сложное вещество. Наименьшее число компонентов системы,
- 7. Степень свободы – это число термодинамических параметров (t, p, c ), определяющих состояние системы, которые можно
- 8. Условия равновесия • С = К – Ф + n при любом числе фаз количество таких
- 9. Уравнение правила фаз устанавливает связь между числом степеней свободы, числом компонентов и числом фаз в данной
- 10. Системы принято классифицировать По числу фаз: однофазные двухфазные По числу компонентов: однокомпонентные двухкомпонентные По числу степени
- 11. Однокомпонентные системы В однокомпонентных системах могут быть одна, две или три устойчиво существующих фазы: твердая, жидкая,
- 12. Уравнение Клаузиуса - Клапейрона
- 13. Расчет теплоты испарения и возгонки по уравнению Клапейрона – Клаузиуса Для процессов испарения и возгонки изменение
- 14. Расчет теплоты испарения и возгонки по уравнению Клапейрона – Клаузиуса Аналитический способ: После интегрирования уравнения в
- 15. Расчет теплоты испарения и возгонки по уравнению Клапейрона – Клаузиуса После интегрирования уравнения в неопределенных пределах:
- 16. Пример: Определите давление, при котором вода закипит при 98°С. Решение: Кипение воды представляет собой фазовый переход:
- 17. Давление пара бензола при 20°С и 30°С соответственно равно 100·102 Па и 157·102 Па. Рассчитайте молярную
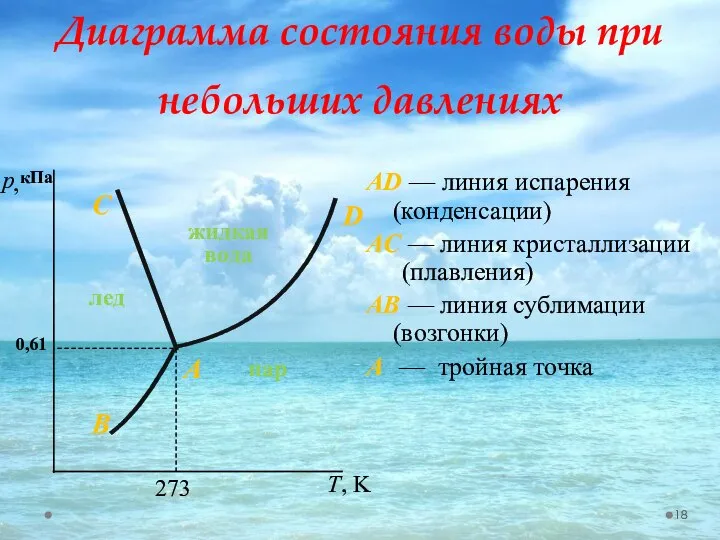
- 18. Диаграмма состояния воды при небольших давлениях АD — линия испарения (конденсации) AC — линия кристаллизации (плавления)
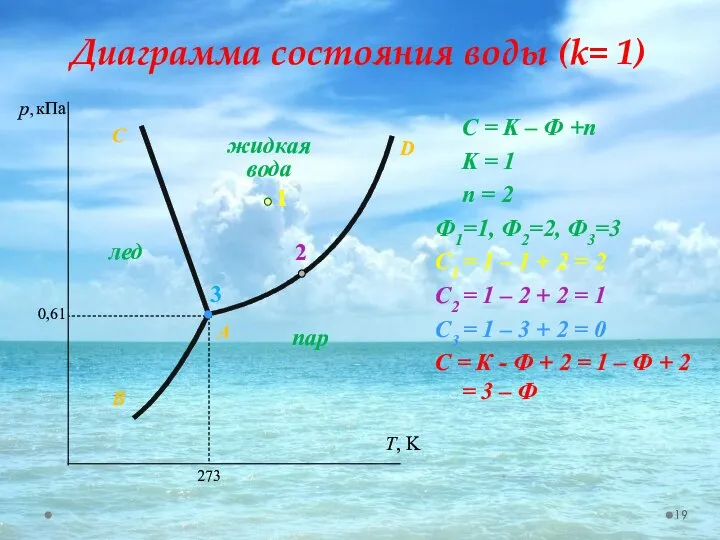
- 19. С = K – Ф +n K = 1 n = 2 Ф1=1, Ф2=2, Ф3=3 С1
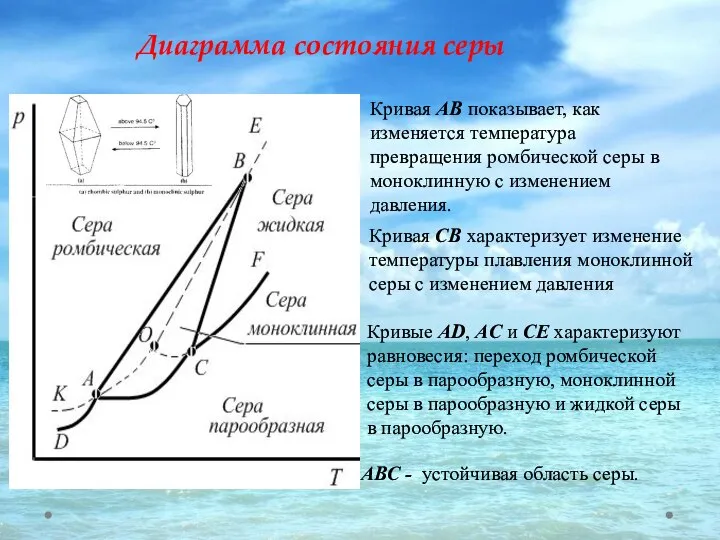
- 20. Диаграмма состояния серы АВС - устойчивая область серы. Кривая АВ показывает, как изменяется температура превращения ромбической
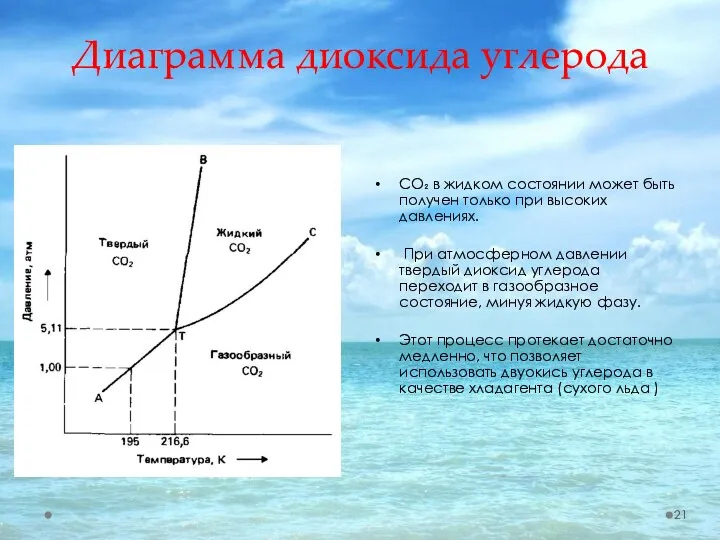
- 21. Диаграмма диоксида углерода СО₂ в жидком состоянии может быть получен только при высоких давлениях. При атмосферном
- 22. Диаграмма гелия При температуре ниже T = 2,172К жидкий гелий испытывает фазовый переход, переходя из «нормального»
- 24. Понятие о физико-химическом анализе. Термический анализ Учение о зависимости свойств многокомпонентных систем (давление пара, температура плавления,
- 25. Принцип соответствия Согласно принципу соответствия, на диаграмме состояния системы каждой фазе соответствует часть плоскости – поле
- 26. Визуальный метод применяю если система состоит из прозрачных компонентов и температура не слишком низкая и не
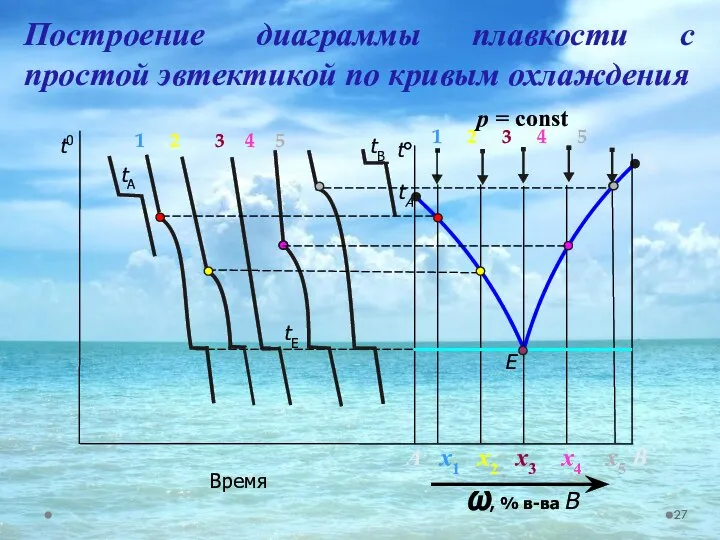
- 27. Построение диаграммы плавкости с простой эвтектикой по кривым охлаждения p = const 1 2 3 4
- 28. Рассмотрим общий вид диаграммы двухкомпонентной системы. Линии АО и ВО называется линиями ликвидуса. Выше этих линий
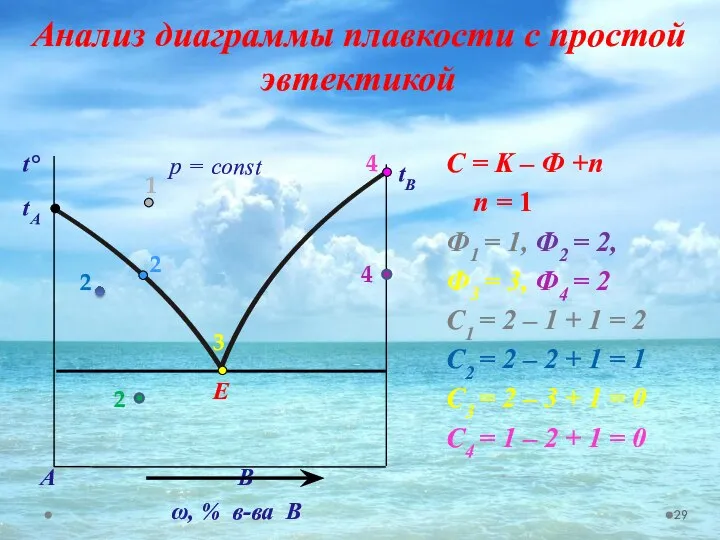
- 29. Анализ диаграммы плавкости с простой эвтектикой С = K – Ф +n n = 1 Ф1
- 30. Правило рычага |GK |·m p=|GH |·m кp m p = m см – m кр m
- 31. Вернемся к точке g. Согласно правилу рычага, фигуративная точка системы, например, точка g, делит проходящую через
- 32. Химические соединения Твердое химическое соединение постоянного состава – однофазная система, имеющая одну кристаллическую решетку, в которой
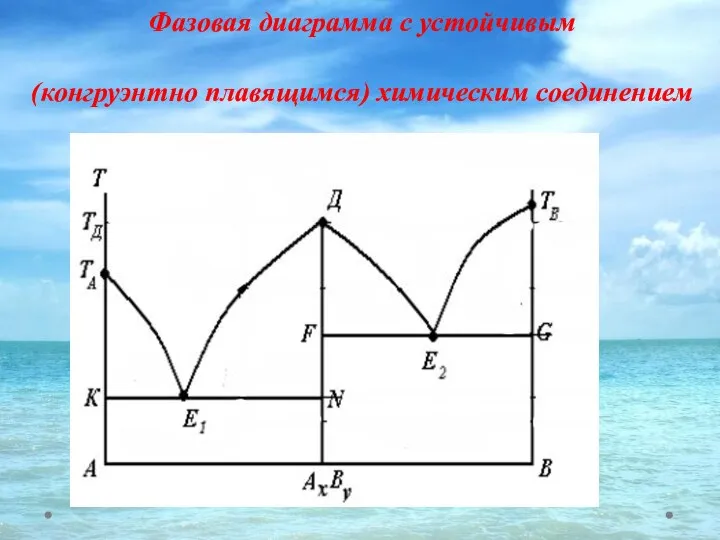
- 33. Фазовая диаграмма с устойчивым (конгруэнтно плавящимся) химическим соединением
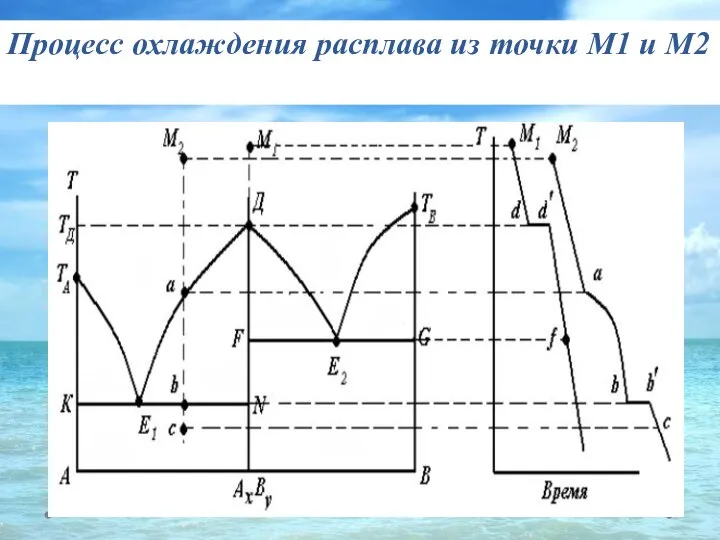
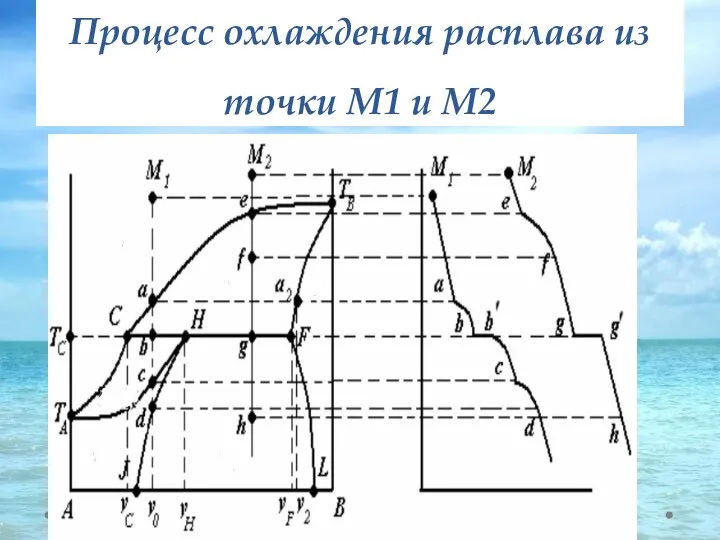
- 34. Процесс охлаждения расплава из точки М1 и М2
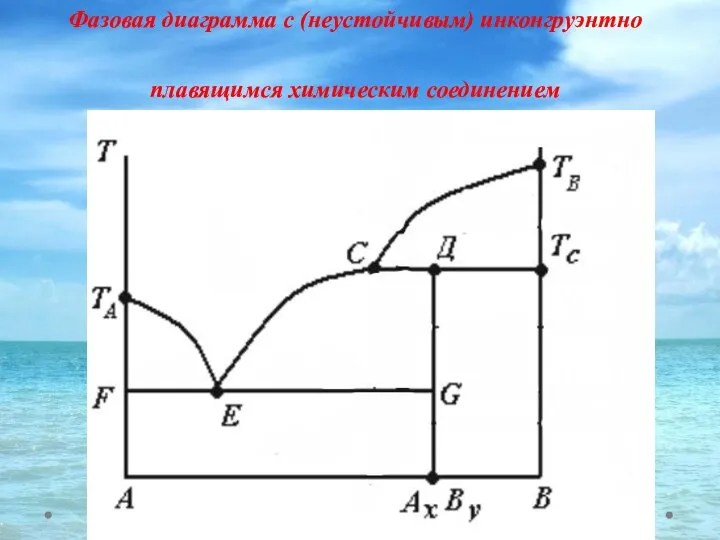
- 35. Фазовая диаграмма с (неустойчивым) инконгруэнтно плавящимся химическим соединением
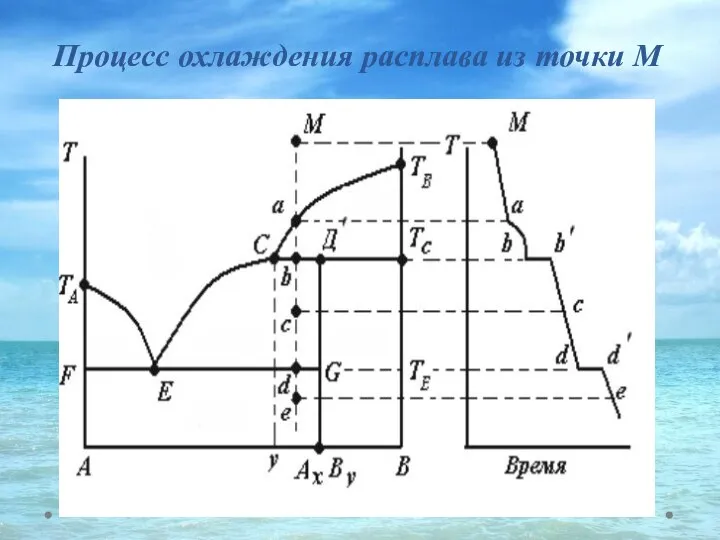
- 36. Процесс охлаждения расплава из точки М
- 37. Твердые растворы Твердые растворы – гомогенные системы переменного состава, состоящие из двух или более компонентов.
- 38. Типы твердых растворов Твердые растворы внедрения – растворы, при кристаллизации которых частицы (атомы, молекулы или ионы)
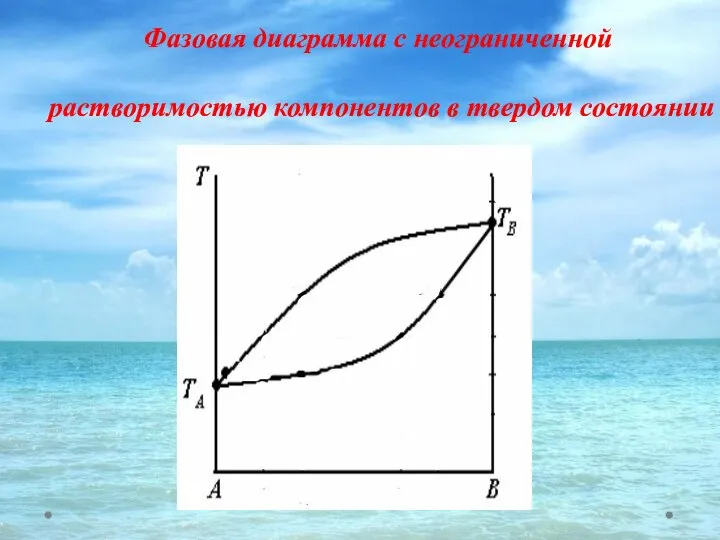
- 39. Фазовая диаграмма с неограниченной растворимостью компонентов в твердом состоянии
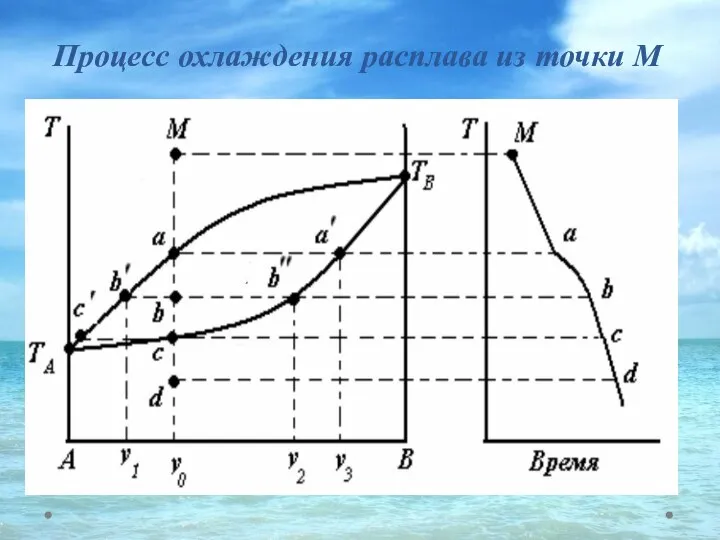
- 40. Процесс охлаждения расплава из точки М
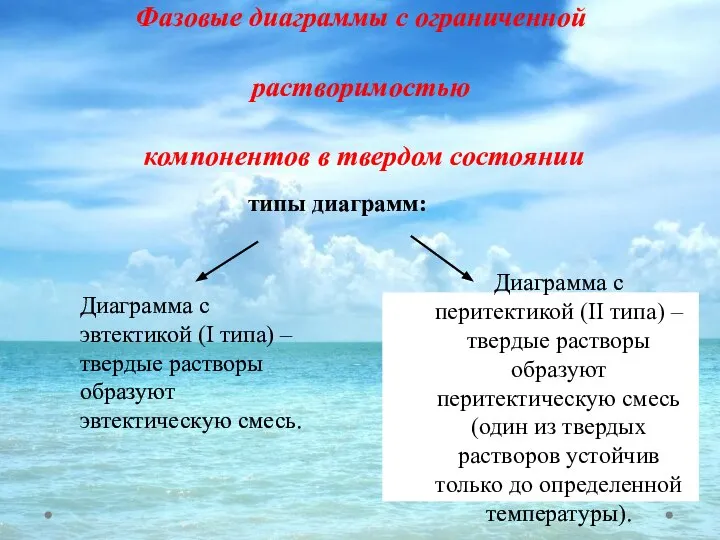
- 41. Фазовые диаграммы с ограниченной растворимостью компонентов в твердом состоянии Диаграмма с перитектикой (II типа) – твердые
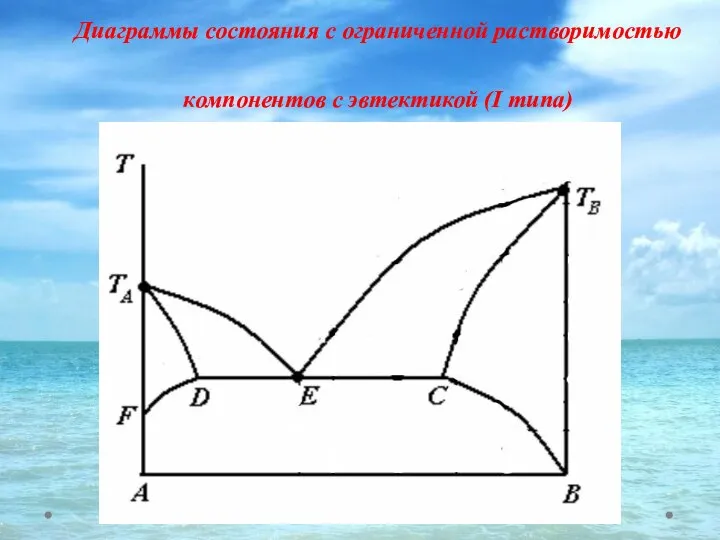
- 42. Диаграммы состояния с ограниченной растворимостью компонентов с эвтектикой (I типа)
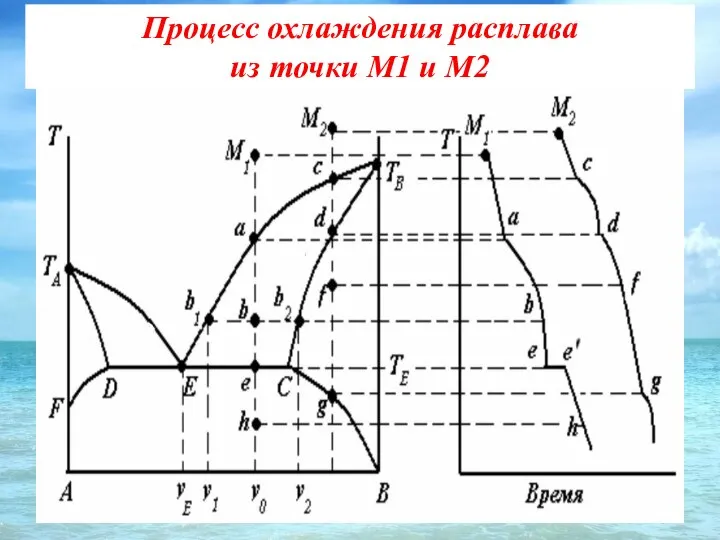
- 43. Процесс охлаждения расплава из точки М1 и М2
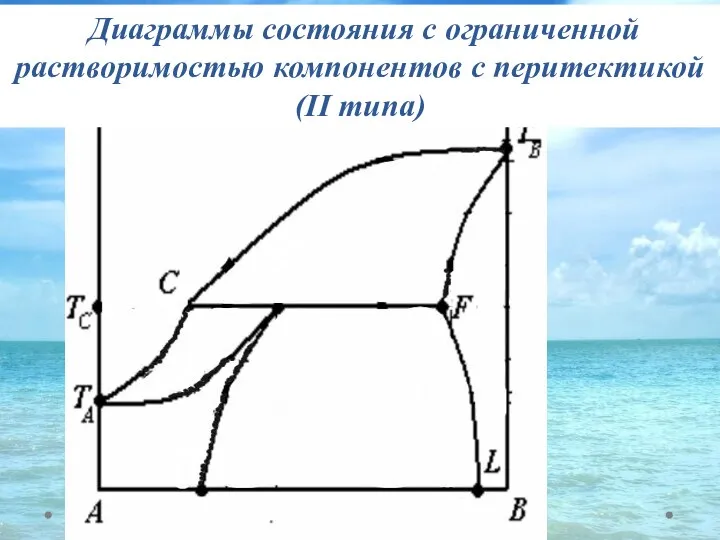
- 44. Диаграммы состояния с ограниченной растворимостью компонентов с перитектикой (II типа)
- 45. Процесс охлаждения расплава из точки М1 и М2
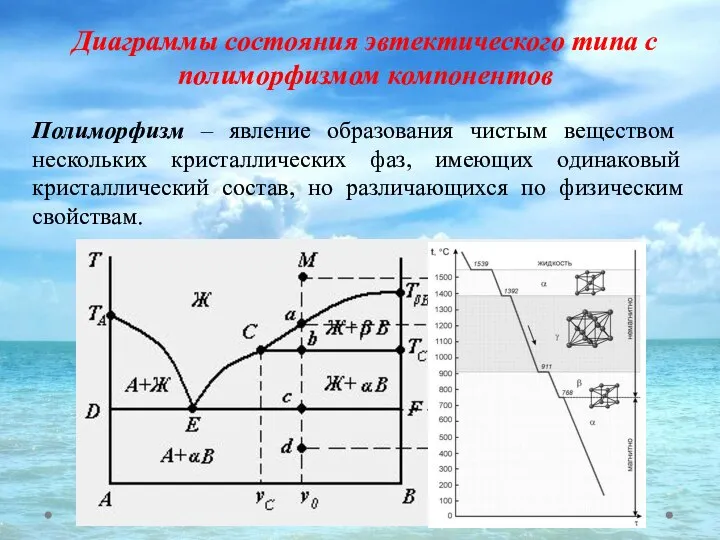
- 46. Полиморфизм – явление образования чистым веществом нескольких кристаллических фаз, имеющих одинаковый кристаллический состав, но различающихся по
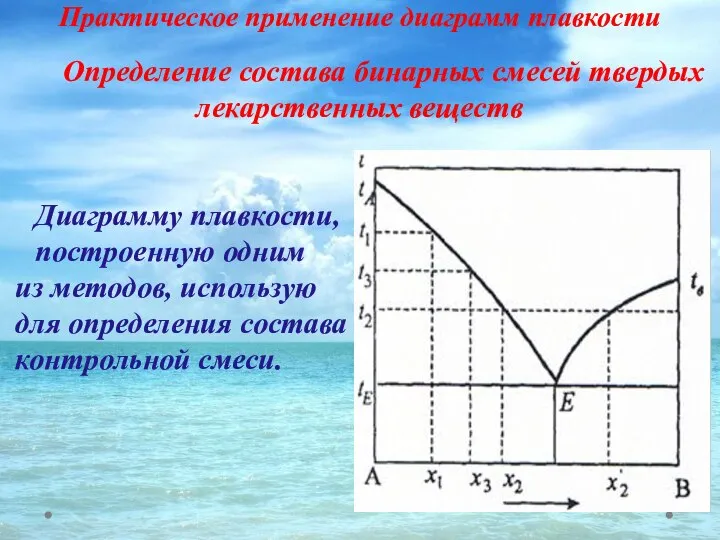
- 47. Практическое применение диаграмм плавкости Определение состава бинарных смесей твердых лекарственных веществ Диаграмму плавкости, построенную одним из
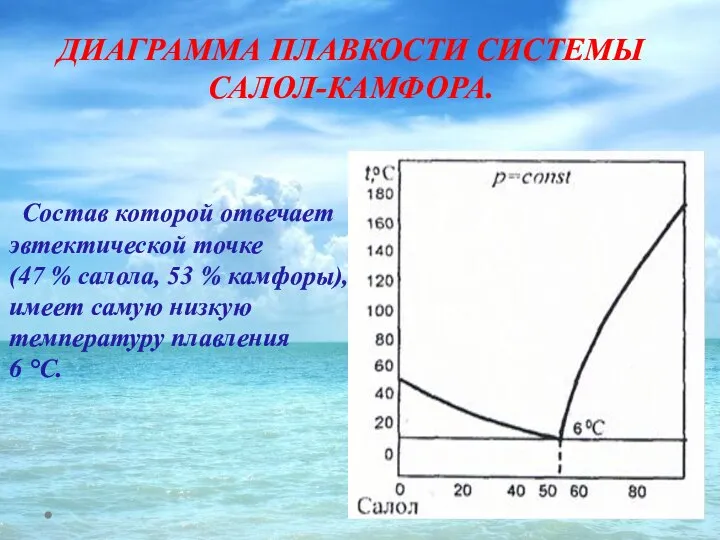
- 48. ДИАГРАММА ПЛАВКОСТИ СИСТЕМЫ САЛОЛ-КАМФОРА. Cостав которой отвечает эвтектической точке (47 % салола, 53 % камфоры), имеет
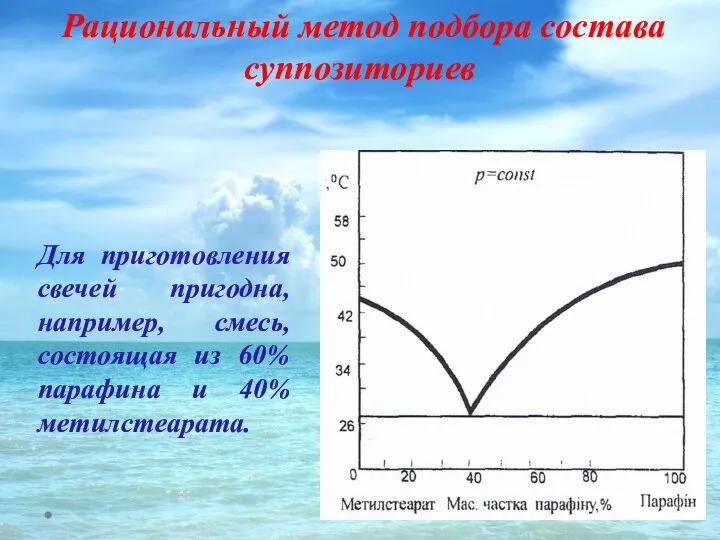
- 49. Рациональный метод подбора состава суппозиториев Для приготовления свечей пригодна, например, смесь, состоящая из 60% парафина и
- 50. Повышение биодоступности твердых лекарственных форм. Сехигуки и Оби (1961) был предложен способ повышения степени дисперсности ряда
- 52. Если взять две несмешивающиеся жидкости и добавить третий компонент, то он будет растворяться в разной степени
- 53. Отношение равновесных концентраций вещества в органическом растворителе и в воде есть величина постоянная при данной температуре.
- 54. Экстракция — это процесс извлечения одного или нескольких веществ из сложных систем (жидких или твердых) селективным
- 56. хорошо оправдывается если: добавление вещества к системе не вызывает изменения взаимной растворимости жидких фаз; растворенное вещество
- 57. При распределении уксусной или бензойной кислоты между водой и бензолом в бензоле образуются двойные молекулы (ассоциация),
- 58. Зная коэффициент распределения К, можно рассчитать количество вещества, оставшееся в растворе после однократного или многократного извлечения
- 59. mn — масса вещества, оставшегося в растворе после n экстракций; V — объем экстрагента; V0 —
- 61. Скачать презентацию





































 Классификация химических, физических и механических свойств порошка
Классификация химических, физических и механических свойств порошка Нуклеиновые кислоты
Нуклеиновые кислоты Вредные вещества
Вредные вещества Технологии создания и обработки кристаллических материалов
Технологии создания и обработки кристаллических материалов Номенклатура органических соединений
Номенклатура органических соединений Неметаллы
Неметаллы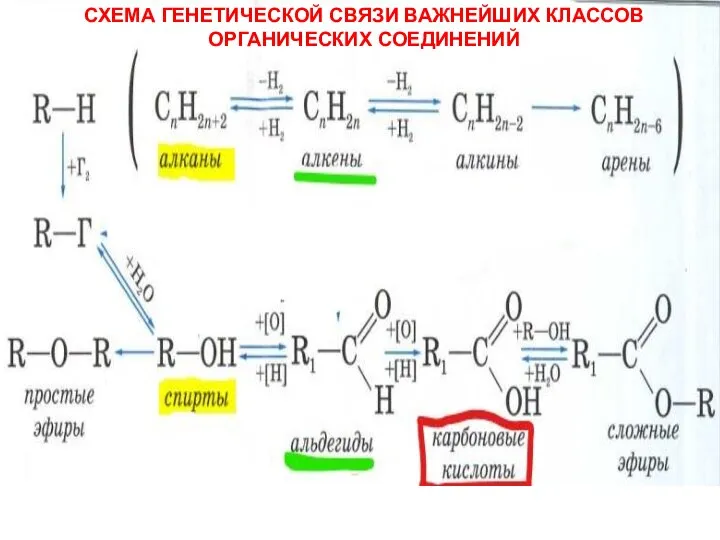 Схема генетической связи важнейших классов органических соединений
Схема генетической связи важнейших классов органических соединений Технология получения гидропероксида изопропилбензола
Технология получения гидропероксида изопропилбензола Iodine
Iodine Коллигативные свойства растворов. Осмос. Осмотическое давление. (Лекция 4)
Коллигативные свойства растворов. Осмос. Осмотическое давление. (Лекция 4) Презентация по Химии "Дисперсные системы" - скачать смотреть
Презентация по Химии "Дисперсные системы" - скачать смотреть  Морфология палочковидных и извитых бактерий. Краски используемые в микробиологии. Приготовление бакпрепаратов. Методы окраски
Морфология палочковидных и извитых бактерий. Краски используемые в микробиологии. Приготовление бакпрепаратов. Методы окраски Классификация, номенклатура углеводородов
Классификация, номенклатура углеводородов Химиялық қауіптілер. Нитраттар
Химиялық қауіптілер. Нитраттар Химическая связь в твердых телах. Классификация твердых тел по типу химической связи
Химическая связь в твердых телах. Классификация твердых тел по типу химической связи Выделение нефтегазоматеринских пород по данным пиролиза. Построение геохимического разреза
Выделение нефтегазоматеринских пород по данным пиролиза. Построение геохимического разреза Методы защиты от коррозии
Методы защиты от коррозии Реакции подлинности лекарственных веществ
Реакции подлинности лекарственных веществ Презентация по Химии "Синтетические моющие средства или химия в ванной" - скачать смотреть _
Презентация по Химии "Синтетические моющие средства или химия в ванной" - скачать смотреть _ Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5)
Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5) Применение синтетических полимеров в вооружении
Применение синтетических полимеров в вооружении Витамины. Классификация витаминов
Витамины. Классификация витаминов Реакции ионного обмена
Реакции ионного обмена Геохимия природных процессов. Редкие элементы, как индикаторы геодинамических обстановок формирования комплексов. (Лекция 5)
Геохимия природных процессов. Редкие элементы, как индикаторы геодинамических обстановок формирования комплексов. (Лекция 5) Химия атмосферы
Химия атмосферы Электронная конфигурация атома
Электронная конфигурация атома Сера и ее соединения
Сера и ее соединения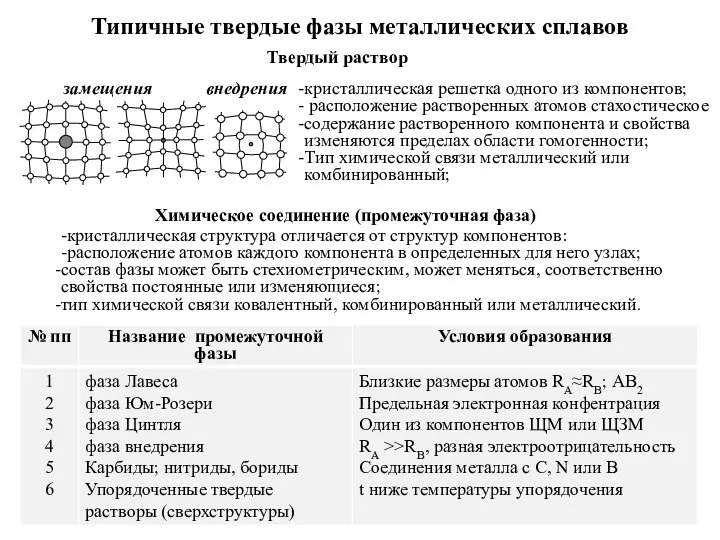 Типичные твердые фазы металлических сплавов
Типичные твердые фазы металлических сплавов