Содержание
- 2. Предмет физической и коллоидной химии ПРЕДМЕТОМ ФИЗИЧЕСКОЙ ХИМИИ ЯВЛЯЕТСЯ ОБЪЯСНЕНИЕ ХИМИЧЕСКИХ ЯВЛЕНИЙ НА ОСНОВЕ БОЛЕЕ ОБЩИХ
- 3. Предмет физической и коллоидной химии В курсе физической химии обычно выделяют несколько разделов. Строение вещества. В
- 4. Предмет физической и коллоидной химии Химическая термодинамика изучает энергетические эффекты химических процессов; позволяет определить возможность, направление
- 5. Предмет физической и коллоидной химии Электрохимия изучает особенности свойств растворов электролитов, явления электропроводности, электролиза, явление коррозии,
- 6. Связь физколлоидной химии с другими дисциплинами Физическая и коллоидная химия базируется на знаниях, полученных в результате
- 7. Тепловая энергия – форма энергии, связанная с движением атомов, молекул или других частиц, из которых состоит
- 8. Механическая энергия может переходить в тепловую энергию и обратно. Превращение механической энергии в тепловую и обратно
- 9. Термодинамика Термодинамика – раздел физики, изучающий соотношения и превращения теплоты и других форм энергии. Термодинамика представляет
- 10. Термодинамика — наука, изучающая взаимные превращения различных видов энергии, связанные с переходом энергии в форме теплоты
- 11. Приложение термодинамики к биологической материи Биоэнергетика - раздел термодинамики, изучающий биосистемы. Биоэнергетика — раздел биохимии, изучающий
- 12. Термохимия Термохимия - это раздел химии, изучающий тепловые эффекты химических процессов. Изобарные процессы – проходят при
- 13. ТЕРМИНЫ И ПОНЯТИЯ Система — это совокупность материальных объектов, отделённых от окружающей среды. Окружающая среда —
- 14. Термодинамическими параметры : экстенсивные и интенсивные. Если система изменяет свои параметры, то в ней происходит термодинамический
- 15. Нулевой закон термодинамики Если каждая из двух термодинамических систем находится в тепловом равновесии с некоторой третьей,
- 16. 1-й закон термодинамики 1-й закон термодинамики – это закон сохранения энергии. Впервые он был сформулирован Ломоносовым
- 17. 1-й закон термодинамики II. Невозможно создать перпетум-мобиле, или двигатель первого рода, т.е. осуществлять работу, не затрачивая
- 18. III. Теплота, подведенная к системе (или выделенная ею) расходуется на изменения внутренней энергии системы и совершение
- 19. IV. Увеличение внутренней энергии системы равно теплоте, которую система получает извне, за исключением работы, которую совершила
- 20. 1-й закон термодинамики
- 21. 1-й закон термодинамики Важно отметить, что Q и А зависят от того, каким образом совершен переход
- 22. А= р ∆ V Для изохорного процесса: V=const, A=0 и Qv=U2- U1 = ∆U Для изотермического:
- 23. Для изобарного: р=const, Qp = ∆U + р∆V или Qp = (U2 - U1) + p(V2
- 24. Природа теплового эффекта химических реакций. Термохимические уравнения. Тепловой эффект химической реакции - это количество теплоты, которая
- 25. Теплотой(энтальпией) сгорания называется тепловой эффект реакции взаимодействия 1 моля вещества с кислородом с образованием высших устойчивых
- 26. Типы тепловых эффектов Стандартная теплота фазовых превращений - это теплота превращения одного моля вещества при температуре
- 27. Типы тепловых эффектов Теплота нейтрализации. В случае разбавленных растворов теплота реакции нейтрализации молярной массы эквивалента сильной
- 28. Закон Гесса В 1840 г. Н. Г. Гесс сформулировал закон постоянства суммы тепла: Тепловой эффект реакции
- 29. Закон Гесса Например: PbSO4 можно получить разными путями: 1. Pb + S + 2O2 = PbSO4
- 30. Закон Гесса Тепловые эффекты реакций в термохимии рассчитывают, используя следствия из закона Гесса. I-е следствие: тепловой
- 31. Закон Гесса II-е - следствие: тепловой эффект реакции равен разности между суммой теплот сгорания исходных веществ
- 32. Закон Гесса III - следствие: Тепловой эффект прямой реакции равен тепловому эффекту обратной реакции с противоположным
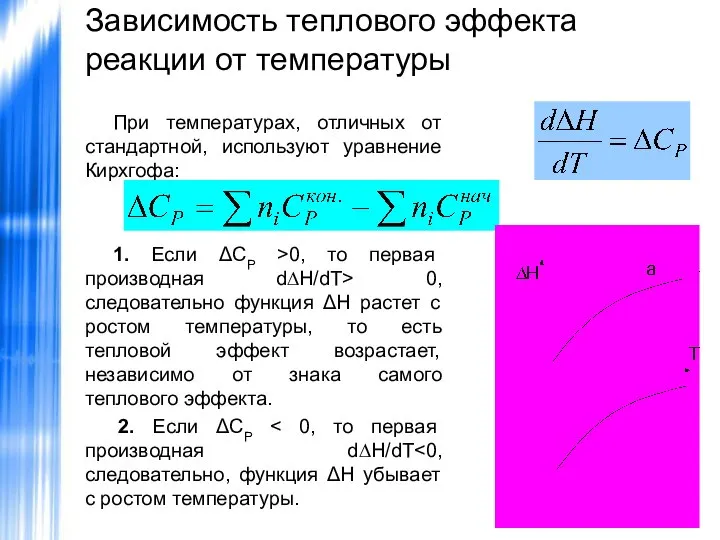
- 33. Зависимость теплового эффекта реакции от температуры При температурах, отличных от стандартной, используют уравнение Кирхгофа: 1. Если
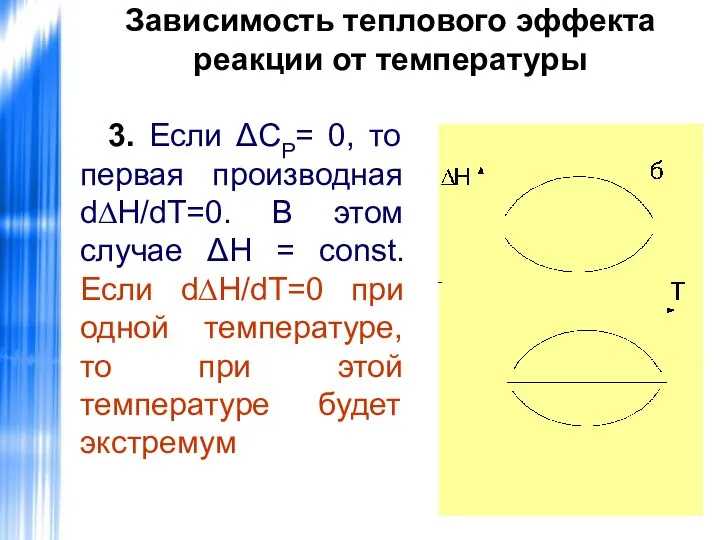
- 34. Зависимость теплового эффекта реакции от температуры 3. Если ΔСР= 0, то первая производная d∆H/dT=0. В этом
- 35. Зависимость теплового эффекта реакции от температуры Интегрирование уравнения Кирхгофа приводит позволяет рассчитать тепловой эффект реакции при
- 36. Исследование термохимических расчетов для энергетической характеристики биохимических процессов В приложении к живому организму закон сохранения энергии
- 37. Предполагается, что теплозатрата организма человека при условии умеренного климата в среднем равна 7100 кДж в сутки.
- 38. Пища включает главным образом жиры, белки, углеводы, минеральные соли, витамины, воду. Энергию дают, в основном, жиры,
- 39. 2-й закон термодинамики Второй закон термодинамики дает ответ на вопрос: возможен ли тот или иной процесс,
- 40. 2-й закон термодинамики По Клаузиусу: «Теплота никогда не переходит с более холодного тела на более горячее,
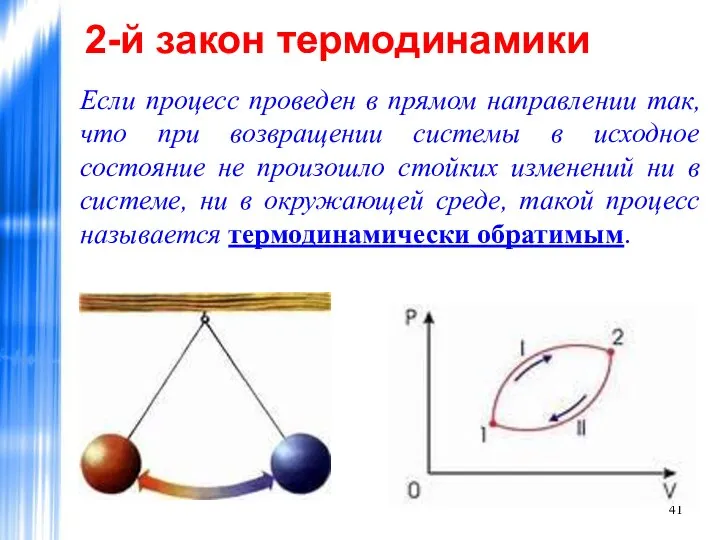
- 41. 2-й закон термодинамики Если процесс проведен в прямом направлении так, что при возвращении системы в исходное
- 42. 2-й закон термодинамики Если же изменения произошли, то процесс называется термодинамически необратимым. Термодинамически обратимый процесс состоит
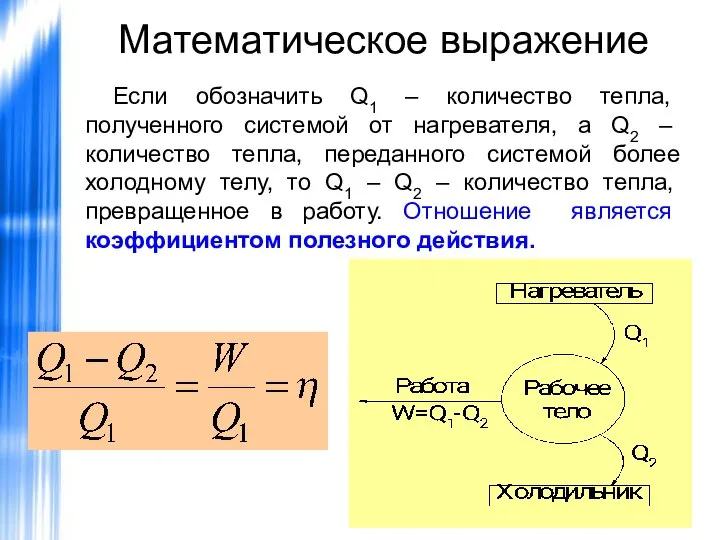
- 43. Математическое выражение Если обозначить Q1 – количество тепла, полученного системой от нагревателя, а Q2 – количество
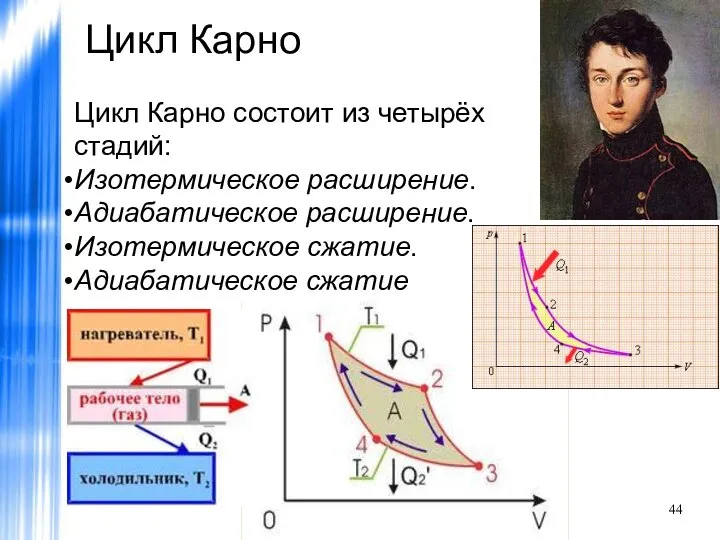
- 44. Цикл Карно Цикл Карно состоит из четырёх стадий: Изотермическое расширение. Адиабатическое расширение. Изотермическое сжатие. Адиабатическое сжатие
- 45. Математическое выражение 2-го начала термодинамики Поскольку или или «Алгебраическая сумма приведенных теплот обратимого цикла Карно равна
- 46. Математическое выражение 2-го закона термодинамики Все реальные самопроизвольные процессы – необратимые. Обратим только идеальный процесс. В
- 47. Фундаментальное уравнение термодинамики Заменяя δQ на выражение из первого начала термодинамики, получаем объединенное уравнение первого и
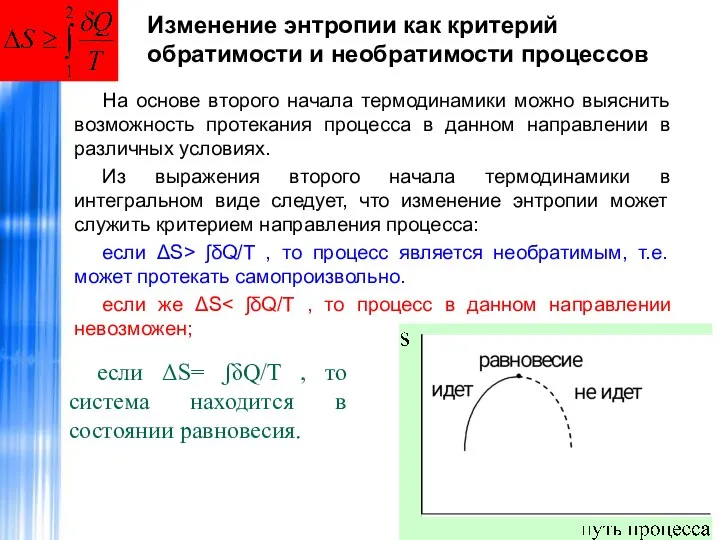
- 48. Изменение энтропии как критерий обратимости и необратимости процессов На основе второго начала термодинамики можно выяснить возможность
- 49. 2-й закон термодинамики Второй закон термодинамики справедлив для систем состоящих из большого количества частичек и носит
- 50. «Жизнь – это борьба с энтропией». А. Шредингер Энтропия связана с термодинамической вероятностью реализации данного состояния
- 51. 2-й закон термодинамики Следствие второго закона термодинамики: суммарное изменение энтропии, необходимое для формирования живого организма и
- 52. 2-й закон термодинамики - характера связи Sков. >Sмет. - чем сложнее химический состав, тем больше S.
- 53. называется приведенной теплотой, - связанной энергией. Абсолютное значение энтропии можно вычислить, исходя из постулата Планка, являющегося
- 54. Изобарно- изотермический потенциал или энергия Гиббса. На ход химической реакции могут влиять два фактора: энтальпийный ∆Н
- 55. Изобарно- изотермический потенциал или энергия Гиббса. Если ∆G 0 – процесс невозможен; обратный процесс идет самопроизвольно
- 57. Скачать презентацию















































 Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1)
Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1) Штучні і синтетичні волокна
Штучні і синтетичні волокна  Химиялық реакция белгілерін атаңыз
Химиялық реакция белгілерін атаңыз Металлы и сплавы с высокой удельной прочностью
Металлы и сплавы с высокой удельной прочностью Физические и химические явления
Физические и химические явления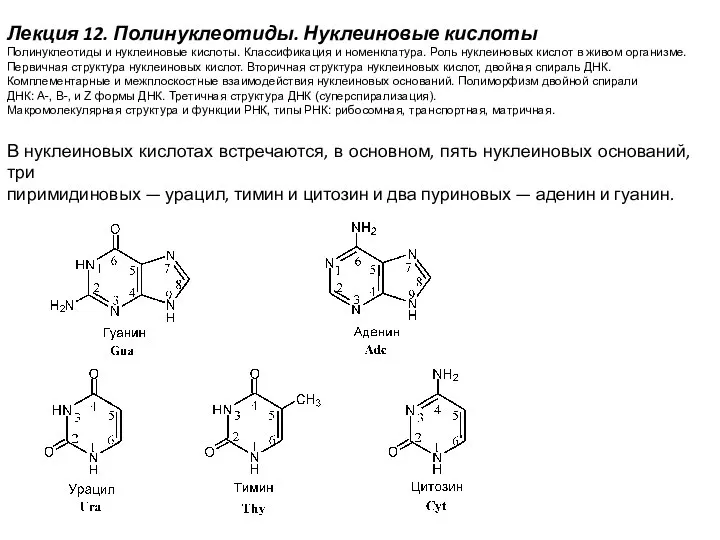 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты Выдающиеся ученые - химики и их заслуги
Выдающиеся ученые - химики и их заслуги Классификация моющих средств
Классификация моющих средств Узинская ООШ исслед.работа Лобановой Елизаветы
Узинская ООШ исслед.работа Лобановой Елизаветы Молярный объём газообразного вещества
Молярный объём газообразного вещества Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов Тыңайтқыштар
Тыңайтқыштар Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат
Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат Неидеальные растворы
Неидеальные растворы Introduction to metabolism
Introduction to metabolism Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов.
Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов. Алкены
Алкены Презентация Лекарства дома
Презентация Лекарства дома Химия (Органическая химия)
Химия (Органическая химия) Цикли трикарбонових кислот
Цикли трикарбонових кислот Алкадиены
Алкадиены Оксиды азота.
Оксиды азота. Общая химия, понятия
Общая химия, понятия Р-элементы IV группы: C, Si, Ge, Sn, Pb
Р-элементы IV группы: C, Si, Ge, Sn, Pb Основні класи неорганічних сполук
Основні класи неорганічних сполук Общая и неорганическая химия
Общая и неорганическая химия Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще
Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии
Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии