Содержание
- 2. Вопросы Основные определения 1 закон термодинамики 2 закон термодинамики Термодинамические потенциалы Методы определения термодинамических потенциалов Изменение
- 3. Основные определения Важнейшим свойством живых организмов является их способность улавливать, преобразовывать и запасать энергию в различных
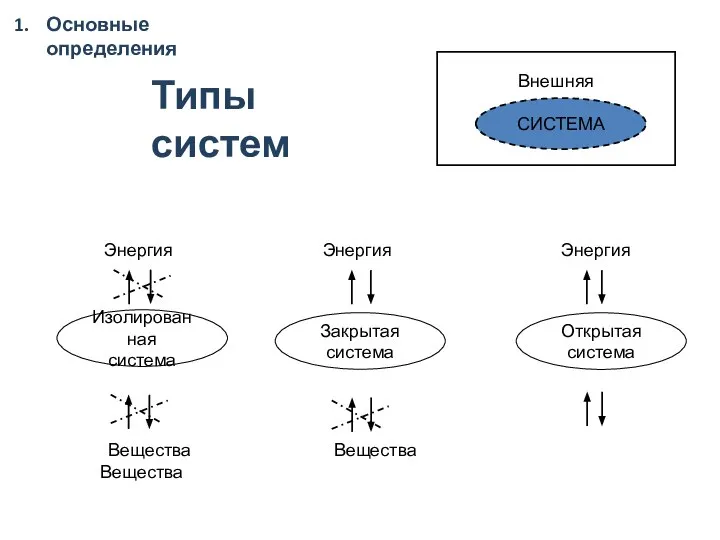
- 4. Основные определения Внешняя среда СИСТЕМА Энергия Энергия Энергия Изолированная система Закрытая система Открытая система Вещества Вещества
- 5. Основные определения Термодинамика стремится описать состояние системы с помощью макроскопических параметров состояния. Параметры состояния – физические
- 6. Основные определения Энергия (U, E, F, G, ΔU, dU, ΔE, dE, ΔF, dF, ΔG, dG) –
- 7. Основные определения Тепловая энергия – сумма кинетической энергии теплового, хаотического движения атомов и молекул вещества. Показатель
- 8. Основные определения Внутренняя энергия системы (U, ΔU, dU) – сумма кинетических и потенциальных энергий всех молекул,
- 9. Основные определения Энергия может накапливаться системой и передаваться от одной системы к другой. Есть 2 формы
- 10. Первый закон термодинамики Общая сумма энергии материальной системы остается постоянной величиной независимо от изменений, происходящих в
- 11. Первый закон термодинамики: Изменение внутренней энергии системы ΔU равно алгебраической сумме тепла ΔQ, переданного в ходе
- 12. Формулировка первого закона термодинамики для живых систем Первый закон термодинамики полностью применим к живым организмам. Для
- 13. Опытная проверка применимости первого закона для живых систем проводилась в специальных биокалориметрах, где измерялась теплота, выделенная
- 14. (1,2) - термометры для измерения температуры Н2О, протекающей по трубкам в камере; (3) – бак для
- 15. К – камера; Б – баллон с кислородом; Н – мотор, выкачивающий воздух из камеры; З
- 16. Определение энергоемкости питательных веществ, поступающих в организм 2. 1 закон термодинамики
- 17. Энергетический баланс человека в сутки Таким образом, живой организм не является источником новой энергии и первый
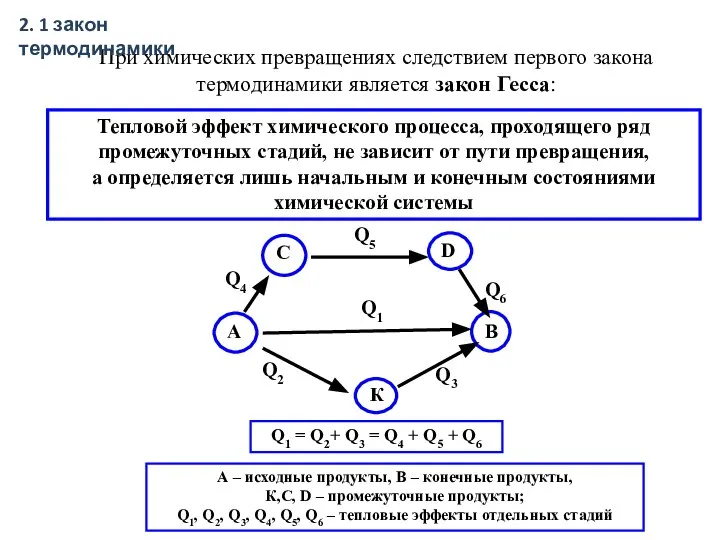
- 18. При химических превращениях следствием первого закона термодинамики является закон Гесса: Тепловой эффект химического процесса, проходящего ряд
- 19. Первый закон термодинамики Общая сумма энергии материальной системы остается постоянной величиной независимо от изменений, происходящих в
- 20. Первый закон термодинамики определяет количественные соотношения между различными формами энергии, которые принимают участие в определенном процессе.
- 21. Термодинамическое равновесие - такое состояние системы, когда изменения различных видов энергии выровнены, и способность системы совершать
- 22. Согласно второму закону термодинамики, состояние системы может быть описано особой функцией – энтропией S. Энтропия определяет
- 23. То есть, при обратимых процессах изменение энтропии равно нулю ΔS = 0, а при необратимых оно
- 24. Роль энтропии 1. Энтропия как мера рассеяния энергии при необратимых процессах Чем больше возрастание энтропии при
- 25. 3. Энтропия - мера упорядоченности системы S = k lnW - уравнение Планка-Больцмана где S -
- 26. Термодинамическая вероятность W – это количество микросостояний, возможных в пределах данного макросостояния. Величина W непосредственно связана
- 27. 4. Термодинамические потенциалы
- 28. Полное теплосодержание системы – энтальпия (H, ΔH, dH) – мера изменения теплоты системы, соответствует теплообмену при
- 29. Свободная энергия G – это способность системы совершать работу. Свободная энергия определяется как G = U
- 30. Общая формулировка второго закона термодинамики: Любой самопроизвольный процесс в изолированной системе приводит к уменьшению свободной энергии,
- 31. 5. Методы определения термодинамических потенциалов
- 32. 5. Методы определения термодинамических потенциалов
- 33. 5. Методы определения термодинамических потенциалов
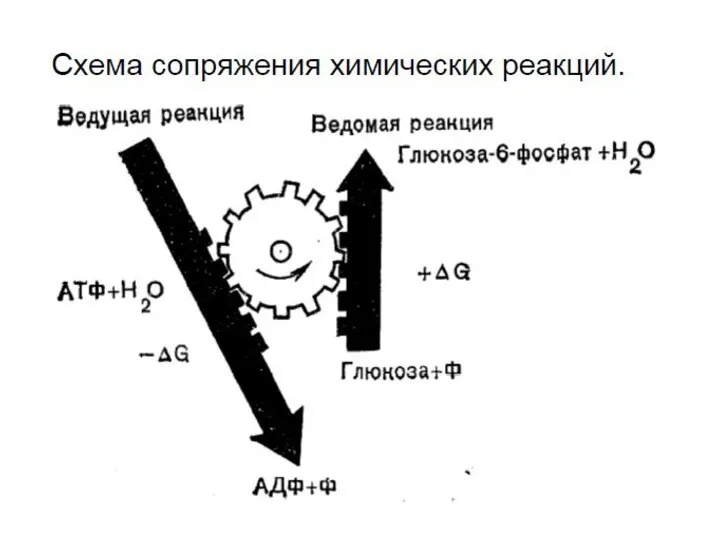
- 34. Организм, являясь открытой системой, получает энергию извне и запасает ее в виде богатых энергией соединений (АТФ).
- 35. 5. Методы определения термодинамических потенциалов
- 36. Общее изменение энтропии dS открытой системы может происходить независимо либо за счет процессов обмена с внешней
- 37. Стационарное состояние биосистем Особенностью биосистем является то, что они не просто открытые системы, но системы, находящиеся
- 38. 7. Стационарное состояние открытой системы
- 39. 7. Стационарное состояние открытой системы
- 40. В стационарном состоянии скорость возрастания энтропии, обусловленного протеканием необратимых процессов, имеет положительное и минимальное из возможных
- 41. Второй закон термодинамики для живых систем Cкорость изменения энтропии ΔS в организме равна алгебраической сумме скоростей
- 45. 8. Информация и энтропия Информация I = - log2 P В качестве единицы информации I принимают
- 47. Скачать презентацию









































 Водородная связь
Водородная связь Лекция 6. Химическая кинетика
Лекция 6. Химическая кинетика Взаимодействие в двухкомпонентных системах. Примитивные виды взаимодействия: без промежуточных фаз
Взаимодействие в двухкомпонентных системах. Примитивные виды взаимодействия: без промежуточных фаз Алканы. Пропан - С3Н8
Алканы. Пропан - С3Н8 Окислительно-восстановительные равновесия и процессы
Окислительно-восстановительные равновесия и процессы Установка изомеризации пентан гексановой фракции
Установка изомеризации пентан гексановой фракции Вклад ученых Казахстана в развитие органической химии
Вклад ученых Казахстана в развитие органической химии Номенклатура органических соединений. Структурные формулы соединений. Алканы. (Лабораторная работа 2)
Номенклатура органических соединений. Структурные формулы соединений. Алканы. (Лабораторная работа 2) Радиоактивный распад. Чернобыль
Радиоактивный распад. Чернобыль Учитель химии МБОУ СОШ №79 г. о. Самара Язрикова Любовь Михайловна
Учитель химии МБОУ СОШ №79 г. о. Самара Язрикова Любовь Михайловна В земное недро ты, химия, Проникни взора остротой, И, что содержит в нем Россия, Драги сокровища открой. М.В.Ломоносов
В земное недро ты, химия, Проникни взора остротой, И, что содержит в нем Россия, Драги сокровища открой. М.В.Ломоносов Строение и функции отдельных коферментов
Строение и функции отдельных коферментов Настольная образовательная игра по химии. Мастер - класс
Настольная образовательная игра по химии. Мастер - класс Сarbonyl compounds. Carboxylic acids. Lipids
Сarbonyl compounds. Carboxylic acids. Lipids Ртуть
Ртуть Презентация по Химии "Щелочные металлы" - скачать смотреть бесплатно__
Презентация по Химии "Щелочные металлы" - скачать смотреть бесплатно__ Строение гетероциклических соединений
Строение гетероциклических соединений Дисперсные (коллоидные) системы и растворы
Дисперсные (коллоидные) системы и растворы Получение наночастиц в сверхкритическом флюиде
Получение наночастиц в сверхкритическом флюиде Свойства фенола
Свойства фенола Ковалентная химическая связь
Ковалентная химическая связь Полудрагоценные камни
Полудрагоценные камни Кислоты с металлами
Кислоты с металлами Мониторинги по химии
Мониторинги по химии IV группа. Главная подгруппа. Кремний
IV группа. Главная подгруппа. Кремний Аттестационная работа. Рабочая программа внеурочной деятельности. Проектная деятельность по химии
Аттестационная работа. Рабочая программа внеурочной деятельности. Проектная деятельность по химии Материаловедение
Материаловедение Типы химических реакций
Типы химических реакций